Механизмы развития (патогенез) мегалобластной анемии
Причины анемий, возникающих в результате нарушения продукции эритроцитов, гетерогенны. Эти анемии можно классифицировать на несколько больших категорий, основываясь на патофизиологических критериях. Наиболее широко распространены и важны анемии, ассоциированные со снижением продукции эритроцитов, обусловленным дефицитом питания.
За ними следуют анемии, возникающие вторично на фоне почечной недостаточности и хронического воспаления. Менее частой причиной анемий служат расстройства, приводящие к генерализованной недостаточности костного мозга, такие как апластическая анемия, первичные гемопоэтические неоплазии и инфильтративные нарушения, которые вызывают замещение костного мозга (например, метастазирующие опухоли и диссеминированное гранулематозное заболевание).
Вначале будут рассмотрены внешние причины сниженного эритропоэза, а затем — внутренние причины неопухолевой природы.
Основным признаком мегалобластных анемий, возникающих по различным причинам, служит нарушение синтеза ДНК, приводящее к характерным морфологическим изменениям, включая присутствие аномально крупных эритроидных клеток-предшественников и эритроцитов. Вначале будут рассмотрены общие признаки мегалобластных анемий, а затем — два основных типа анемий: пернициозная анемия (основная форма анемий, обусловленных дефицитом витамина B12) и анемия вследствие дефицита фолиевой кислоты.
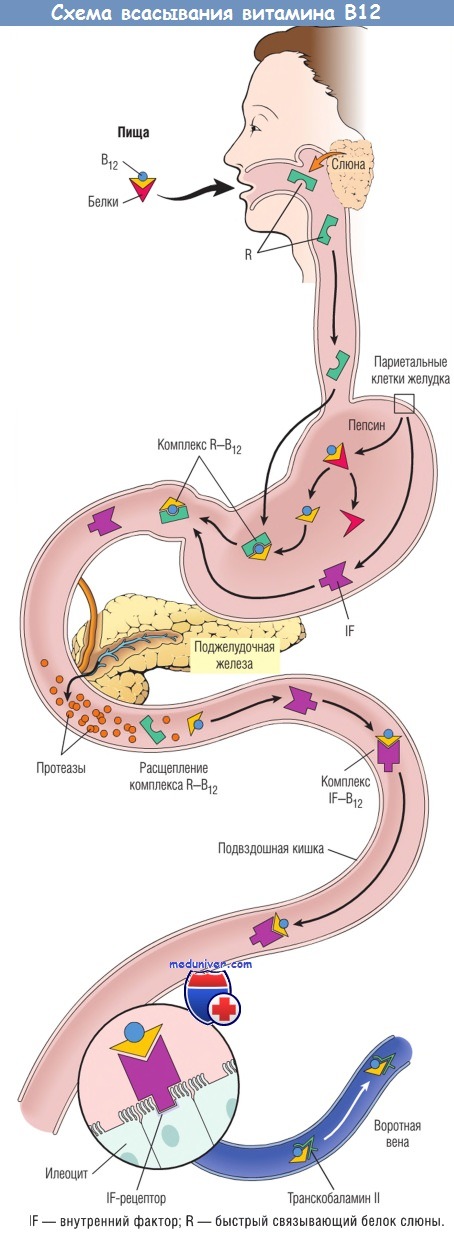
Некоторые метаболические функции витамина В12 и фолиевой кислоты будут обсуждены далее. Здесь же достаточно указать, что витамин B12 и фолиевая кислота являются коферментами, необходимыми для синтеза тимидина, входящего в состав ДНК. Дефицит витамина В12 и фолиевой кислоты или нарушения их метаболизма влекут за собой дефект созревания ядра вследствие нарушения синтеза ДНК, что приводит к замедлению или остановке клеточного деления.

Морфология. Некоторые изменения периферической крови являются общими для всех мегалобластных анемий. Весьма характерный признак — это присутствие макроцитарных овальных эритроцитов (макроовалоцитов). Эти клетки крупнее нормальных и содержат много гемоглобина, у большинства макроовалоцитов отсутствует центральное просветление, свойственное нормальным эритроцитам.
Клетки даже выглядят гиперхромными, однако средняя концентрация гемоглобина в эритроцитах не повышена. Существуют заметные различия размера (анизоцитоз) и формы (пойкилоцитоз) эритроцитов. Количество ретикулоцитов невелико. Иногда, в случае тяжелой анемии, в циркулирующей крови появляются ядросодержащие клетки-предшественники эритроцитов. Нейтрофилы также крупнее нормальных (макрополиморфно-ядерные клетки) и гиперсегментированы с 5 или более ядерными сегментами вместо обычных 3-4.
Клеточность костного мозга, как правило, повышена в результате увеличения количества гемопоэтических клеток-предшественников, которые часто полностью замещают жировую ткань костного мозга. Мегалобластные изменения присутствуют на всех стадиях развития эритроцитов. Большинство примитивных клеток (промегалобластов) крупные, с интенсивно базофильной цитоплазмой, хорошо заметными ядрышками и своеобразной тонкой структурой ядерного хроматина.
По мере дифференцировки этих клеток и начала накопления гемоглобина ядро сохраняет свой тонко распределенный хроматин без образования глыбчатого пикнотического хроматина, типичного для нормобластов. В то время как созревание ядра замедлено, созревание цитоплазмы и накопление гемоглобина происходят с нормальной скоростью, что приводит к асинхронному ядерно-цитоплазматическому развитию.
Поскольку синтез ДНК нарушен во всех пролиферирующих клетках, созревание клеток-предшественников гранулоцитов также нарушается и они становятся гигантскими метамиелоцитами и клетками с палочковидным ядром. Мегакариоциты также могут быть аномально крупными, с причудливым многодольчатым ядром.
Гиперплазия костного мозга — реакция организма на повышение уровней факторов роста, в частности эритропоэтина. Однако нарушения синтеза ДНК приводят к тому, что в костном мозге апоптозу подвергается большинство клеток-предшественников (пример неэффективного гемопоэза), вследствие чего развивается панцитопения, а анемия усиливается вследствие слабого гемолиза эритроцитов неясной этиологии.
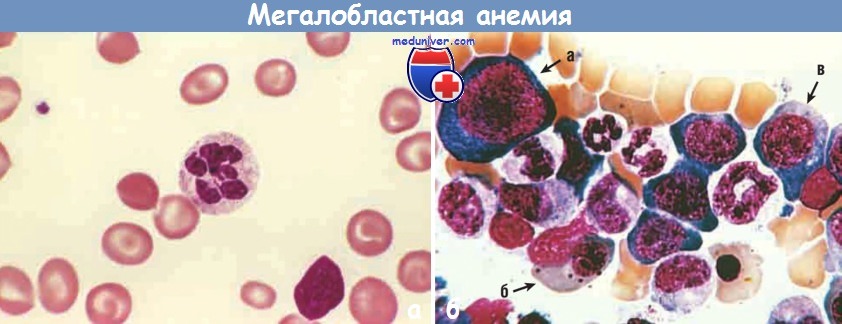
Виден гиперсегментированный нейтрофил, ядро которого состоит из 6 сегментов.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) пернициозной анемии"
Оглавление темы "Патогенез анемий":- Механизмы развития (патогенез) серповидно-клеточной анемии
- Механизмы развития (патогенез) бета-талассемии
- Механизмы развития (патогенез) альфа-талассемии
- Механизмы развития (патогенез) пароксизмальной ночной гемоглобинурии
- Механизмы развития (патогенез) иммуногемолитической анемии
- Механизмы развития (патогенез) мегалобластной анемии
- Механизмы развития (патогенез) пернициозной анемии
- Механизмы развития (патогенез) анемии при дефиците фолиевой кислоты
- Механизмы развития (патогенез) железодефицитной анемии
- Механизмы развития (патогенез) анемии из-за хронического заболевания

