Гипопластическая и апластическая анемии. Анемия вследствие нарушения синтеза глобиновых ДНК.
Гипо- и апластические анемии, развивающиеся в результате преимущественного повреждения стволовых клеток, являются результатом подавления функции костного мозга. По происхождению эти анемии подразделяют на первичные и вторичные.
• К первичным дизэритропоэтическим анемиям относится анемия Фанкони.
• Вторичные (приобретённые) — гипо- и апластические — дизэритропоэтические анемии обычно являются результатом действия одного или нескольких факторов: физической природы (например, ионизирующего облучения), химической природы (чаще всего ЛС, например, левомицетина, бутадиона, иммунодепрессантов, мепробамата, аминазина, цитостатиков и др.), биологической природы (главным образом вирусов, например, вызывающих гепатит, инфекционный мононуклеоз и др., а также антиэритроцитарных AT и Т-цитотоксических лимфоцитов).
Патогенез гипопластических анемий
- Высокие дозы ионизирующей радиации обусловливают гипоплазию костного мозга. Выраженность её зависит от дозы облучения. В основе гипоплазии кроветворной ткани лежат необратимое повреждение и гибель стволовых клеток, вплоть до их полного исчезновения, наблюдающегося при аплазии.
- Химические и биологические факторы (например, вирусы и ЛС) тормозят синтез нуклеиновых кислот и белка в стволовых клетках, нарушают клеточное и/или физико-химическое микроокружение стволовых клеток, что ведёт к расстройствам механизма их пролиферации, повреждают и вызывают гибель стволовых клеток в связи с образованием иммунных лимфоцитов и/или AT.
Любой из указанных механизмов (или их комбинация) обусловливает нарушение пролиферации и/или гибель стволовых гемопоэтических клеток, включая эритропоэтические. Это и ведёт к развитию гипо- или апласти-ческих анемий.
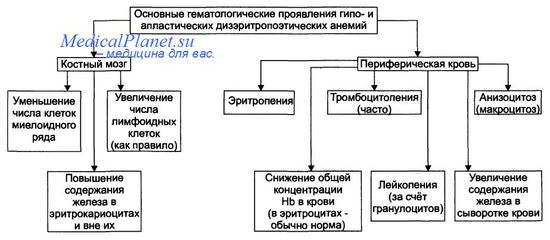
Проявления гипопластических анемий. Один родителей отмечает, что для гипо- и апластических анемий характерны следующие изменения костного мозга и периферической крови.
Клинические проявления гипопластических анемий (в связи с указанными изменениями): признаки гипоксии (недомогание, слабость, гиподинамия, головная боль, быстрая утомляемость и др.), частые кровотечения и кровоизлияния (обусловленные снижением свёртываемости крови) и высокая заболеваемость инфБ (наблюдается у пациентов с лимфопенией).
Анемия вследствие нарушения синтеза глобиновых ДНК
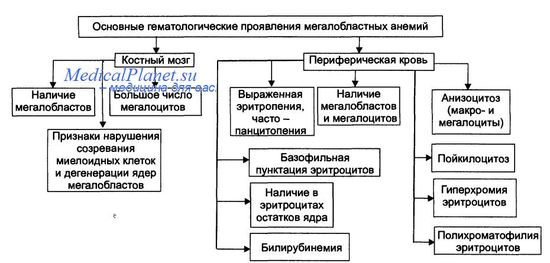
Анемии вследствие нарушения синтеза глобиновых ДНК — как правило, гиперхромные макроцитарные анемии с мегалобластным типом кроветворения. Мегалобластный эритропоэз возникает вследствие нарушения синтеза ДНК в условиях дефицита витамина В12 (цианкобаламина) или фолиевой кислоты, а также при недостаточности метионин синтетазы и дигидрофолатредуктазы. При макроцитарнои мегалобластнои анемии эритроидныи росток костного мозга представляют аномальные эритроидные клетки — мегалобласты. В эту группу анемий входят пернициозная анемия и другие В12-дефицитные анемии, а также фолиеводефицитная анемия. Эти анемии протекают тяжело и трудно поддаются лечению. Именно поэтому мегалобластные анемии ранее называли пернициозными (витамин В12-дефицитные анемии, в том числе анемия Аддисона— Бирмера).
• Патогенез мегалобластных анемий см. в статьях «Анемии витамин В12-дефицитные», «Анемия фолиеводефицитная», «Витамин В12», «Гиповитаминоз В12», «Кислота фолиевая», «Недостаточность фолиевой кислоты».
• Проявления мегалобластных анемий приведены на рисунке.
- Читать далее "Обмен железа в организме. Значение железа."
Оглавление темы "Эритроциты. Эритремии. Анемии.":1. Эритроциты. Обмен гемоглобина. Эритроцитозы. Виды эритроцитозов.
2. Проявления эритремии. Признаки эритроцитозов.
3. Вторичные эритроцитозы. Виды и признаки вторичных эритроцитозов.
4. Анемия. Что такое анемия? Виды анемий.
5. Механизм развития анемий. Острая постгеморрагическая анемия.
6. Хронические постгеморрагические анемии. Гемолитические анемии. Классификация гемолитических анемий.
7. Механизм развития гемолитических анемий. Патогенез гемолитических анемий.
8. Проявления гемолитических анемий. Лечение гемолитических анемий. Дизэритропоэтические анемии.
9. Гипопластическая и апластическая анемии. Анемия вследствие нарушения синтеза глобиновых ДНК.
10. Обмен железа в организме. Значение железа.

