Метод флюоресцентной гибридизации амниотической жидкости in situ. Сенсебилизация после амниоцентеза
Известно, что для получения результатов цитогенетического анализа требуется от 10 до 16 дней. До недавнего времени FISH-метод использовался в качестве вспомогательного диагностического исследования для быстрой диагностики наиболее часто встречающихся хромосомных аберраций. Для его проведения не требуется культивации амниоцитов, поскольку анализ основан на специфической гибридизации определенных участков хромосом с флуоресцентно-меченными зондами и позволяет определять их структурные перестройки и выявлять число копий хромосом 13, 18, 21, а также X и Y в интерфазных ядрах.
A. Morris et al. опубликовали результаты проспективных исследований с использованием FISH-метода для быстрого (без культивирования) цитогенетического анализа. Из 1504 протестированных образцов амниотической жидкости в 1467 наблюдениях было правильно индентифициро-вано нормальное количество хромосом 21 (дисомия) в кариотипе и в 35 наблюдениях диагностирована трисомия. Только в 2-х наблюдениях не удалось осуществить диагностику.
В среднем для получения результатов требовалось около 48 ч (от 1 до 7 дней). Эти данные не противоречат полученным В. Eiben et al., у которых точность правильного установления нормального кариотипа плода составила 98% (727 из 741) и аномального кариотипа - 95,5% (68 из 71). Преимуществами FISH-метода по сравнению с обычно используемыми являются возможность проведения анализа при наличии небольшого количества амниотической жидкости, а также точность и быстрота получения результатов (в течение 24 ч) в отношении наиболее часто встречающихся видов хромосомной патологии.
Эти преимущества приобретают особую ценность при выполнении амниоцентеза в первом триместре беременности. К сожалению, возможности метода ограничиваются набором имеющихся зондов, в связи с чем многие другие структурные и количественные хромосомные аберрации пока не могут быть диагностированы с его помощью. Другой особенностью метода является необходимость подготовки специально обученных врачей для его проведения.
До настоящего времени американский университет медицинской генетики продолжает рассматривать FISH-гибридизацию в качестве экспериментального метода и не рекомендует определять клиническую тактику ведения беременной, основываясь исключительно на его результатах. Однако в некоторых медицинских учреждениях считается допустимым принимать окончательное решение о характере дальнейшего ведения пациенток даже до получения результатов окончательного цитогенетического анализа, если во втором триместре беременности обнаруживаются соответствующие ультразвуковые маркеры хромосомной патологии плода в сочетании с информативными результатами диагностики с помощью FISH-метода.
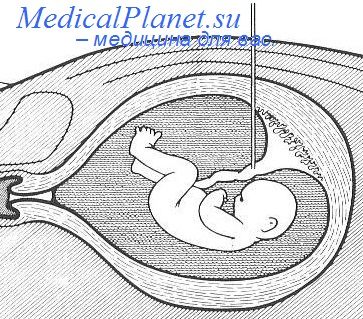
Возникновение сенсибилизации после амниоцентеза
Известно, что эритроциты резус-положительного плода содержат на своей поверхности D-антиген, который вызывает появление антител у матерей с резус-отрицательной кровью после плодово-материнской трансплацентарной трансфузии во втором триместре. Это явление может происходить самопроизвольно при физиологически протекающей беременности или после амниоцентеза. Всемирная организация здравоохранения (ВОЗ) и Американский университет акушерства и гинекологии рекомендуют вводить иммуноглобулин анти-D всем беременным после амниоцентеза во втором триместре. До настоящего времени дискутируются вопросы, связанные с необходимой дозой препарата: по рекомендациям ВОЗ для профилактики считается достаточным 50 мкг, а по американским стандартам следует вводить 300 мкг.
Основой для данной рекомендации послужило то, что проведение процедуры сопровождается повышением частоты трансплацентарных кровотечений, которые являются фактором риска для возникновения сенсибилизации. Однако степень этого риска пока остается не уточнена окончательно. Частота развития резус-сенсибилизации по данным рандомизированного контролируемого исследования, выполненного A. Tabor et al., составила 0,3% (7 из 370) в основной группе и 0,1% (3 из 347) в контрольной группе женщин с резус-отрицательной кровью (всем пациенткам из основной группы после амниоцентеза вводили профилактическую дозу иммуноглобулина анти-D).
Эти различия оказались недостоверны, однако, если бы число пациенток достигало в каждой группе 2896, различие между ними было бы на уровне 1%. По предварительным данным можно предположить, что амниоцентез является фактором риска в отношении возникновения сенсибилизации беременной примерно в 1% случаев.
J.C. Murray et al. провели сравнительный анализ преимуществ и недостатков профилактического использования иммуноглобулина анти-D. Возражения против рутинного назначения этого препарата основываются на предположениях о недоказанности его эффективности (описаны отдельные случаи возникновения сенсибилизации при введении иммуноглобулина анти-D) и отсутствии сведений о его безопасности в отдаленном периоде. Иммуноглобулин проникает через плаценту и может взаимодействовать с резус-положительными эритроцитами плода, а неблагоприятные эффекты такого воздействия пока остаются невыяснены.
Теоретически можно предположить увеличение риска заболевания. Это может быть связано с активацией иммунной системы в ответ на невысокую концентрацию антител в крови (по принципу обратной связи). Кроме того, неизвестны отдаленные результаты воздействия вводимых человеческих антител на иммунологически «наивные» клетки иммунной системы развивающегося плода.
Несмотря на отсутствие неопровержимых доказательств эффективности использования иммуноглобулинов антирезус в профилактических целях, назначение их после амниоцентеза во втором триместре беременности в настоящее время является рутинной практикой в США.
- Читать далее "Ранний амниоцентез. Риски и преимущества раннего амниоцентеза"
Оглавление темы "Особенности амниоцентеза. Диагностика внутриутробного инфицирования":1. Метод флюоресцентной гибридизации амниотической жидкости in situ. Сенсебилизация после амниоцентеза
2. Ранний амниоцентез. Риски и преимущества раннего амниоцентеза
3. Культивирование амниотических клеток. Амниофильтрация при раннем амниоцентезе
4. Амниоцентез при многоплодной беременности. Техника амниоцентеза при двойне
5. Методика однократного введения иглы при амниоцентезе. Трудности амниоцентеза при многоплодной беременности
6. Прерывание многоплодной беременности после амниоцентеза. Внутриутробное инфицирование плода
7. Стадии внутриутробного инфицирования плода. Частота внутриутробного инфицирования
8. Диагностика внутриутробного инфицирования. Амниоцентез при внутриутробном инфицировании
9. Окраска околоплодных вод акридиновым оранжевым. Лимулиновый тест околоплодных вод
10. Подсчет лейкоцитов в околоплодных водах. Определение глюкозы в амниотической жидкости

