Механизм развития (патогенез) аденокарциномы толстой кишки
Аденокарцинома толстой кишки — самая частая злокачественная опухоль ЖКТ, а также основная причина заболеваемости и летальности во всем мире. Напротив, в тонкой кишке, доля которой составляет 75% всей длины ЖКТ, крайне редко наблюдаются доброкачественные и злокачественные опухоли. В тонкой кишке практически с равной частотой развиваются аденокарциномы и нейроэндокринные опухоли, реже возникают лимфомы и саркомы.
а) Эпидемиология. Ежегодно в США регистрируют более 130 тыс. новых случаев аденокарциномы толстой кишки и 55 тыс. смертей, связанных с нею. Это составляет 15% всех летальных исходов, обусловленных злокачественной опухолью, и является второй по частоте причиной смерти после рака легкого.
Пик заболеваемости приходится на возраст 60-70 лет, лишь менее 20% случаев заболевания наблюдаются в возрасте до 50 лет. Мужчины страдают аденокарциномой толстой кишки немного чаще, чем женщины. Аденокарцинома толстой кишки больше всего распространена в США, Канаде, Австралии, Новой Зеландии, Дании, Швеции и других развитых странах. Заболеваемость этой формой рака в 30 раз ниже в Индии, Южной Америке и Африке.
Однако в Японии, где заболеваемость раньше была низкой, в настоящее время отмечается рост до промежуточного уровня (сходного с таковым в Великобритании), вероятно в результате изменения образа жизни и диеты.
Особенностями диеты, влияющими на заболеваемость раком толстой кишки, являются низкое потребление клетчатки и высокое потребление рафинированных углеводов и жиров. Однако причины взаимосвязи между диетой и риском недостаточно понятны. Предполагается, что снижение потребления клетчатки уменьшает скорость продвижения каловых масс и нарушает состав кишечной микрофлоры. Эти изменения могут приводить к накоплению потенциально токсичных побочных продуктов метаболизма бактерий, которые в течение длительного времени контактируют со слизистой оболочкой толстой кишки.
Дефицит витаминов А, С и Е, нейтрализующих свободные радикалы, может усиливать повреждение, вызванное продуктами перекисного окисления. Высокое потребление жиров увеличивает синтез холестерина и желчных кислот в печени, которые под действием кишечных бактерий могут трансформироваться в канцерогены.
Кроме последствий изменения рациона питания областью интереса исследователей является фармакологическая профилактика. Результаты некоторых эпидемиологических исследований позволяют предположить, что ацетилсалициловая кислота и другие НПВС обладают протективным эффектом в отношении рака толстой кишки. Это согласуется с данными других исследований, которые показали, что некоторые НПВС вызывают регрессию полипов у тех пациентов с НАП, у которых прямая кишка не была удалена во время резекции ободочной кишки.
Предполагается, что такой эффект — следствие подавления активности фермента СОХ-2, высокая экспрессия которой определяется в 90% карцином толстой кишки и в 40-90% аденом толстой кишки. СОХ-2 необходима для выработки простагландина Е2, который стимулирует пролиферацию эпителия, особенно после его повреждения. Интересно, что экспрессия СОХ-2 регулируется TLR4, который распознает липополисахариды и также избыточно экспрессируется в аденомах и карциномах.
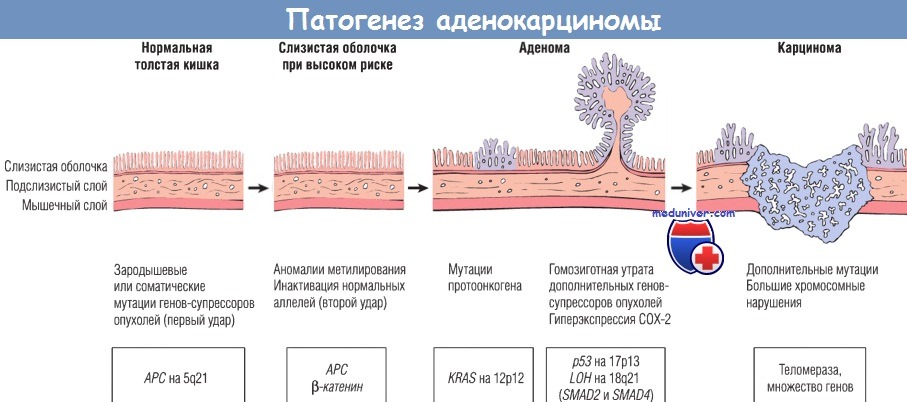
Предполагается, что на начальных этапах происходит утрата одного аллеля гена-супрессора опухолей АРС.
Человек может иметь один мутантный аллель уже при рождении, что делает его предрасположенным к развитию рака толстой кишки, или же инактивация гена АРС происходит позднее.
Согласно гипотезе «два удара», это является первым ударом. Затем происходит утрата второго аллеля АРС (второй удар).
Другие мутации, включая мутации KRAS и делеции в 18q21, вовлекающие SMAD2 и SMAD4, а также инактивация гена-супрессора опухолей р53 приводят к развитию карциномы с дополнительными мутациями.
Наиболее критичным является именно накопление мутаций, а не их появление в определенном порядке (хотя мутации развиваются последовательно).
СОХ — циклооксигеназа.
б) Патогенез. Исследования патогенеза рака толстой кишки обеспечили фундаментальное понимание общих механизмов эволюции злокачественной опухоли. Далее рассмотрим концепции, специфичные для патогенеза рака толстой кишки.
Молекулярные события, приводящие к развитию аденокарциномы толстой кишки, являются гетерогенными и включают генетические и эпигенетические нарушения. Описано 2 различных генетических пути канцерогенеза в толстой кишке. Первый — это путь АРС/b-катенина, который связан с геном WNT и классической последовательностью аденома-карцинома. Второй — путь микросателлитной нестабильности, который связан с дефектом системы репарации ДНК. Оба пути приводят к постепенному накоплению многочисленных мутаций, но вовлеченные гены и механизмы, посредством которых накапливаются мутации, различны.
Эпигенетические нарушения, самым частым из которых является сайленсинг, индуцированный метилированием, могут усиливать прогрессирование процесса по обоим путям.
Классическая последовательность аденомакарцинома, которая наблюдается почти в 80% спорадических опухолей толстой кишки, обычно обусловлена мутациями АРС на ранних стадиях опухолевого процесса. Для развития аденомы обе копии гена АРС должны быть функционально неактивными как вследствие мутации, так и из-за эпигенетических воздействий. АРС служит ключевым отрицательным регулятором b-катенина, являющегося компонентом сигнального пути WNT. В норме белок АРС связывается b-катенином и вызывает его разрушение. При утрате функции АРС b-катенин накапливается и переносится в ядро, где активирует транскрипцию генов MYC и циклина D1, которые активируют пролиферацию.
Последующие дополнительные мутации, включая активирующие мутации гена KRAS, приводят к активации роста и препятствуют апоптозу клеток. Мутация KRAS является последним событием в цепи канцерогенеза. Это подтверждается тем, что эти мутации присутствуют только в 10% аденом диаметром менее 1 см, но обнаруживаются в 50% аденом диаметром более 1 см и в 50% инвазивных аденокарцином. Прогрессирование опухоли также сопровождается мутациями других генов-супрессоров опухолей — SMAD2 и SMAD4, которые являются эффекторами сигнального пути TGF-p. Поскольку сигнал TGF-b в норме подавляет клеточный цикл, утрата этого гена может приводить к неконтролируемому клеточному росту.
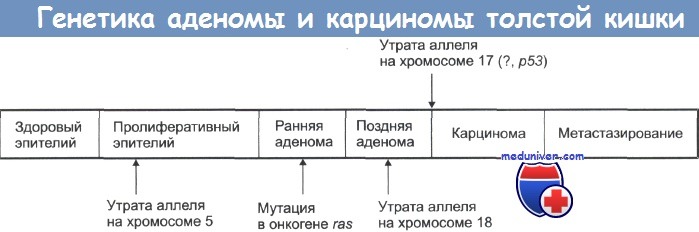
Мутации гена-супрессора опухолей р53 определяются в 70-80% случаев рака толстой кишки, но редко наблюдаются при аденомах, позволяя предположить, что мутации р53 возникают на поздних этапах прогрессирования опухоли. Причиной утраты функций р53 и других генов-супрессоров опухолей часто являются делеции, указывающие на то, что хромосомная нестабильность — типичный признак пути АРС/Р-катенина. Активность генов-супрессоров опухолей может подавляться также метилированием островка CpG, который представляет 5'-нетранслируемый участок некоторых генов, включающий промотор и зону начала транскрипции. На более поздних стадиях опухолевого процесса повышается экспрессия теломеразы.
У пациентов с нарушением работы системы репарации ошибок репликации ДНК вследствие утраты генов, исправляющих эти ошибки, в микросателлитных последовательностях накапливаются мутации. Такое состояние называют микросателлитной нестабильностью (мутаторным фенотипом). Эти мутации, как правило, являются «молчащими», т.к. микросателлиты обычно расположены в некодирующих участках ДНК.
Однако некоторые микросателлитные последовательности располагаются в кодирующем участке или промоторной зоне генов, участвующих в регуляции клеточного роста, например генов рецептора TGF-b II типа и проапоптотического белка ВАХ. Поскольку TGF-b подавляет пролиферацию эпителиальных клеток толстой кишки, мутантные рецепторы TGF-b II типа могут способствовать бесконтрольному клеточному росту, а утрата ВАХ может повышать выживаемость генетически аномальных клеточных клонов. Мутации онкогена BRAF и сайленсинг различных групп генов вследствие гиперметилирования островка CpG также часто определяются в клетках злокачественной опухоли, развивающейся в результате нарушений работы системы репарации ошибок репликации ДНК. Напротив, мутации KRAS и р53 нетипичны для таких опухолей.
Таким образом, комбинация микросателлитной нестабильности, мутации BRAF и метилирования специфических мишеней, таких как MLH1, являются отличительными признаками этого пути канцерогенеза.
Существует группа злокачественных опухолей толстой кишки с повышенным метилированием островка CpG при отсутствии микросателлитной нестабильности. Многие из таких опухолей имеют мутации KRAS, но мутации р53 и BRAF присутствуют редко. Напротив, мутации р53 часто обнаруживаются в злокачественных опухолях толстой кишки, которые не сопровождаются метилированием островка CpG.
Морфологически невозможно определить молекулярные изменения, которые приводят к канцерогенезу, однако есть определенные связи между морфологией опухоли, нарушением работы системы репарации ошибок репликации ДНК и микросателлитной нестабильностью. Такие нарушения часто выявляют в плоских зубчатых аденомах. В инвазивных карциномах с микросателлитной нестабильностью нередко обнаруживают обширные участки муцинозной дифференцировки и лимфоцитарную инфильтрацию вокруг ткани опухоли. Такие опухоли, так же как и опухоли с метилированием островка CpG, часто локализуются в проксимальном отделе ободочной кишки.
Опухоли с микросателлитной нестабильностью можно определить по отсутствию иммуногистохимической реакции с антителами к белкам системы репарации повреждений ДНК или с помощью молекулярно-генетического анализа микросателлитных последовательностей.
Важно идентифицировать опухоли, относящиеся к HNPCC, поскольку наличие генетических нарушений повышает риск вторичной малигнизации толстой кишки и других органов, а в некоторых случаях определяет прогноз и лечение.
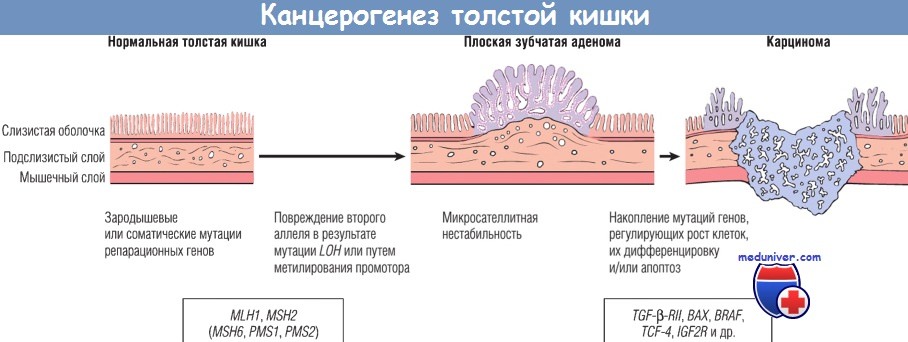
Дефекты репарационных генов приводят к микросателлитной нестабильности и способствуют накоплению мутаций в многочисленных генах.
Если эти мутации затрагивают гены, регулирующие рост клеток, их дифференцировку и/или апоптоз, может развиться злокачественная опухоль.
в) Морфология. Аденокарциномы практически с одинаковой частотой поражают все отделы толстой кишки. Опухоли проксимальных отделов толстой кишки обычно растут в виде полиповидных экзофитных масс, распространяющихся вдоль одной стенки слепой кишки или восходящей ободочной кишки. Такие опухоли редко приводят к кишечной непроходимости. Напротив, опухоли дистальных отделов толстой кишки обычно имеют вид кольцевидных образований и приводят к сужению просвета кишки, а иногда — к кишечной непроходимости. В обоих случаях опухоли со временем прорастают в стенку толстой кишки и при пальпации определяются в виде плотных масс. Общие гистологические характеристики аденокарцином дистального и проксимального отделов толстой кишки сходны. Большинство опухолей состоят из высоких цилиндрических клеток, напоминающих диспластичный эпителий, обнаруживаемый в аденомах.
Инвазивный компонент этих опухолей вызывает выраженную десмопластическую реакцию стромы, которая и обеспечивает характерную плотную консистенцию. Некоторые низкодифференцированные опухоли формируют всего несколько желез, другие могут продуцировать слизь, которая накапливается в стенке кишки. Такие аденокарциномы имеют плохой прогноз. Опухоли также могут состоять из перстневидных клеток, сходных с таковыми в аналогичных опухолях желудка.
В других опухолях могут определяться признаки нейроэндокринной дифференцировки.
г) Клинические признаки. Доступность эндоскопического скрининга в сочетании с накопленными знаниями о том, что аденокарциномы развиваются из аденом, дает уникальную возможность для предотвращения рака толстой кишки. Однако эта опухоль развивается бессимптомно, поэтому может быть не распознана в течение длительного времени. Обычно раньше других манифестируют аденокарциномы слепой кишки и других отделов восходящей ободочной кишки, проявляясь повышенной утомляемостью и общей слабостью вследствие железодефицитной анемии. Согласно клиническому правилу, причиной железодефицитной анемии у пожилых мужчин или женщин в постменопаузе является рак ЖКТ, если не доказано обратное. Аденокарциномы в дистальном отделе толстой кишки могут вызвать скрытое кровотечение, кишечный дискомфорт или спазмы в области левого нижнего квадранта живота.
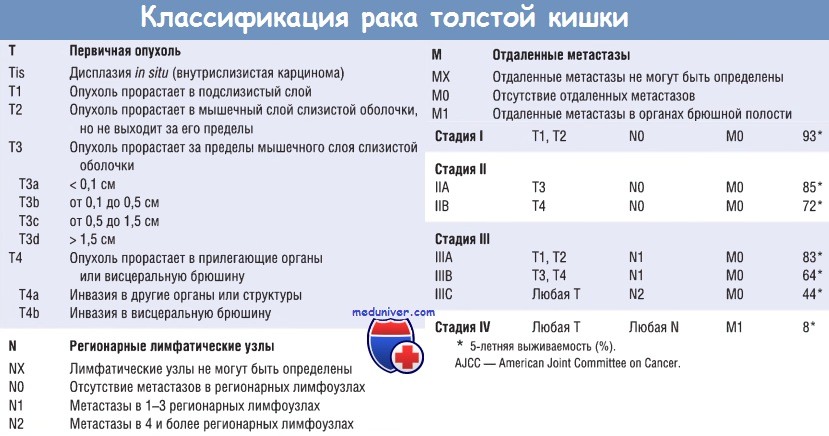
Низкодифференцированные опухоли и опухоли с муцинозной дифференцировкой имеют неблагоприятный прогноз, определяемый двумя наиболее значимыми факторами — глубиной инвазии опухоли и наличием метастазов в лимфоузлах. Инвазия в мышечную оболочку и метастазы в лимфатических узлах значительно снижают выживаемость. Эти прогностические факторы были впервые описаны Дюксом и Кирклином и легли в основу классификации, названной системой TNM: Т (Tumor) — первичная опухоль, N (Node) — вовлеченность регионарных лимфатических узлов, М (Metastasis) — метастазирование во внутренние органы.
American Joint Committee on Cancer (AJCC) была разработана система стадирования злокачественных опухолей. Необходимо помнить, что независимо от стадии некоторые пациенты с небольшим количеством метастазов хорошо себя чувствуют в течение нескольких лет после удаления пораженных регионарных лимфатических узлов. Это еще раз подчеркивает клиническую и молекулярную гетерогенность карциномы толстой кишки. Метастазы могут быть в регионарных лимфоузлах, легких и костях, но самым частым местом локализации метастазов является печень из-за оттока крови от толстой кишки в систему воротной вены. Поскольку кровь от прямой кишки не оттекает в систему воротной вены, метастазирование рака анальной области в печень наблюдается редко.
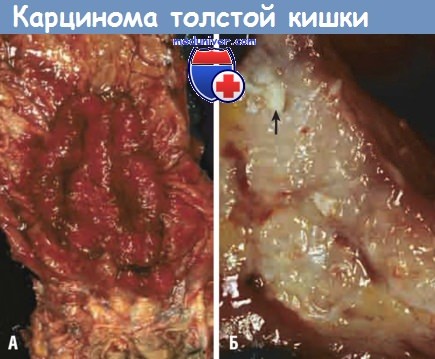
(А) Кольцевидная злокачественная опухоль прямой кишки с изъязвлением.
Внизу снимка видна слизистая оболочка анального канала.
(Б) Злокачественная опухоль сигмовидной кишки, прорастающая сквозь мышечный слой стенки и врастающая в субсерозную жировую клетчатку (слева).
В стенке толстой кишки определяются участки мелового некроза (стрелка).
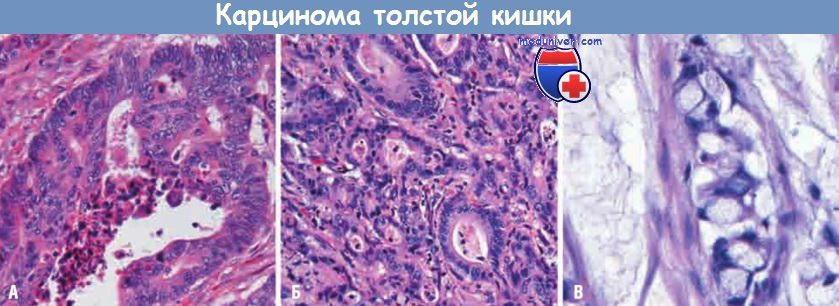
(А) Высокодифференцированная аденокарцинома. Определяются вытянутые гиперхромные ядра.
В просвете железы присутствует характерный некротический тканевый детрит.
(Б) Низкодифференцированная аденокарцинома формирует несколько желез,
но большая часть опухоли состоит из инфильтрирующих гнездных скоплений опухолевых клеток.
(В) Муцинозная аденокарцинома из перстневидных клеток и «озер» внеклеточной слизи.
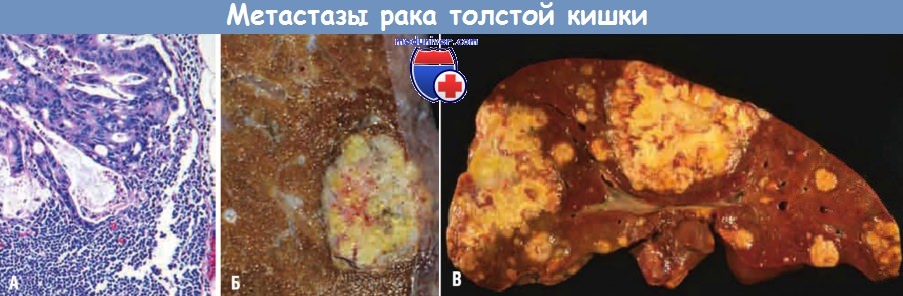
(А) Метастаз в лимфатическом узле. В подкапсульном синусе определяются псевдожелезистые структуры.
(Б) Одиночный субплевральный метастаз в легком.
(В) Печень с двумя крупными и множеством мелких метастазов, в которых отмечаются зоны центрального некроза.
- Рекомендуем ознакомиться со следующей статьей "Механизм развития (патогенез) опухоли анального канала"
Оглавление темы "Патогенез опухолей кишечника":- Механизм развития (патогенез) ювенильных полипов
- Механизм развития (патогенез) синдрома Пейтца-Егерса
- Механизм развития (патогенез) синдрома Каудена и Баннаян-Рувалкаба-Рилей
- Механизм развития (патогенез) синдрома Кронкайта-Канада
- Механизм развития (патогенез) гиперпластического полипа
- Механизм развития (патогенез) аденомы толстой кишки
- Механизм развития (патогенез) наследственного аденоматозного полипоза
- Механизм развития (патогенез) наследственного неполипозного рака толстой кишки
- Механизм развития (патогенез) аденокарциномы толстой кишки
- Механизм развития (патогенез) опухоли анального канала

