Патогенез и морфология респираторного дистресс-синдром (РДС) новорожденных
Существует множество причин расстройства дыхания у новорожденных, например избыточная седация беременной, родовая травма головы, аспирация крови или амниотической жидкости и внутриутробная гипоксия, вызванная обвитием пуповиной. Однако наиболее распространенной причиной считают респираторный дистресс-синдром (РДС), также известный как болезнь гиалиновых мембран из-за отложения гиалиноподобных веществ в периферических воздухоносных путях новорожденных, страдающих этим заболеванием. Ежегодно в США РДС регистрируют у 24 тыс. новорожденных, при этом активная профилактика и лечение данного заболевания за 10 лет привели к резкому снижению количества летальных исходов в результате дыхательной недостаточности с 5000 в год до 900.
У новорожденных, не получающих лечения сурфактантом, развивается типичная клиническая картина. Такой ребенок почти всегда недоношен и соответствует своему гестационному возрасту, отмечается выраженная, но непостоянная ассоциация с мужским полом, сахарным диабетом у беременной и необходимостью кесарева сечения до начала родовых схваток. После рождения ребенку может быть необходима стимуляция, но обычно в течение нескольких минут восстанавливается ритмичное дыхание и кожа ребенка приобретает нормальный цвет.
Однако достаточно быстро, часто в течение 30 мин, дыхание становится затрудненным и в пределах нескольких часов проявляется цианоз, выслушиваются незначительные хрипы сурфактанта для нормального функционирования легких подтверждается тем, что при врожденном его дефиците, возникающем в результате мутаций в генах SFTPB или SFTBC, у новорожденных развиваются тяжелейшие дыхательные нарушения.
Синтез сурфактанта, который осуществляют альвеоциты типа 2, возрастает после 33-й недели гестации. При рождении первый вдох приводит к повышению давления в легких. При нормальном уровне сурфактанта легкие сохраняют « 40% остаточного объема, поэтому для дальнейшего дыхания нужно меньшее давление воздуха.
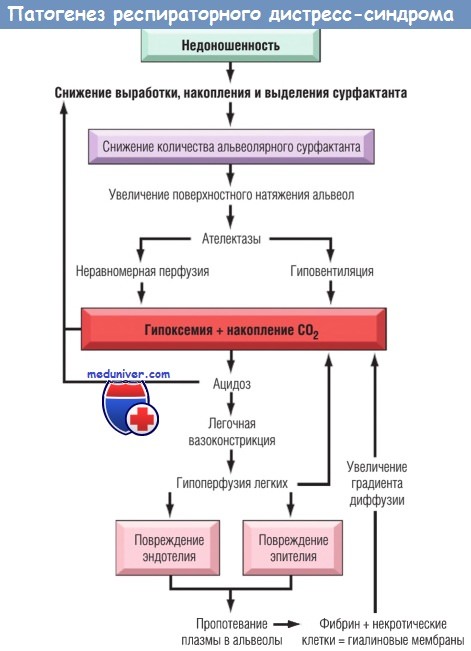
При дефиците сурфактанта легкие на выдохе спадаются и организм ребенка должен каждый раз проделывать такую же работу для их раскрытия, как и при первом вдохе. Ателектатические легкие приводят к втяжению мягких тканей грудной клетки новорожденного и поднятию диафрагмы. Прогрессирующий ателектаз и коллапс легкого запускают цепь событий, в результате которых экссудат, богатый фибрином и белками, заполняет альвеолярные пространства и формируются гиалиновые мембраны. Они создают препятствие для газообмена и приводят к увеличению концентрации в крови углекислого газа и гипоксемии. Гипоксемия, в свою очередь, обусловливает снижение синтеза сурфактанта, в результате возникает порочный круг.
Синтез сурфактанта регулируется различными гормонами и факторами роста, включающими кортизол, инсулин, пролактин, тироксин, TGF-b. При этом роль глюкокортикостероидов особенно важна. Состояния, ассоциированные с внутриутробным стрессом и ВЗРП, при которых увеличивается выброс глюкокортикостероидов, снижают риск развития РДС.
Синтез сурфактанта может подавляться компенсаторно высоким уровнем инсулина в крови плода, если беременная женщина страдает сахарным диабетом (эффекты инсулина противоположны действию стероидов). Этим можно объяснить, в частности, тот факт, что дети матерей, страдающих сахарным диабетом, имеют повышенный риск развития РДС. Известно, что в ходе естественных родов происходит усиление синтеза сурфактанта в легких плода, а кесарево сечение, выполненное до начала родовой деятельности, может повысить риск развития РДС.
Морфология. При макроскопическом исследовании легкие имеют нормальный размер, но плотные, безвоздушные, красно-фиолетового цвета, обычно пропитаны жидкостью и внешне напоминают ткань печени. При микроскопическом исследовании видно, что ткань легкого содержит плохо развитые, по большей части спавшиеся альвеолы. Если ребенок погибает в первые несколько часов после рождения, в терминальных бронхиолах и альвеолярных ходах обнаруживаются только остатки некротических клеток.
Некротический материал организуется в эозинофильные гиалиновые мембраны, которые выстилают альвеолы, забивают респираторные бронхиолы и альвеолярные ходы. Формирующиеся гиалиновые мембраны в основном состоят из фибрина, смешанного с клеточным детритом, который образуется при распаде некротических альвеоци-тов типа 2. Последовательность событий, приводящая к формированию гиалиновых мембран, описана на рисунке ниже. Обращает на себя внимание низкая выраженность нейтрофильной реакции на гиалиновые мембраны. Следует подчеркнуть, что гиалиновые мембраны никогда не наблюдаются у мертворожденных детей.
Если ребенок проживает более 48 час, в легких отмечаются репаративные изменения. Альвеолярный эпителий пролиферирует под поверхностью мембраны, при этом она может быть вытеснена в воздушное пространство, где может произойти ее частичное расщепление или фагоцитоз альвеолярными макрофагами.
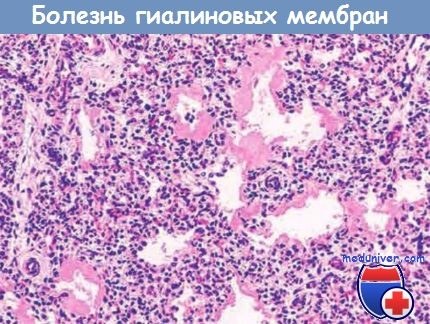
Обратите внимание на толстые эозинофильные гиалиновые мембраны, выстилающие эти альвеолы.
- Рекомендуем ознакомиться со следующей статьей "Клиника респираторного дистресс-синдром (РДС) новорожденных"
Оглавление темы "Патофизиология новорожденных":- Причины смерти детей в зависимости от возраста
- Варианты врожденных аномалий детей
- Генетические причины аномалий развития
- Экологические причины аномалий развития плода
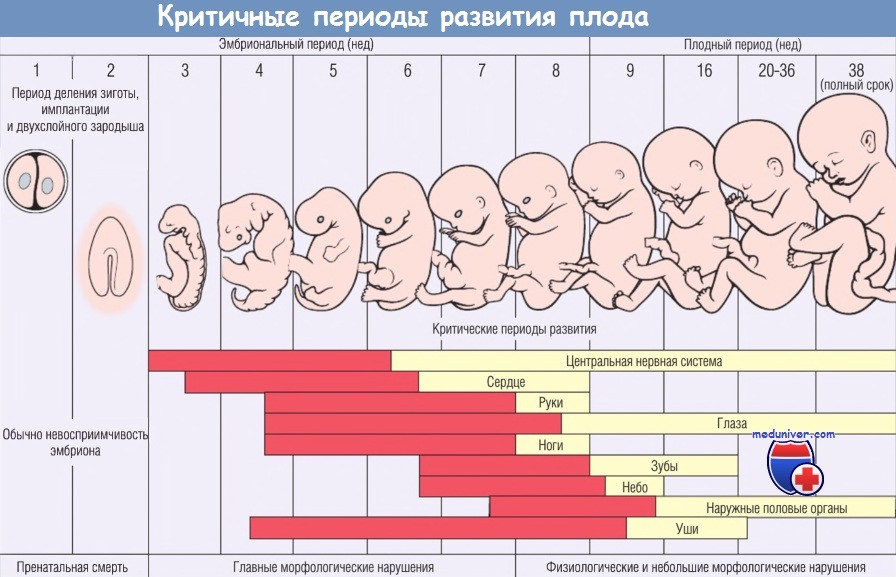
- Патогенез врожденных аномалий развития плода - критичные периоды
- Причины недоношенности и преждевременных родов
- Причины внутриутробной задержки роста плода (ВЗРП)
- Патогенез и морфология респираторного дистресс-синдром (РДС) новорожденных
- Клиника респираторного дистресс-синдром (РДС) новорожденных
- Патогенез бронхолегочной дисплазии (БЛД)

