Кожные признаки прогрессирования ВИЧ инфекции
Дерматологические симптомы в ходе BИЧ-заболевания развиваются более чем у 90% ВИЧ-инфицированных. По мере ухудшения иммунной функции частота этих симптомов возрастает. К специфическим кожным заболеваниям, коррелирующим с низким количеством Т-клеток CD4+ (<300/мкл) относятся дерматозы (такие как эозинофильный фолликулит и папулезная пруритическая сыпь ВИЧ-инфекции), оппортунистические злокачественные заболевания (такие как саркома Капоши) и оппортунистические инфекции (такие как микобактериальные инфекции, кандидоз ротоглотки, контагиозный моллюск и глубокие грибковые инфекции).
а) Воспалительные дерматозы:
1. Зуд и зудящие высыпания при ВИЧ-заболевании. Зуд является распространенной жалобой пациентов с поздним симптоматическим и прогрессирующим ВИЧ-заболеванием.
В большинстве случаев причиной зуда являются первичные или вторичные дерматозы, а не метаболические нарушения. Дифференциальный диагноз зуда у ВИЧ-инфицированных лиц представлен в блоке ниже.
Диатез по типу атопии и зуд могут проявиться у лиц с прогрессирующим ВИЧ-заболеванием даже в отсутствие атопии в анамнезе. Часто наблюдаются вторичные изменения вследствие растираний и расчесов, в том числе экскориации, простой хронический лишай и узловатое пруриго. В травматизированных очагах возможна вторичная инфекция S. aureus (импетигинизация, фурункулез или целлюлит). Вульгарный ихтиоз и ксероз часто отмечаются на поздних стадиях ВИЧ-заболевания и могут сопровождаться слабым зудом. Ингибиторы протеазы (особенно индинавир) могут вызвать ретиноидный дерматит. Эти изменения обычно развиваются относительно быстро после начала лечения.
Идиопатический зуд сочетается с количеством Т-клеток CD4+ < 200/mkm и вирусной нагрузкой >55,000 копий/мл, в то время как APT ассоциируется с ослаблением идиопатического зуда.

2. Эозинофильный фолликулит. Эозинофильный фолликулит — хронический пруритический дерматоз, который развивается у пациентов на поздней стадии ВИЧ-заболевания. В ретроспективном исследовании ВИЧ-инфицированных пациентов низкое количество Т-клеток CD4+ (<200/мкл) ассоциировалось с развитием эозинофильного фолликулита независимо от статуса APT. Клинически эозинофильный фолликулит проявляется интенсивно зудящими, маленькими, розово-красными, отечными, фолликулоцентричными папулами, реже пустулами. Очаги обычно развиваются симметрично над линией сосков на груди, на проксимальных участках верхних конечностей, на голове и шее.
Нередко наблюдаются вторичные изменения, в том числе экскориации, простой хронический лишай и узловатое пруриго, а также вторичная инфекция S. aureus. У пациентов с темной кожей поствоспалительная гиперпигментация часто приводит к значительному косметическому дефекту. Гистологические признаки эозинофильного фолликулита довольно специфические и включают воспалительный инфильтрат из лимфоцитов и эозинофилов на уровне фолликулярного перешейка и сальных желез. Периферическая эозинофилия наблюдается примерно у 25-50% пациентов.
Наиболее эффективной терапией эозинофильного фолликулита является преднизон (стартовая доза 70 мг ежедневно с постепенным снижением по 5 или 10 мг в течение 7 или 14 дней). Однако у большинства пациентов после успешного лечения эозинофильного фолликулита очаги рецидивируют в течение нескольких недель после прекращения приема преднизона. Пациентам с тяжелыми симптомами преднизон можно назначать через день или еженедельно. Сообщалось об эффективности итраконазола в дозе 200 мг ежедневно. Если через две недели ответ на терапию отсутствует или лишь частичный, дозу повышают до 300 или 400 мг ежедневно. Третья альтернатива — прием внутрь изотретиноина в дозе 40-80 мг ежедневно.
Когда очаги и симптомы разрешатся, дозу можно понизить до 40 мг ежедневно и продолжать прием в течение нескольких недель, а затем до 20 мг ежедневно или до 40 мг через день. Изотретиноин может повышать сывороточные уровни триглицеридов, которые у ВИЧ-инфицированных и без того часто высокие. Следовательно, уровень сывороточных липидов необходимо регулярно контролировать. Фототерапия узкополосным ультрафиолетом В (УФВ) и ультрафиолетом А с псораленом или без псоралена считается безопасной и эффективной терапевтической возможностью для ВИЧ-инфицированных пациентов и не увеличивает вирусную нагрузку. Местные кортикостероиды высокой фармакологической активности могут уменьшить образование новых очагов, а также действуют на экзематозный дерматит, обеспечивая облегчение симптомов.
Местные препараты, содержащие 4% гидрохинона, сравнительно неэффективны для лечения поствоспалительной гиперпигментации.
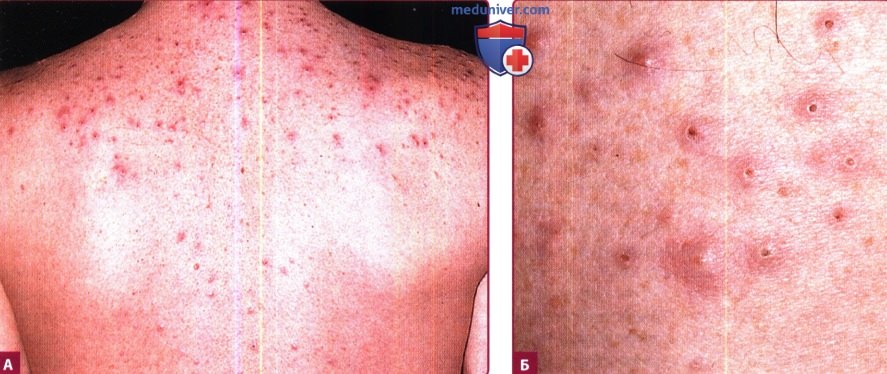
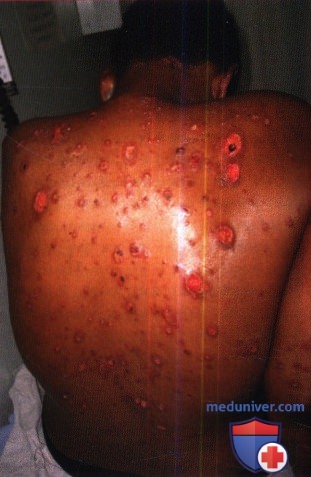
А. Множественные эритематозные пруритические папулы на туловище у пациента с количеством CD4-клеток 50/мкл.
Б. Папулы крапивницы, пустулы и эрозии, вторичные вследствие расчесов и корок.
3. Папулезно-пруритическая сыпь при ВИЧ. Папулезно-пруритическая сыпь (ППС) при ВИЧ-инфекции считается частью спектра пруритических папулезных высыпаний при ВИЧ-заболевании, который включает эозинофильный фолликулит и неспецифический зуд. Первичным очагом является твердая уртикарная папула, хотя описаны также стерильные пустулы. Высыпания обычно симметричные и расположены в основном на конечностях, реже на туловище и лице. Иногда, но не всегда, очаги фолликулоцентричные. Поскольку высыпания интенсивно зудящие, они типично ассоциируются с многочисленными экскориациями, выраженной поствоспалительной гиперпигментацией и рубцеванием.
О ППС редко сообщается в Европе и Северной Америке, однако распространенность ППС достигает 18-46% в Африке и на Гавайях, где она часто является первоначальным признаком ВИЧ-заболевания. Фактически, ППС является маркером тяжелой иммуносупресии, поскольку более чем у 80% ВИЧ-инфицированных с ППС количество Т-клеток CD4+ составляет < 100/мкл. Этиопатогенез ППС неизвестен, но предполагается, что ППС может представлять собой реакцию гиперчувствительности на укусы насекомых. ППС очень сложно эффективно лечить, поскольку сыпь лишь умеренно реагирует на антигистаминные препараты и местные стероиды. Эффективным лечением ППС является иммунная реконституция посредством APT, хотя для разрешения очагов может потребоваться несколько месяцев терапии. Эффективна также УФВ-терапия, хотя ее применение ограничено странами с ограниченными ресурсами, где отсутствуют специализированные центры и где распространенность ППС наиболее высока.
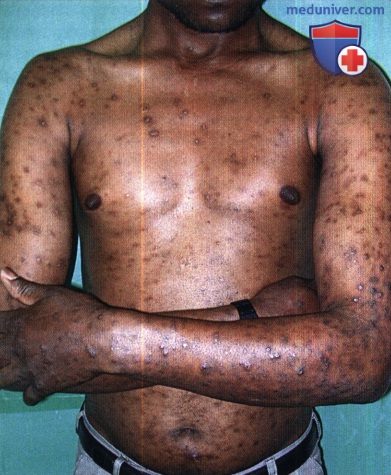
Присутствуют множественные, диссеминированные экскориативные папулы, поствоспалительная гиперпигментация и небольшие рубцы. Сыпь сопровождается значительным зудом.
4. Фоточувствительность. О фоточувствительности у ВИЧ-инфицированных сообщалось в связи с другими заболеваниями, такими как поздняя кожная порфирия, хронический актинический дерматит, лихеноидный фотодерматит и фоточувствительная гранулема. Идиопатическая фоточувствительность — необычное явление при ВИЧ-инфекции, но может быть первоначальной жалобой при прогрессировании ВИЧ-заболевания. Клинически, фоточувствительные высыпания имеют две характерных морфологических картины: (1) лихеноидные высыпания на открытых воздействию света участках и (2) экзематозные высыпания на открытых воздействию света участках. К факторам риска развития фоточувствительности относятся принадлежность к афроамериканской этнической группе (риск, кратный 6,7) и APT (риск, кратный 2,8).
5. Эритродермия. Эритродермия при ВИЧ-за-болевании может быть связана с лекарственной гиперчувствительностью, атопическим дерматитом, псориазом, себорейным дерматитом, дерматитом фоточувствительности, сопутствующей инфекцией человеческого Т-клеточного лимфотропного вируса-1, красным волосяным лишаем или кожной Т-клеточной лоимфомой.
б) Заболевания ротоглотки при ВИЧ-инфекции. Почти у всех не получавших лечения ВИЧ-инфицированных в течении их заболевания развиваются поражения ротоглотки. Примерно в 10% случаев о заболеваниях ротоглотки сообщается как о первом признаке ВИЧ-заболевания. Таким образом, наличие стойкого заболевания ротоглотки может быть показанием к обследованию на ВИЧ-инфекцию. При исследовании заболеваний ротоглотки в случае прогрессирующего ВИЧ-заболевания самым частым оказался кандидоз, который диагностировался у 90% пациентов. Другие распространенные поражения ротоглотки включали герпетические язвы, ксеростомию, эксфолиативный хейлит, волосатую лейкоплакию полости рта, саркому Капоши, очаговое отсутствие сосочков на языке и язвы неизвестной этиологии. У лиц, получающих APT, частота заболеваний в полости рта ниже, чем у нелеченых индивидуумов.
в) Волосатая лейкоплакия полости рта. Волосатая лейкоплакия является доброкачественной инфекцией эпителиальных клеток слизистой полости рта, вызванной вирусом Эпштейна-Барр. Как частое проявление ВИЧ-заболевания в полости рта, волосатая лейкоплакия является маркером умеренной или прогрессирующей иммуносупрессиии. Однако частота волосатой лейкоплакии снизилась с внедрением APT. Клинически, волосатая лейкоплакия проявляется бессимптомными гиперпластическими белесыми бляшками на обеих боковых поверхностях языка. Очаги типично асимметричные и имеют вертикальные бороздки, которые контрастируют с нормальным рифлением поверхности языка. Лечение может не потребоваться, поскольку очаги часто бессимптомные. Однако иногда эффективны ацикловир и валацикловир. Сообщалось о положительном действии подофиллина.
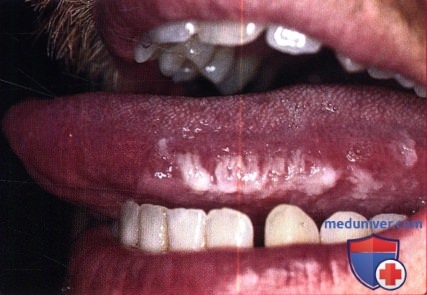
Белые бляшки с вертикальными бороздами на нижнебоковой поверхности языка.
Поражения фиксированы, в отличие от поражений при кандидозе, когда они могут счищаться марлевым шариком.
г) Оппортунистические инфекции при ВИЧ-инфекции:
1. Bartonella. Бациллярный ангиоматоз, вызванный Bartonella henselae и Bartonella quintana, развивается чаще всего на фоне прогрессирующего позднего ВИЧ-заболевания (количество Т-клеток CD4+ < 200/мкл). Клинически, кожные очаги бациллярного ангиоматоза представляют собой красно-фиолетовые, куполообразные папулы, узлы или бляшки, которые могут напоминать вишневую ангиому, пиогенную гранулему или саркому Капоши. Очаги, иногда болезненные при пальпации, достигают размеров от нескольких миллиметров до 2-3 см в диаметре. Реже могут развиться куполообразные подкожные образования без характерного для более поверхностных сосудистых очагов красного цвета. Очаги могут быть одиночными или множественными, в редких случаях их количество может составлять более 1000. Поражаться может любой участок кожной поверхности, однако ладони, подошвы и полость рта обычно остаются незатронутыми.
К спектру системных заболеваний, вызванных В. henselae и В. quintana после гематогенной или лимфогенной диссеминации возбудителя, относятся образования в мягких тканях, поражение костного мозга, лимфаденопатия, спленомегалия и гепатомегалия. У ряда ВИЧ-инфицированных пациентов сообщалось об инфекции печени в форме ассоциированного с Bartonella пелиоза печени.
В настоящее время распространенность бациллярного ангиоматоза в Северной Америке и Европе низкая вследствие широкой доступности APT и профилактики инфекций, в частности комплекса Mycobacteria avium. Антибиотиками выбора при бациллярном ангиоматозе являются эритромицин (250-500 мг внутрь четыре раза в день) или доксициклин (100 мг два раза в день) в течение минимум четырех недель или до разрешения очагов. Вторичная профилактика показана пациентам с рецидивирующим бациллярным ангиоматозом.
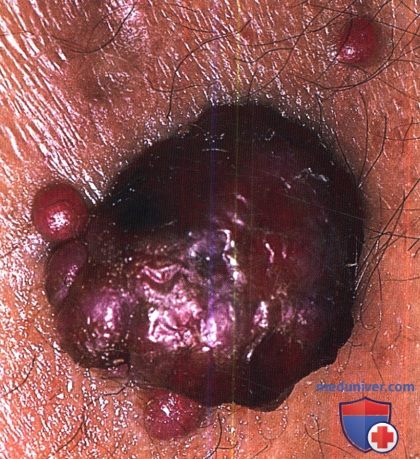
Папулы, напоминающие вишневую гемангиому, и узелки, напоминающие крупную пиогенную гранулему на поздней стадии ВИЧ-инфекции.
Также отмечаются подкожные узловые образования.
2. Кожный туберкулез. Хотя туберкулезные инфекции относятся к распространенным оппортунистическим инфекциям при ВИЧ-заболевании, особенно в развивающихся странах, кожный туберкулез встречается редко. Возбудителями туберкулеза кожи являются Mycobacterium tuberculosis, Mycobacterium bovis и вакцина БЦЖ. У ВИЧ-инфицированных описаны различные проявления кожного туберкулеза, в том числе скрофулодерома, лихеноидный туберкулез (лишай золотушных), диссеминированный милиарный туберкулез, гумматозный туберкулез и туберкулезный абсцесс. О кожном милиарном туберкулезе — в прошлом редкой форме кожного туберкулеза вследствие гематогенного распространения бацилл в кожу из внутреннего очага инфекции — сообщалось у многих больных с прогрессирующей поздней стадией ВИЧ-заболевания (количество Т-клеток CD4+ < 100/мкл). Клинически, кожный милиарный туберкулез может вначале проявляться красно-коричневыми точечными пятнышками, папулами и папуловезикулами.
Очаги часто развиваются в маленькие папулы с плоской поверхностью и коркой в центре. Высыпания обычно распределяются симметрично, с предпочтительной локализацией на ягодицах, бедрах и разгибательных поверхностях. Кожные признаки милиарного туберкулеза кожи неспецифические и могут напоминать бактериальный фолликулит. Иногда присутствуют легочные симптомы, однако результаты радиографического исследования также могут быть неспецифическими. В случае кожного милиарного туберкулеза проводится мультилекарственная противотуберкулезная терапия; однако уровень смертности высокий (> 50%), особенно в случае организмов с мультилекарственной резистентностью.
3. Кандидоз. Колонизация ротоглотки организмом Candida часто встречается у ВИЧ-инфицированных, о ней сообщается у 90% пациентов с поздней прогрессирующей стадией заболевания. Кандидоз ротоглотки типично проявляется в четырех различных клинических формах: (1) псевдомембранозной (молочница), (2) гиперпластической, (3) эритематозной (атрофической) и в форме (4) ангулярного хейлита. Псевдомембранозный кандидоз обычно поражает язык и проявляется желто-белыми бляшками, которые удаляются при соскабливании. Гиперпластический кандидоз обычно развивается на слизистой щек и состоит из белых бляшек, которые соскабливанием не удаляются. Эритематозный кандидоз обычно проявляется эритематозными пятнами на твердом небе и аналогичными очагами на дорсальной поверхности языка, в которых при этом отсутствуют сосочки. Ангулярный хейлит представляет собой эритему с творожистыми пятнами или болезненными трещинами в уголках губ.
Ряд исследований показал повышенную частоту вульвовагинального кандидоза у ВИЧ-инфицированных женщин, особенно у пациенток на поздней стадии заболевания. В одном проспективном исследовании, например, было показано, что у женщин с количеством Т-клеток CD4+ <200/мкл риск симптоматического вульвовагинального кандидоза возрастает в четыре раза по сравнению с иммунокомпетентными женщинами. В исследовании двухсот ВИЧ-инфицированных женщин в Северной Америке рецидивирующий вагинальный кандидоз был самым распространенным начальным клиническим проявлением ВИЧ-инфекции у 37% пациенток. У детей с ВИЧ-инфекцией часто наблюдается кандидоз полости рта, пеленочный кандидоз и интертриго в паховых и шейных складках.
4. Дерматофитные инфекции. У ВИЧ-инфицированных лиц, как и у иммунокомпетентных индивидуумов, чаще всего наблюдаются такие дерматофиты, как Trichophyton rubrum и Trichophyton mentagrophytes. При ВИЧ-заболевании дерматофитные инфекции эпидермиса, обычно вызываемые Т. rubrum, могут быть более распространенными и часто бессимптомными. Диссеминированное заболевание может иногда проявляться атипично. Сообщалось, например, что диссеминированная инфекция Т. rubrum имитировала саркому Капоши. Инфекции ногтей также встречаются часто. Т. rubrum нередко вызывает дистальный и латеральный подногтевой онихомикоз как у ВИЧ-инфицированных, так и у иммунокомпетентных лиц. Однако Т. rubrum вызывает также проксимальный подногтевой онихомикоз (инфекцию внутренней поверхности проксимальной ногтевой пластинки), который наблюдается исключительно у ВИЧ-инфицированных лиц. Следовательно, диагноз проксимального подногтевого онихомикоза является показанием к обследованию на ВИЧ-инфекцию. До восстановления иммунокомпетент-ного состояния дерматофитные инфекции часто хронические и рецидивируют. Внедрение APT значительно уменьшило частоту этих инфекций, и побочные лекарственные взаимодействия между APT и противогрибковыми медикаментами представляются клинически менее значимыми, чем считалось ранее.
5. Инвазивные грибковые инфекции. Диссеминированные грибковые инфекции на поздней стадии ВИЧ-заболевания могут возникать либо (1) путем локальной инвазии в кожу или слизистые при вторичной лимфатической или гематогенной диссеминации, либо (2) при реактивации латентного легочного очага инфекции. Кожные проявления часто напоминают множественные очаги контагиозного моллюска с предпочтительной локализацией на лице и верхней части туловища.
6. Криптококкоз. Диссеминированная инфекция инкапсулированного дрожжевого организма Cryptococcus neoformans, вероятно, самая распространенная из угрожающих жизни грибковых инфекций, ассоциирующихся с поздней стадией ВИЧ-заболевания. Диссеминированное заболевание типично поражает головной мозг, почки, предстательную железу, кости и перикард. Диссеминированный криптококкоз чаще наблюдается у лиц с количеством Т-клеток CD4+ < 50/мкл. Самым распространенным клиническим проявлением кожного криптококкоза являются розовые или телесного цвета папулы или узлы с вдавлением в центре, расположенные на голове и шее и имитирующие высыпания контагиозного моллюска. Реже наблюдаются подкожные узлы, целлюлит, герпетиформные язвы, пальпируемая пурпура, фиолетовые бляшки, имитирующие саркому Капоши и очаги по типу гангренозной пиодермии. Кожные очаги могут развиться за много недель или месяцев до появления системных симптомов.
7. Кокцидиоидомикоз. Диморфный гриб Coccidioides immitis является эндемичным для юго-западных штатов США, Мексики, а также Центральной и Южной Америки. Кожные очаги диссеминированного кокцидиоидомикоза обычно бессимптомные и типично начинаются в форме папул, развивающихся в пустулы, бляшки и узлы с минимальной эритемой вокруг. Очаги часто напоминают высыпания контагиозного моллюска. Со временем очаги могут увеличиваться и сливаться, образуя абсцессы, многочисленные дренирующие свищевые ходы, язвы, целлюлит, веррукозные бляшки и гранулематозные узлы. В отличие от гистоплазмоза и криптококкоза, слизистые оболочки полости рта обычно не поражаются.
8. Гистоплазмоз. Histoplasma capsulation является диморфным почвенным грибом. К эндемическим районам относятся речные долины на Среднем и Южном Западе США, юго-восточная часть Южной Америки и Южная и Восточная Африка. Диссеминированный гистоплазмоз чаще всего наблюдается у лиц на поздней стадии ВИЧ-заболевания (количество Т-клеток CD4+ < 50/ мкл) и проявляется лихорадкой, потерей веса, легочными симптомами, лимфаденопатией, гепатоспленомегалией и кожными высыпаниями. Кожные признаки, ассоциированные с диссеминированным гистоплазмозом, могут включать очаги различной морфологии, в том числе эритематозные папулы, некротические папулы и узлы с вдавлением в центре, имитирующие контагиозный моллюск, фолликулит, акнеформные, розацеа-подобные и псориазиформные высыпания, язвы, вегетирующие бляшки и очаги по типу гангренозной пиодермии. Чаще всего очаги развиваются на лице, затем на конечностях и туловище. Также могут поражаться слизистые оболочки полости рта, иногда наблюдаются узлы и изъязвления на мягком небе, в ротоглотке, надгортаннике и преддверии носа. У ВИЧ-инфицированных пациентов, уже получающих противогрибковую терапию, могут развиться распространенные, слабо выраженные, экзантематозные или псориазоформные высыпания.
9. Аспергиллез. Инвазивный аспергиллез при ВИЧ-заболевании встречается редко и является осложнением, наблюдаемым главным образом у лиц с количеством Т-клеток CD4+ < 50/мкл. Первичный кожный аспергиллез типично развивается в случае прямой инокуляции и иногда наблюдается на месте внутривенных катетеров. Вторичный кожный аспергиллез обычно является результатом гематогенной диссеминации или прямого распространения инфекции на кожу из очага в легких. К факторам риска инвазивного аспергиллеза при ВИЧ-заболевании относятся нейтропения, применение кортикостероидов и внутривенное введение наркотиков. Кожные очаги обычно представляют собой папулы и узлы телесного или розового цвета, напоминающие контагиозный моллюск, а также флуктуирующие папулы, глубоко расположенные пустулы, везикулезно-пустулезные бляшки и незаживающие язвы. Смертность при инвазивном аспергиллезе остается высокой даже при соответствующей терапии. Сообщалось о том, что терапия вориконазолом ассоциируется с повышением выживаемости и меньшими побочными эффектами по сравнению с амфотерицином В.
10. Пенициллиоз. Диморфный гриб Penicillium marneffei является возбудителем третьей по частоте ассоциированной с ВИЧ оппортунистической инфекции в Юго-Восточной Азии и является эндемичным организмом в северо-восточной части Индии, во Вьетнаме, Таиланде, Индонезии и Южном Китае. Клинические проявления пенициллиоза вариабельные, хотя у пациентов с количеством Т-клеток CD4+ < 50/мкл он часто проявляется лихорадкой, потерей веса, анемией и лимфаденопатией. Кожные очаги присутствуют у 70% пациентов и обычно состоят из папул с вдавлением в центре, которые преимущественно локализуются на лице, ушных раковинах, верхней части туловища и руках. Сообщалось также о пустулах, подкожных узлах и акне-подобных высыпаниях. Терапия амфотерицином или итраконазолом эффективна, хотя рецидивы случаются часто. Вторичная профилактика показана пациентам до иммунной реконституции методом APT.
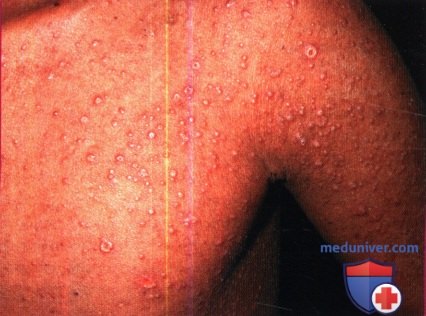
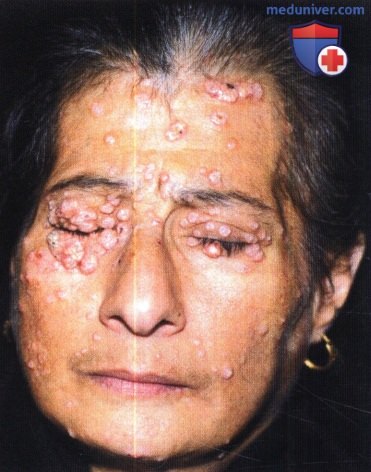
11. Контагиозный моллюск. Очаги контагиозного моллюска вызваны инфекцией поксвируса и являются кожным маркером поздней стадии ВИЧ-заболевания (количество Т-клеток CD4+ < 100/мкл). Часто наблюдаемые у детей, инфекции контагиозного моллюска у ВИЧ-инфицированных пациентов могут проявляться папулами с вдавлением в центре перламутрово-телесного цвета, которые характерны для иммунокомпетентных лиц. Однако для поздней стадии ВИЧ-заболевания типичны крупные, сливающиеся очаги, которые локализуются преимущественно на лице. Часто встречаются атипчиные очаги, которые могут напоминать фолликулит, абсцессы, фурункулы, бородавки и кожный рог. Дифференциальный диагноз очагов у ВИЧ-инфицированного пациента, напоминающих контагиозный моллюск, приведен в блоке ниже. В исследовании, проводившемся до внедрения AFT, очаги контагиозного моллюска выявлялись у 30% пациентов с количеством Т-клеток CD4+ < 100/мкл. После инициации APT очаги контагиозного моллюска часто полностью разрешаются.
У ВИЧ-инфицированных лиц инфекция контагиозного моллюска обычно прогрессирует и рецидивирует. Электрофульгурация с многократным кюретажем эффективна в случае множественных, крупных и сливающихся очагов. В случаях, устойчивых к стандартной терапии, эффективным как у детей, так и у взрослых может быть крем имиквимода 5%. Сообщалось также об эффективности местного цидофовира, нуклеотидного аналога с активностью против ДНК нескольких вирусов.
12. Т-клеточный лимфотропный вирус человека. Человеческий Т-клеточный лимфотропный вирус-1 (HTLV-1) представляет собой ретровирус человека, который ассоциируется с Т-клеточным лейкозом взрослых, медленно прогрессирующим неврологическим заболеванием (ассоциированная с HTLV-1 миелопатия/тропический спастический парапарез), увеитом и хроническим экзематозным дерматитом, так называемым «инфекционным дерматитом». Кожные признаки инфекции HTLV-1 имитируют хронический атопический дерматит и типично проявляются у детей и подростков эритематозными, шелушащимися и покрытыми коркой бляшками на волосистой части кожи головы, в области шеи и паха. Вблизи бровей могут наблюдаться периорбитальные папулы с себорейным шелушением. В небольшом количестве случаев наблюдаются заушные трещины и генерализованный ихтиоз. Экссудативная природа этих очагов может помочь дифференцировать HTLV-1 и атопический дерматит.
Высокий процент серопревалентности к HTLV-1 обнаружен в Японии, странах Карибского бассейна, Африке и Южной Америке (в частности, в Бразилии). Точный процент коинфекции HTLV-1 и ВИЧ неизвестен, хотя в одном исследовании ВИЧ-инфицированных в Бразилии процент сопутствующей инфекции HTLV-1 составил 12,5%. При сопутствующей инфекции HTLV-1 у ВИЧ-инфицированных взрослых отмечается повышенная частота воспалительных дерматозов, в том числе себорейного дерматита и пруриго. Кроме того, коинфекция ВИЧ и HTLV-1 протекала на фоне более высоких показателей количества Т-клеток CD4+, но в более тяжелой клинической форме, чем в случае одной ВИЧ-инфекции, следовательно, повышение уровня Т-клеток, CD4+ не приносит иммунологической пользы на фоне коинфекции HTLV-1.
13. Чесотка. Чесотка, паразитарная инфекция вызванная клещом Sarcoptes scabiei hominis, включена в дифференциальный диагноз зуда при ВИЧ-заболевании. У ВИЧ-инфицированных лиц чесотка может протекать с типичными симптомами, но на поздних стадиях заболевания, когда пациенты неспособны контролировать репликацию клещей, существует риск развития крустозной формы чесотки. Крустозная чесотка обычно проявляется обширными, толстыми, кератотическими бляшками с бурыми чешуйками в атипичной локализации, в частности, на волосистой части кожи головы, в области роста бороды, на ладонях и подошвах. Зуд в очагах часто отсутствует или минимальный. Если у иммунокомпетентного пациента насчитывается 10-15 клещей, то один грамм корки у пациента с крустозной чесоткой может содержать тысячи паразитов. По этой причине крустозная чесотка является острозаразной. Возможна суперинфекция S. aureus, но она редко осложняется бактериемией. В случае классической чесотки обычно эффективен местный скабицидный препарат или системный ивермектин (200 мкг/кг в неделю) х 2 дозы. В случае крустозной чесотки могут потребоваться несколько доз ивермектина (200 мг/кг в неделю), а именно 3-7 доз (в зависимости от тяжести инфекции), которые необходимо комбинировать с применением местного скабицида (каждые 2-3 дня в течение 1-2 недель) и кератолитического крема для улучшения пенетрации действующего вещества.
14. Лейшмании. Процент коинфекции ВИЧ и лейшманий варьирует; однако в исследованиях сообщалось, что этот показатель составляет от 2% до 30% в эндемических регионах. Сообщалось, что ВИЧ-инфекция повышает риск развития висцерального лейшманиоза в эндемических регионах в 100-2320 раз, как и риск рецидивирующего заболевания. Лейшманиоз, в свою очередь, усиливает инфекционность ВИЧ и способствует прогрессированию ВИЧ-заболевания, вероятно стимулируя репликацию ВИЧ-1. У ВИЧ-инфицированных пациентов с лейшманиозом ниже процент излечения, выше процент рецидивов и смертности, чем у иммунокомпетентных лиц. См. дискуссию о лечении лейшманиоза в отдельной статье на сайте.

в) Оппортунистические неоплазии при ВИЧ-инфекции. У лиц с ВИЧ-заболеванием сообщалось о более высокой распространенности определяющих наличие СПИДа злокачественных заболеваний, саркомы Капоши, ПКР шейки матки in situ и инвазивного, а также неходжскинской лимфомы. Кроме того, у ВИЧ-инфицированных лиц отмечалась также повышенная заболеваемость ПКР ануса, in situ и инвазивным, ПКР вульвы и влагалища, ходжкинской лимфомой, первичным раком печени, раком легких, меланомой, немеланомными видами рака кожи, раком ротоглотки и лейкозом.
С внедрением APT частота некоторых оппортунистических неоплазий, таких как саркома Капоши и неходжкинская лимфома резко снизилась. Однако заболеваемость многими видами злокачественных новообразований, определяющими наличие СПИДа (такими как анальный ПКР, немеланомные виды новообразований кожи, меланома и ходжкинская лимфома) не уменьшилась, несмотря на внедрение APT, и имеются данные о том, что в некоторых случаях их частота фактически возросла. Этиология более высокой частоты злокачественных опухолей у ВИЧ-инфицированных лиц, вероятно, многофакторная. Способствующие факторы могут включать уменьшение иммунологического контроля опухоли, сопутствующую инфекцию онкогенными вирусами (такими как вирус Эпштейна-Барр, ВПЧ и герпесвирус человека типа 8), а также факторы, связанные с поведением и образом жизни пациентов.
г) Список использованной литературы:
1. Hall HI et al: Estimation of HIV incidence in the United States. JAMA 300(5):520-529, 2008
2. Lapins J et al: Mucocutaneous manifestations in 22 consecutive cases of primary HIV-1 infection. Br J Dermatol 134(2):257-261, 1996
3. French MA et al: Immune restoration disease after the treatment of immunodeficient HIV-infected patients with highly active antiretroviral therapy. HIV Med 1(2):107—115, 2000
4. Patel P et al: Incidence of types of cancer among HIVinfected persons compared with the general population in the United States, 1992-2003. Ann Intern Med 148( 10):728-736, 2008
5. Coopman SAet al: Cutaneous disease and drug reactions in HIV infection. N Engl J Med 328(23): 1670-1674, 1993
6. Saiag P et al: Drug-induced toxic epidermal necrolysis (Lyell syndrome) in patients infected with the human immunodeficiency virus. I Am Acad Dermatol 26(4):567-574,1992
7. Zancanaro PC et al: Cutaneous manifestations of HIV in the era of highly active antiretroviral therapy: An institutional urban clinic experience. J Am Acad Dermatol 54(4):581-588, 2006
8. Rosenthal D et al: Human immunodeficiency virusassociated eosinophilic folliculitis. A unique dermatosis associated with advanced human immunodeficiency virus infection. Arch Dermatol 127(2):206-209, 1991
9. Venkatesan P, Perfect JR, Myers SA: Evaluation and management of fungal infections in immunocompromised patients. Dermatol Ther 18(l):44-57, 2005
- Рекомендуем далее ознакомиться со статьей "Классификация риккетсиозов, эрлихиозов, анаплазмозов"
Редактор: Искандер Милевски. Дата публикации: 19.5.2019

