Причины и механизмы развития герпетиформного дерматита (ГД)
- Хронические папуло-везикулезные высыпания с симметричным распределением на разгибательных поверхностях. Сопровождаются сильным зудом.
- В сосочках дермы определяются скопления нейтрофилов (микроабсцессы).
- Диагностическим признаком заболевания являются отложения гранулярного иммуноглобулина А во внешне неизмененной коже.
- В большинстве случаев наблюдается ассоциация с глютенсенситивной энтеропатией.
- В терапии герпетиформного дерматита эффективен дапсон; большинству пациентов помогает строгая безглютеновая диета.
а) Эпидемиология. Герпетиформный дерматит (ГД) представляет собой хронические интенсивно зудящие папуло-везикулезные высыпания, которые, как правило, имеют симметричную локализацию на разгибательных поверхностях. Заболевание четко дифференцируется от других высыпаний с образованием субэпидермальных пузырей по гистологическим, иммунологическим и гастроинтестинальным критериям. Распространенность ГД в различных популяциях европеоидной расы составляет от 10 до 39 случаев на 100000 населения. В некоторых сообщениях указывается на соотношение мужчин и женщин при герпетиформном дерматите (ГД) как 1,5:1.
Герпетиформный дерматит (ГД) может развиться в любом возрасте (зарегистрированы случаи детского ГД), однако чаще всего заболевание встречается у лиц в возрасте 20-40 лет. ГД персистирует неопределенно долго с переменной степенью тяжести. Два долгосрочных исследования пациентов с иммунологически подтвержденным диагнозом ГД указывают, что примерно в 10-12% случаев заболевание в итоге регрессирует.
У пациентов с герпетиформным дерматитом (ГД) нередко отмечается ассоциированная глютенчувствительная энтеропатия, которая в большинстве случаев протекает бессимптомно.
б) Этиология и патогенез герпетиформного дерматита (ГД). В 1884 году Луи Дюринг впервые описал клинические признаки и естественное течение полиморфного зудящего заболевания, которое он назвал герпетиформным дерматитом; однако основные звенья патогенеза ГД оставались неизвестными до 1960-х годов. В 1966 году Marks и соавторы впервые обратили внимание на желудочно-кишечные аномалии у пациентов с ГД. Вскоре после этого было показано, что очаги заболевания разрешаются при исключении из диеты белка глютена. Вначале считалось, что кишечная аномалия присутствует у 60-70% пациентов с ГД. Однако это мнение дважды изменялось.
Во-первых, были более точно установлены диагностические критерии для герпетиформного дерматита (ГД), а, во-вторых, было показано, что у некоторых пациентов без очевидной патологии ЖКТ гастроинтестинальное поражение могло развиваться при приеме большого количества глютена и, следовательно, у таких пациентов можно предположить наличие латентной целиакии. Таким образом, у большинства пациентов с ГД имеется аномалия ЖКТ, подобная (если не идентичная) целиакии, которая, однако, бывает минимальной, если человек принимает нормальное количество глютена. Все эти исследования подтвердили, что глютен, белок, который содержится в пшенице, ячмене и ржи, играет ведущую роль в патогенезе ГД. Овес, который долго считали содержащим глютен и участвующим в появлении очагов ГД, согласно исследованиям не оказывает токсического действия на пациентов с ГД. Как и при целиакии, в тонкой кишке пациентов с ГД отмечается повышенная плотность внутриэпителиальных Т-клеток с γ/δ Т-клеточными рецепторами.
В различных клинических проявлениях глютенчувствительной энтеропатии (ГЧЭ) и герпетиформного дерматита участвуют различные профили цитокинов, поскольку Т-клеточные линии пациентов с ГД производят значительно больше интерлей-кина-4 (ИЛ-4), чем аналогичные клетки пациентов с ГЧЭ, а в биопсиях кишечника симптоматических пациентов с истинной ГЧЭ отмечается повышенная экспрессия ин-терферона-γ. В сыворотке и коже пациентов с ГД обнаруживаются системные признаки иммунного ответа со стороны слизистой кишечника. У пациентов с ГД, регулярно принимающих глютен-содержащую пищу, выявляются повышенные уровни рецепторов ИЛ-2 и ИЛ-8 сыворотки, повышенная экспрессия в коже Е-селектина эндотелиальных клеток, а также повышенная экспрессия CD 11b в нейтрофилах крови. Такие системные проявления иммунного ответа со стороны слизистой кишечника, вероятно, участвуют в создании провоспалительной среды в коже, необходимой для развития кожных очагов. ГЧЭ, наблюдаемая у пациентов с ГД, вероятно, связана с отложениями иммуноглобулина А, которые выявляются в коже таких пациентов, однако прямой связи установлено не было. Сообщалось о пациентах с клинической картиной ГД и частичным дефицитом.
В 1999 г. Dieterich и соавт. идентифицировали в сыворотке пациентов с ГД антитела к тканевым трансглютаминазам. На основе разграничения различных типов трансглютаминаз Sardy и соавт. в 2002 г. было показано, что доминирующим аутоантигеном при ГД являются эпидермальные трансглютаминазы. Этот факт был подтвержден исследованием 9 пациентов, проведенным Donaldson и соавторами, которые показали, что отложения эпидермальной трансглютаминазы локализованы совместно с отложениями IgA в верхушках сосочков дермы. Поскольку эпидермальная трансглютаминаза интенсивно экспрессирована в верхних слоях эпидермиса, авторы предположили, что в участках травмы они могут диффундировать через базальную мембрану после высвобождения из эпидермальных кератиноцитов. Эпидермальные трансглютаминазы были также обнаружены в непораженной коже, как минимум, в пяти сантиметрах от очага, что указывает на участие других факторов в развитии очагов герпетиформного дерматита (ГД).
Также известно, что у пациентов, как с ГЧЭ, так и ГД, отмечаются циркулирующие антитела к IgA, направленные против трансглютаминаз. При ГД эти циркулирующие IgA-аутоантитела связываются преимущественно с эпидермальными трансглютаминазами, в то время как у пациентов с истинной ГЧЭ эти аутоантитела связываются преимущественно с тканевыми трансглютаминазами. Точная роль циркулирующих IgA-антител к антигену эпидермальной трансглютаминазы в развитии кожных очагов ГД точно неизвестна. Однако у детей с целиакией уровни циркулирующих IgA-антител к эпидермальной трансглютаминазе ниже, чем у взрослых с целиакией, в то время как уровни IgA-антител к тканевой трансглютаминазе у детей и взрослых с целиакией значительно не отличаются. Это наблюдение привело к гипотезе о том, что распространение эпитопов со временем приводит к появлению IgA-антител к эпидермальной трансглютаминазе, и что позднее появление этих антител может играть определенную роль в том, что ГД типично развивается во второй или третьей декаде жизни.
Механизм, посредством которого IgA-антитела к эпидермальным трансглютаминазам связываются с кожей у пациентов с ГД полностью не выяснен. Одна из длительно существующих гипотез состоит в том, что за отложения IgA в коже больных ГД ответственны содержащие IgA циркулирующие иммунные комплексы. Недавнее открытие IgA-антител к эпидермальной трансглютаминазе привело к предположению, что в коже пациентов с ГД могут откладываться иммунные комплексы «IgA-эпидермальная трансглютаминаза». Однако выяснилось, что совместные периваскулярные отложения IgA и эпидермальной тканевой трансглютаминазы отмечаются только у небольшого количества пациентов. Кроме того, периваскулярные отложения нейтрофилов, которые типично обнаруживаются вместе с периваскулярными отложениями иммунных комплексов, редко встречаются у пациентов с герпетиформным дерматитом (ГД). На этих данных основана альтернативная гипотеза о том, что IgA-антитела к эпидермальной трансглютаминазе могут непосредственно связываться в коже с эпидермальной тканевой трансглютаминазой.
Прямая связь IgA-антител с антигеном эпидермальных трансглютаминаз в коже также не представляет собой полный механизм, поскольку отложения IgA в коже нельзя удалить применением обычного метода элюции (смыва) антитела, непосредственно связанного антигеном. Возможно, что IgA-антитела к эпидермальным трансглютаминазам связываются вначале через взаимодействия «антиген-антитело», при этом способность трансглютаминаз перекрестно связывать белки приводит к перекрестной связи IgA с белками дермы, и в результате в коже пациентов с ГД наблюдаются стойкие и длительные отложения IgA. Эта гипотеза еще ждет своего подтверждения.
Неизвестно также, имеют ли отложения IgA в коже при герпетиформном дерматите (ГД) какое-либо отношение к патогенезу образования пузырей. Присутствие отложений IgA и комплемента практически на всех участках кожного покрова (в том числе за пределами области очагового поражения) позволяет предположить, что если IgA (отдельно или как часть иммунного комплекса) и играет определенную роль в данном процессе, то возникновение очагов, тем не менее, обусловлено также и некими дополнительными факторами. Согласно исследованию Takeuchi и соавт., минимальная травма кожи приводит к повышению экспрессии IL-8 и Е-селектина, причем и тот и другой могут предрасполагать к образованию воспалительного нейтрофильного инфильтрата. В связи с этим, поскольку очаги ГД во многих случаях возникают на подвергшихся травмированию участках разгибательных поверхностей, можно предположить, что одним из инициирующих факторов высыпаний ГД является локальная выработка цитокинов/хемоки-нов.
Возможно, в результате связывания первоначального нейтрофильного инфильтрата с кожным IgA происходит высвобождение таких факторов, как цитокины, хемокины и протеазы, что непосредственно вызывает образование пузыря и стимулирует базальные кератиноциты к синтезу коллагеназ или стромелизина-1, которые в свою очередь способствуют дальнейшему образованию пузырей. В других исследованиях патогенез кожных очагов связывается с Т-клетками; тем не менее специфического Т-клеточного ответа на глютен не обнаружено.
Тот факт, что прием йодидов внутрь способен вызывать герпетиформный дерматит (ГД) или ухудшать его течение, ранее использовался в диагностических целях. С появлением иммунопатологических методов обнаружения отложений IgA в коже подобные провокационные тесты вышли из употребления.
Отсутствие как естественных, так и экспериментальных моделей заболевания на животных долгое время ограничивало возможности изучения патогенеза ГД. Модель ГД на мышах недавно была описана Marietta и соавт. Исследователи обнаружили, что у трансгенных мышей линии NOD (аббр. от англ, non-obese diabetic mouse—не страдающие ожирением мыши с диабетом) при иммунизации глютеном развивались нейтрофильные кожные очаги одновременно с отложениями IgA в коже. Кроме того, исключение глютена из рациона питания животных приводило к разрешению кожных очагов. Дальнейшее изучение данной модели, вероятно, будет способствовать лучшему пониманию патогенеза ГД. Наконец, имеются несколько сообщений о начале ГД при приеме таких медикаментов как интерферон, рибаварин и аналог гонадотропин-высвобождающего гормона.
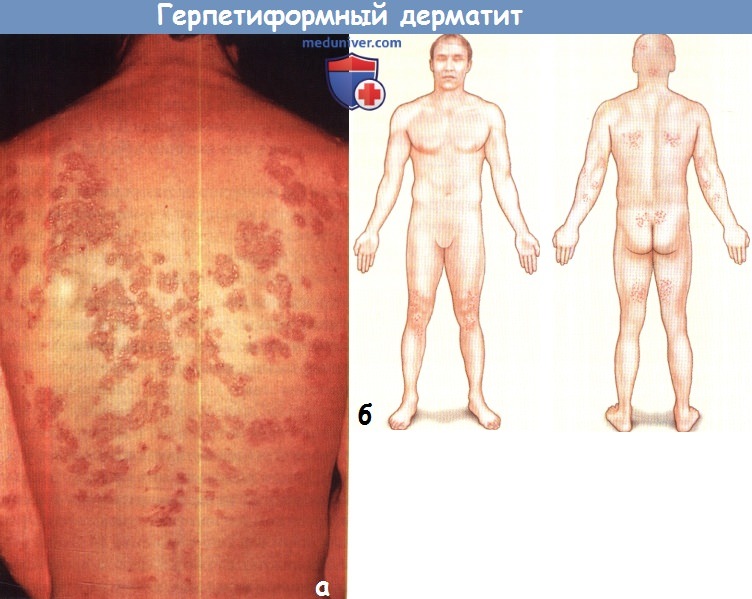
б - Распределение высыпаний при герпетиформном дерматите.
- Рекомендуем далее ознакомиться со статьей "Симптомы и клиника герпетиформного дерматита"
Оглавление темы "Герпетиформный дерматит.":
