Боррелиоз Лайма: эпидемиология, этиология, патогенез
Боррелиоз Лайма - краткий обзор:
- Болезнь Лайма вызывается спирохетами Borrelia burgdorferi.
- Клиническое течение заболевания может быть затяжным, затрагивая множество систем органов.
- Кожными проявлениями заболевания являются мигрирующая эритема и атрофический хронический акродерматит.
- Диагноз обычно устанавливается на основании клинической картины и/или серологических исследований.
- Высокоэффективна ранняя антибиотикотерапия (доксициклин, амоксициллин или цефуроксим).
Боррелиоз Лайма, или болезнь Лайма, является самым распространенным заболеванием, вызываемым членистоногими, как в США, так и в Европе. Болезнь впервые выявлена в 1970-х годах после эпидемиологических исследований серии случаев олигоартрита у детей в Западном Коннектикуте, когда была предположена микробная этиология заболевания. В 1981 г. из среднего отдела кишечника клеща Ixodes dammini (в настоящее время известного как I. scapularis) Бургдорфер (Burgdorfer) изолировал новую спирохету — Borrelia burgdorferi.
Последующее выделение микроорганизма из кожных высыпаний, спинномозговой жидкости (СМЖ) и образцов крови у пациентов с болезнью Лайма как в США, так и в Европе позволило окончательно связать заболевание с В. burgdorferi.
а) Эпидемиология боррелиоза Лайма. Бактерия В. burgdorferi в северо-восточных штатах США, существовала, вероятно, за несколько тысяч лет до прибытия туда переселенцев из Европы. Сфера действия и ареал распространения организма постоянно растут с момента его идентификации в 1970-х годах. Считается, что в новые зоны инфицированных клещей доставляют, в первую очередь, птицы и олени. В США по инициативе Центра по контролю и профилактике заболеваний (CDC) в 1982 г. организован надзор за болезнью Лайма, а в 1991 г. Советом по государственной и территориальной эпидемиологии болезнь Лайма была отнесена к подлежащим обязательной регистрации. С 1982 г. Советом было зарегистрировано более 200000 случаев.
В 2006 году число новых случаев заболевания в Соединенных Штатах достигло 19931 (средняя заболеваемость в стране составила 0,5 случая на 100000 человек). С 1992 года наблюдается рост ежегодной заболеваемости на 101%. Считается, что показатели заболеваемости болезнью Лайма занижены, и действительное число новых случаев в США приближается к 150000 в год. В течение пятнадцатилетнего периода, за который Центр контроля и профилактики заболеваний в США (CDC) располагает соответствующими данными, примерно 93% зарегистрированных случаев произошли в десяти штатах, расположенных в Северо-Восточном, Среднеатлантическом и Центрально-Северном регионах США: Коннектикуте, Делавэре, Мэне, Мериленде, Массачусетсе, Миннесоте, Нью-Хэмпшире, Нью-Джерси, Нью-Йорке, Пенсильвании, Род-Айленде и Висконсине.
За последние 15 лет практически во всех штатах в определенные моменты времени были зарегистрированы случаи болезни Лайма, хотя средняя заболеваемость значительно варьирует: от 0,0 в Колорадо, Монтане и на Гавайях, до 73,6 на 100000 человек в Коннектикуте. Во многих штатах с низкой заболеваемостью случаи болезни зарегистрированы у лиц, инфицированных во время поездки в более эндемические регионы.
Болезнь Лайма также широко распрастранена в Европе, каждый год выявляется приблизительно 120000 новых случаев. Чаще заболевание выявляется в лесных районах Центральной и Северной Европы (Германия, Австрия, Словения и Швеция). Эта инфекция также встречается в западных областях России и Китая, Корее и Японии.
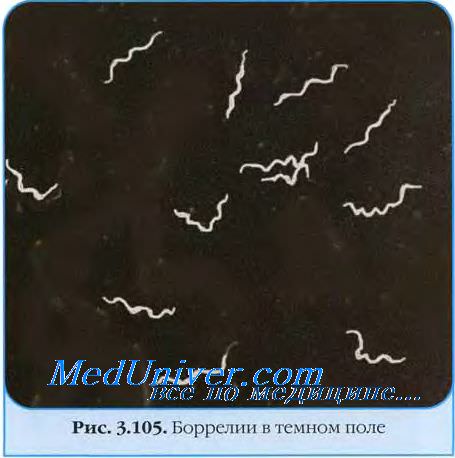
б) Этиология боррелиоза Лайма:
1. Возбудитель. Borrelia burgdorferi sensu lato, вызывающая боррелиоз Лайма, относится к эубактериям спирохетам — легко подвижным извитым бактериям. Геном боррелий состоит из линейной хромосомы и более чем 20 кольцевидных и линейных плазмид — самого большого количества, известного у бактерий. Некоторые плазмиды можно считать микрохромосомами, так как они необходимы для выживания организма. Среди интересных характеристик микроорганизма можно отметить большое число липопротеинов (более 150). В геноме В. burgdorferi отсутствуют гены токсинов или других идентифицируемых факторов вирулентности. У боррелии также отсутствует аппарат биосинтеза для продукции многих важных веществ (например, аминокислот, жирных кислот), что говорит о том, что В. burgdorferi в значительной степени зависима от хозяина, от которого она получает основные питательные вещества.
В пределах типа В. burgdorferi sensu lato в мире описано одиннадцать видов боррелий (Borrelia sp.). Доказано, что только три из них — (1) В. burgdorferi sensu stricto, (2) В. afzelii и (3) В. garinii — патогенны для человека и вызывают боррелиоз Лайма, хотя другие виды также изучаются в свете отношения к заболеваниям человека (включая В. bissettii и В. Lonestari).
В США этиологическим агентом болезни Лайма является исключительно В. burgdorferi sensu stricto. В. afzelii и В. garinii вызывают большинство случаев болезни Лайма в Европе, хотя присутствует и В. burgdorferi sensu stricto. В Азии подтверждено существование только В. afzelii и В. garinii.
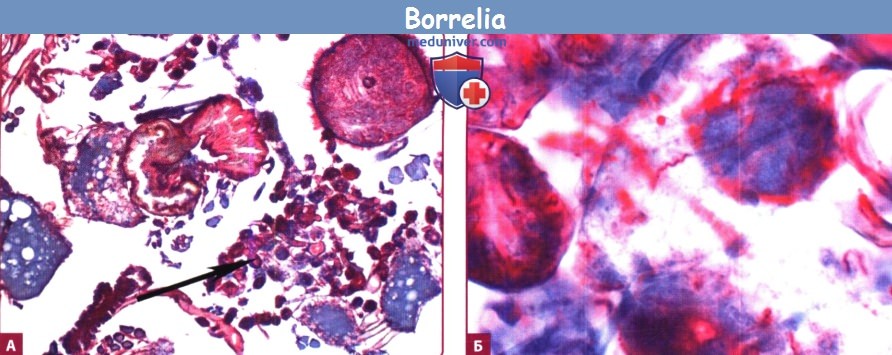
2. Жизненный цикл возбудителя болезни Лайма. В. burgdorferi поддерживает жизненный цикл в природе за счет мелких грызунов, птиц и клещей видов Ixodes. Не будучи сами по себе резервуаром для В. burgdorferi, олени являются важными хозяевами взрослых клещей, и снижение популяции оленей может вести к значительному уменьшению популяции клещей.
Иксодовые клещи имеют двухлетний, трехэтапный (личинка или ларва, нимфа и взрослая особь) жизненный цикл. Клещи заражаются В. burgdorferi на личиночной стадии, питаясь кровью инфицированных животных, и поддерживают инфекцию на протяжении последующего превращения в нимфальную и взрослую стадию. В. burgdorferi между кормлениями находится в латентном состоянии, сохраняясь в среднем отделе кишечника клеща. На каждой стадии жизненного цикла клеща требуется одно кормление кровью: ларвы питаются в конце лета, нимфы — весной и ранним летом, а взрослые клещи — осенью и ранней зимой. Важнейшими резервуарами для В. burgdorferi являются мелкие грызуны и птицы, на которых кормятся клещи на личиночной и нимфальной стадиях. Взрослые клещи кормятся на крупных млекопитающих (оленях), которые не являются собственно резервуаром В. burgdorferi. Человек является случайным хозяином, не значимым для поддержания популяции В. burgdorferi.
Большинство случаев заболеваемости человека возникают поздней весной и летом, когда нимфы наиболее активны, а время пребывания людей на природе возрастает.
Клинически значимым является тот факт, что некоторые иксодовые клещи наряду с болезнью Лайма являются переносчиками и других клещевых инфекций: клещи I. scapularis в США и I. ricinus в Европе могут переносить Babesia microti (паразит эритроцитов) или Anaplasma phagocytophilum (раннее считался возбудителем гранулоцитарного эрлихиоза человека). I. ricinus в Европе и I. persulcatus в Азии также являются переносчиками вируса клещевого энцефалита.
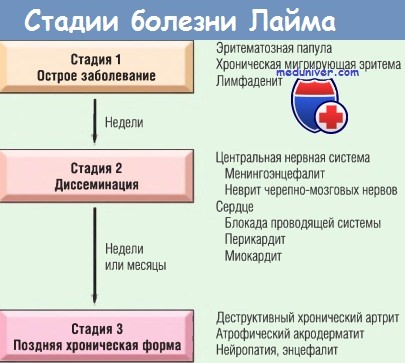
в) Патогенез болезни Лайма. Попав в кожу хозяина В. burgdorferi быстро распространяется по кровотоку из очага первичного заражения, оседая во множестве очагов. Время от заражения до диссеминации варьирует от трех дней до нескольких недель.
В. burgdorferi обладает развитыми механизмами адаптации и выживания в различных условиях. На протяжении жизненного цикла микроорганизм экспрессирует широкий спектр белков, отвечающих за связывание с белками хозяина, миграцию в пределах тканей, передачу и уход от иммунного ответа. Хорошо известным примером адаптации к хозяину является широкая экспрессия наружных поверхностных белков (Osp) А и С. Считается, что белок OspA, экспрессирующийся изначально во время дремлющей стадии в среднем отделе кишечника клеща, служит якорем для связывания с белком кишечника клеща TROSPA. Когда клещ начинает кормление кровью хозяина, происходит снижение синтеза белка OspA, высвобождение В. burgdorferi из кишечника клеща, размножение и миграция к слюнным железам. Этот процесс занимает 24-48 часов, что объясняет, почему удаление клеща в пределах 24 часов после прикрепления предотвращает передачу заболевания.
При подавлении синтеза OspA происходит активация синтеза OspC, который стимулирует миграцию бактерии из кишечника в слюнные железы клеща. OspC связывается с белком слюны Salp 15, защищающим бактерию от элиминации иммунной системой хозяина. Иммуносупрессивное действие слюны клеща также стимулирует развитие ранней инфекции. Например, слюна клеща содержит белки, которые связываются с хемокинами организма-хозяина. Эти белки, называемые эвазинами, помогают подавить рекрутирование воспалительных клеток в зону питания клеща, позволяя паразиту беспрепятственно насыщаться и иногда обеспечивая защиту таким организмам, как В.burgdorferi, которые передаются человеку во время питания клеща.
Кроме того, В. burgdorferi связывает фактор хозяина Н для защиты от комплемент-опосредованной иммунной реакции. Специфичность штаммов В. burgdorferi к фактору Н различных видов животных может частично объяснять различия в тропности к видам хозяев. Было показано, что В. burgdorferi приводит к усилению синтеза таких протеаз хозяина, как матриксные металлопротеиназы кожи и суставов, которые могут играть важную роль в патогенезе при растворении белков внеклеточного матрикса, что обусловливает диссеминацию, однако этот вопрос требует дальнейших подробных исследований.
г) Иммунология. В контроле инфекции В. burgdorferi важную роль играет как врожденный, так и приобретенный иммунитет; однако ни один обычно не может элиминировать инфекцию. Фагоцитоз, как комплемент-опосредованный, так и комплемент-независимый, является первой линией защиты против В. burgdorferi. Естественные антитела (поликлональные антитела IgM) также могут функционировать в качестве первой линии защиты против В. burgdorferi, убивая спирохет в среднем отделе кишечника клеща во время кормления паразита, и ограничивая распространение бактерии до развития специфического адаптивного иммунного ответа.
Попав в организм хозяина, В. burgdorferi вызывает сильное воспаление. Наружные поверхностные липопротеины являются провоспалительными стимулами. Распознавание боррелиозных липопротеинов происходит посредством связывания с гетеродимерами 1 и 2 Toll-подобных рецепторов, инициирующих каскад внутриклеточных сигналов с кульминацией в виде продукции провоспалительных цитокинов, хемокинов и других молекул, важных для защиты хозяина. Исследования на мышах, не имеющих Toll-подобных рецепторов, показали, что В. burgdorferi стимулирует также другие патологические пути, приводящие к высвобождению медиаторов воспаления. Среди других рецепторов врожденного иммунитета, распознающих В. burgdorferi и опосредующих воспаление, можно назвать интегриновые рецепторы.
Развитие специфического гуморального иммунного ответа обычно происходит в течение недель или месяцев. Пик синтеза IgM приходится на 3-6 недели от начала заболевания и может держаться несколько месяцев или лет; ответ IgG обычно отстает от IgM на несколько недель, поэтому у большинства пациентов IgG определяется через 4-6 недель после инфицирования. Развитие гуморального ответа, то есть появление антител, обычно свидетельствует о значительном снижении числа микроорганизмов и уровня воспаления. Кстати, достигнутый гуморальный ответ обычно не защищает от реинфекции, частично вследствие значительной вариабельности эпитопов защитных антигенов между штаммами В. burgdorferi и отсутствия экспрессии менее вариабельных защитных антигенов (например, OspA) у хозяина-млекопитающего.
- Рекомендуем далее ознакомиться со статьей "Кожа при боррелиозе Лайма: симптомы, клиника"
Редактор: Искандер Милевски. Дата публикации: 9.4.2019

