Внешний путь развития апоптоза
Внешний путь развития апоптоза инициируется рецепторами смерти плазматической мембраны на разных клетках. Рецепторы смерти являются белками семейства рецепторов TNF, содержащими цитоплазматический домен, вовлеченный во взаимодействие белок-белок и называемый доменом смерти, поскольку он необходим для передачи сигналов к запуску апоптоза. (Некоторые белки семейства рецепторов TNF не содержат домена смерти, их функция состоит в активации воспалительного каскада, и их роль в запуске апоптоза не совсем понятна.)
Подробно изучены рецепторы смерти TNF-1 и связанный белок Fas (CD95), но были описаны и другие. Механизм развития апоптоза, индуцированный этими рецепторами смерти, хорошо изучен на примере рецептора Fas, экспрессируемого на многих типах клеток.
Его лиганд FasL экспрессируется на Т-клетках (распознающих собственные антигены и удаляющих аутоагрессивные лимфоциты) и на некоторых цитотоксических Т-лимфоцитах (убивающих инфицированные вирусом и опухолевые клетки).
Когда FasL присоединяется к Fas, три молекулы Fas или более собираются вместе и их цитоплазматические домены смерти формируют участок для связи с белком-адаптером, который содержит Fas-ассоциированный домен смерти (FADD).
В свою очередь, FADD, связанный с рецепторами смерти, через домен смерти присоединяется к неактивной форме каспазы-8 — прокаспазе-8 (и прокаспазе-10 у человека). Таким образом, множество молекул прокаспазы-8 собираются вместе и расщепляют друг друга для генерации активной каспазы-8.
Затем фермент запускает активацию каскада каспаз, активируя другие прокаспазы, и активные ферменты опосредуют фазу, запускающую апоптоз. Этот путь развития апоптоза может быть ингибирован белком FLIP, который присоединяется к прокаспазе-8, но не может ее расщепить и превратить в активную форму, т.к. у него отсутствует протеазный домен.
Некоторые вирусы и нормальные клетки продуцируют FLIP и используют его для защиты от Fas-опосредованного апоптоза.
Внутренний и внешний пути развития апоптоза разные, т.к. при инициации вовлекают совершенно разные молекулы, но эти пути могут быть взаимосвязаны. Например, в гепатоцитах и некоторых других видах клеток сигнал Fas активирует белок ВН3-only (Bid), который затем активирует внутренний путь развития апоптоза.
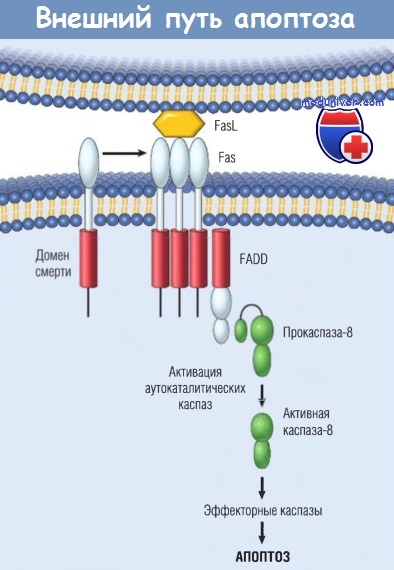
FADD — Fas-ассоциированный домен смерти; FasL — Fas-лиганд.
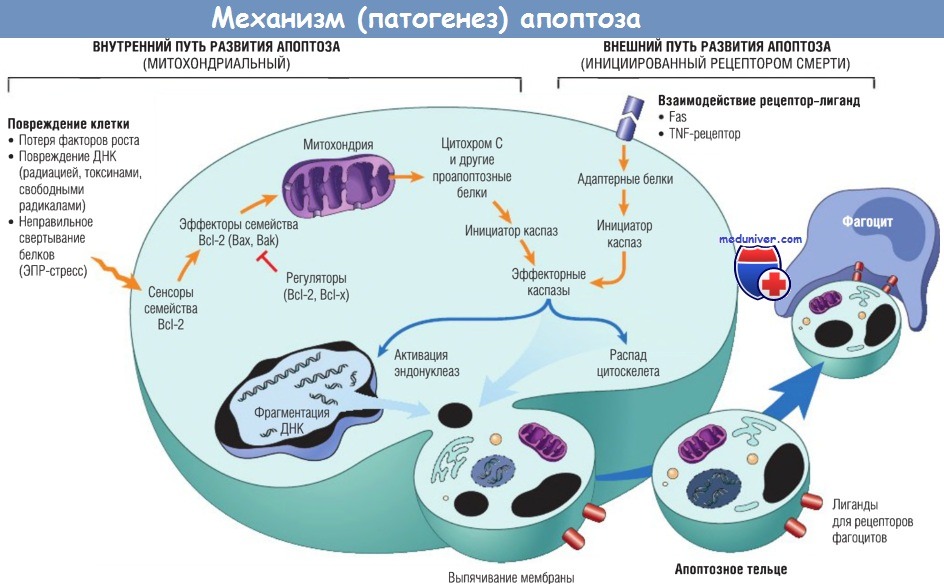
Два пути развития апоптоза отличаются индукцией и регуляцией, но оба заканчиваются активацией эффекторных каспаз.
При внутреннем пути развития апоптоза индукция вовлекает сенсоры и эффекторы семейства Bcl-2, которые индуцируют выход митохондриальных белков.
Показаны также некоторые антиапоптозные белки (регуляторы), которые ингибируют митохондриальный выход и активацию цитохром С-зависимой каспазы во внутреннем пути.
При внешнем пути развития апоптоза инициация рецепторов смерти напрямую вызывает активацию каспаз.
Регуляторы активации каспаз, опосредованные рецептором смерти, не показаны.
TNF — фактор некроза опухоли; ДНК — дезоксирибонуклеиновая кислота; ЭПР — эндоплазматический ретикулум.
- Рекомендуем ознакомиться со следующей статьей "Механизмы запуска апоптоза"
Оглавление темы "Патология клетки":- Ишемическое и гипоксическое повреждение клеток
- Реперфузионное повреждение клетки после ишемии
- Механизмы химического повреждения клетки
- Что такое апоптоз? Причины апоптоза
- Морфологические изменения при апоптозе
- Биохимические признаки апоптоза
- Механизмы апоптоза и их патогенез
- Внутренний путь развития апоптоза
- Внешний путь развития апоптоза
- Механизмы запуска апоптоза

