Схема болезней клеток нервной системы - нейронов
Для выполнения своих функций нейроны должны быть способны не только получать информацию от других клеток, но и передавать ее другим клеткам. Как правило, нейроны воспринимают информацию с помощью мембранных рецепторов, активируемых нейротрансмиттерами. Активность ионных каналов нейронов регулируется либо непосредственно нейротрансмиттерами, либо с помощью внутриклеточных механизмов, запускаемых нейротрансмиттерами.
Так, ацетилхолин (АХ) в соответствующих нейронах открывает неспецифические катионные каналы, через которые затем будет осуществляться движение Na+ и К+. Это приведет к деполяризации клеточной мембраны и к открытию потенциалзависимых Na+- и Са2+-каналов. Затем ионы Са2+ вызывают высвобождение нейротрансмиттеров клеткой-мишенью. Долговременные эффекты таких воздействий характеризуются изменениями метаболизма клетки-мишени, характера экспрессии генов, процессов образования синапсов, а также синтеза и накопления нейротрансмиттеров в этой клетке.
Патологические изменения могут затрагивать любой элемент этого каскада. Например, может снижаться плотность рецепторов или подавляться их активность. Помимо этого могут блокироваться различные механизмы внутриклеточной передачи сигнала, например, в случае блокады G-белков различными веществами, в т. ч. и коклюшным токсином.
Некоторые лекарственные средства способны блокировать ионные каналы, активность которых может изменяться ионами Ca2+, Mg2+ или Н+. Нарушение мембранного потенциала нейронов может быть следствием изменения ионных градиентов, в частности, при увеличении или уменьшении внутриклеточной либо, что более важно, внеклеточной концентрации К*. Такое возможно при снижении активности Na+/K+-АТФазы, например, при гипоксии и дефиците энергии.
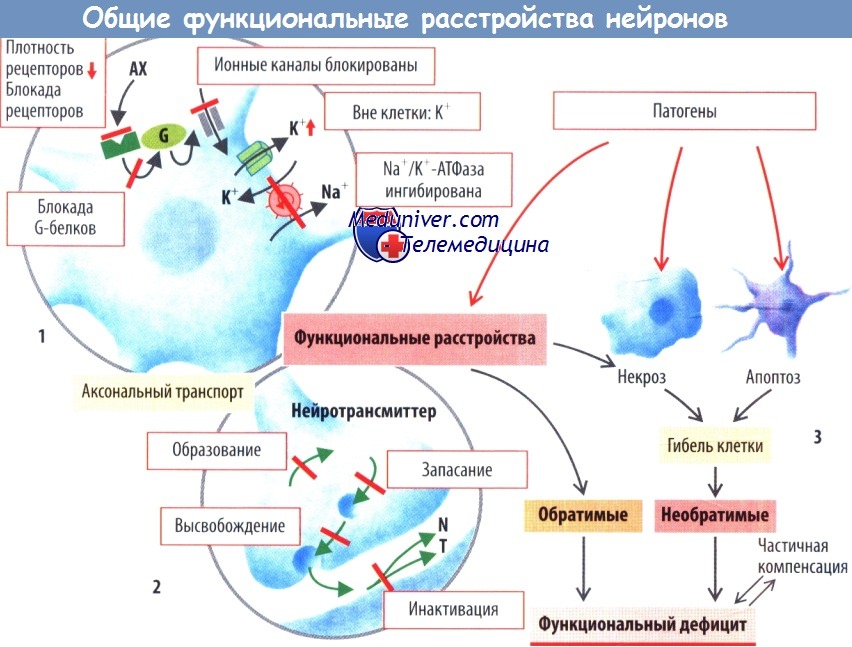
Процессы аксонального транспорта, а также образование, запасание, высвобождение и инактивация нейротрансмиттеров могут страдать при различных генетически обусловленных формах патологии или в результате воздействия некоторых лекарственных средств. Примечательно, что функциональные расстройства потенциально обратимы при прекращении действия повреждающего фактора.
Возможно и необратимое разрушение нейронов. Так, нейроны могут погибать вследствие их прямого повреждения (некроз, вызванный дефицитом энергии или механическим разрушением) или апоптоза. Усиленный апоптоз играет важную роль в механизмах развития нейродегенеративных заболеваний (болезнь Альцгеймера, хорея Хантингтона, боковой амиотрофический склероз, младенческая дистрофия спинных мышц), а также служит одной из причин гибели клеток во время ишемии.
Апоптоз нейронов запускается при самых разнообразных расстройствах, включая недостаточную активность NOS, снижена активности поли-АДФ-рибозополимеразы или супероксиддисмутазы (СОД). В мозге взрослых погибшие нейроны новыми практически не замещаются (в ограниченной степени замещение погибших нейронов возможно в гиппокампе и обонятельных луковицах). Следовательно, гибель нейронов обычно приводит к необратимой утрате функции, даже если остальные нейроны будут способны частично взять на себя функции погибших.
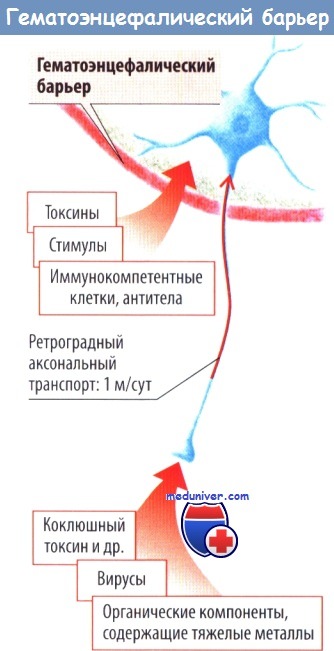
Вредные вещества могут проходить через гематоэнцефалический барьер и достигать нейронов, расположенных в ЦНС. Интактный гематоэнцефалический барьер препятствует прохождению через неге большинства веществ, патогенов и иммунокомпетентных клеток. Однако некоторые токсины (коклюша и ботулотоксин) достигают нейронов спинного мозга посредством аксонального ретроградного транспорта по периферическим нервам, минуя таким образом гематоэнцефалический барьер. Аналогичным образом в ЦНС попадают некоторые вирусы.
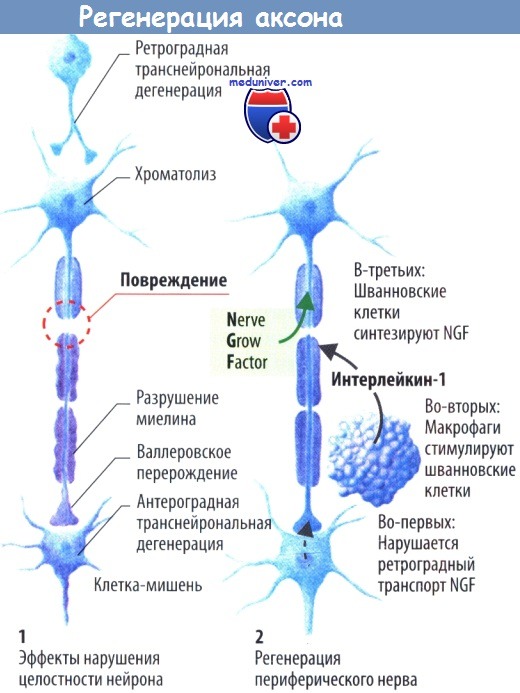
Если аксон расчленен механически, дистальная его часть погибает (валлеровское перерождение). Аксоны центральных нейронов, как правило, не способны расти вновь, и поврежденный нейрон, скорее всего, погибнет в результате апоптоза. Такой же сценарий наблюдается и при отсутствии фактора роста нервов (NGF), который в обычных условиях высвобождается иннервируемыми постсинаптическими клетками и, распространяясь по аксонам, обеспечивает выживание пресинаптических клеток.
Аксональную регенерацию подавляют внеклеточные макромолекулы, такие как хондроитинсульфат, гликопротеид миелина олигодендроцитов (OMGP), белок, ассоциированный с миелином (MAG), и Nogo. Нарушение ретроградного аксонального транспорта в остальных интактных аксонах также приводит к гибели нейрона. Проксимальная культя периферического нейрона способна отрастать. Белки, необходимые для этого процесса, образуются в клетке и доставляются к месту повреждения с помощью аксонального транспорта.
Возможно, поврежденные клетки выживают вследствие того, что макрофаги, мигрирующие к периферическим нервам, образуют IL-1, который стимулирует продукцию NGF шванновскими клетками. В то же время макрофаги не способны проникать в ЦНС.
Рассечение или полный разрыв аксона вызывают не только гибель поврежденного нейрона. Отсутствие иннервации часто приводит к гибели клетки-мишени (антероградная транснейрональная дегенерация), а иногда и к гибели клеток, иннервируемых поврежденным нейроном (ретроградная транснейрональная дегенерация).
Учебное видео - строение нейрона
- Рекомендуем ознакомиться со следующей статьей "Схема развития демиелинизации нервов при рассеянном склерозе"
Оглавление темы "Патофизиология в схемах":- Схема последствий избытка инсулина и развития гипогликемии
- Схема функций гистамина и брадикинина
- Схема функций серотонина
- Схема функций эйкозаноидов
- Схема вариантов повреждений нервной системы
- Схема болезней клеток нервной системы - нейронов
- Схема развития демиелинизации нервов при рассеянном склерозе
- Схема нарушения нервно-мышечной передачи при миастении и синдроме Ламберта-Итона
- Схема поражения двигательной единицы, миотонии и мышечной дистрофии
- Схема электромиографии и образования креатинина

