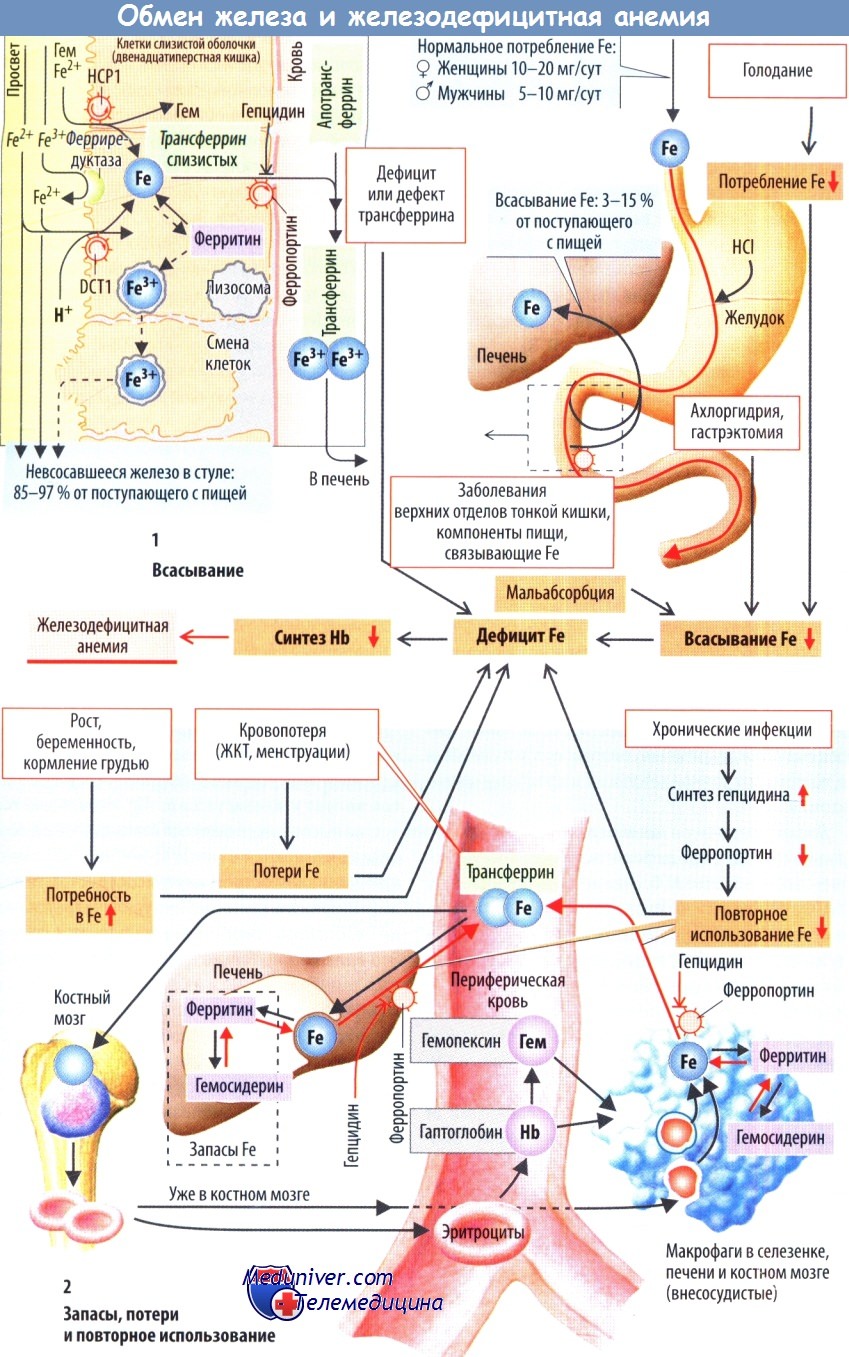
Схема развития железодефицитной анемии
Запасы железа в организме составляют 2 г у женщин и 5 г у мужчин. Они состоят из железа, связанного с гемоглобином, депонированного железа (ферритин, гемосидерин) и железа, выполняющего различные функции (миоглобин, железосодержащие ферменты). Суточные потери железа составляют 1 мг у мужчин и 2 мг у женщин (менструация, беременность, роды). В двенадцатиперстной кишке всасывается 3-15 % железа, поступающего с пищей, причем в условиях дефицита железа этот показатель повышается до 25 %. Следовательно, с пищей человек должен получать хотя бы 10-20 мг/сут железа (женщины > дети > мужчины).
Всасывание железа. Железо достаточно эффективно всасывается с помощью переносчика гема НСР1, который обеспечивает транспорт гемового Fe2+, содержащегося в мясе и рыбе. Железо, освобожденное от гема, либо поступает в кровь, либо запасается в клетках слизистой оболочки в виде ферритина (Fe3+). При слущивании клеток слизистой оболочки это железо вновь оказывается в просвете кишки. Негемовое железо может всосаться только в форме Fe2+ с помощью белка-переносчика DCT1, осуществляющего ко-транспорт Fe2+-H+. Крайне важно для всасывания этого железа низкое значение pH химуса, т. к. оно способствует:
1) увеличению градиента Н+, обеспечивающего поступление Fe2+ в клетки с помощью DCT1, и
2) высвобождению железа из компонентов пищи.
Негемовое железо пищи Fe3+ должно восстанавливаться ферриредуктазой в присутствии аскорбата в Fe2+ на поверхности клеток слизистой оболочки, обращенной в просвет кишечника. Для поступления железа в кровь Fe2+ должно окислиться до Fe3+ медьсодержащим белком с ферроксидазными свойствами гефе-стином (при поступлении железа из слизистой кишечника) или церулоплазмином (при поступлении железа в кровь из макрофагов).
Выход Fe2+ из клеток обеспечивается переносчиком железа ферропортином, встроенным в мембрану эпителиальных клеток двенадцатиперстной кишки, гепатоцитов и макрофагов. Ферропортин интернализуется (путем эндоцитоза убирается внутрь клетки). Этот процесс подавляется гормоном белковой природы гепцидином, образующимся в печени.

В крови Fe3+ взаимодействует с апоферритином (в соотношении 2:1) с образованием трансферрина, который обеспечивает перенос железа в плазме и доставляет Fe3+ к рецепторам трансферрина на эритробластах, гепатоцитах и клетках некоторых других тканей (например, плаценты). После высвобождения Fe3+ апотрансферрин вновь становится свободным и может опять связывать Fe из клеток кишечника и макрофагов.
Запасы железа состоят из ферритина (быстро доступного Fe) и гемосидерина. Для утилизации железа Hb-Fe и гем-Fe, выделяющиеся из неправильно сформированных эритробластов (неэффективный эритропоэз) и гемолизированных эритроцитов, связываются соответственно с гаптоглобином и гемопексином и захватываются макрофагами в костном мозге или в печени и селезенке посредством эндоцитоза. Таким образом повторно используется 97 % Fe.
Трансферрин, проходящий через почечный фильтр, возвращается в кровоток путем реабсорбции в почечных канальцах.
При дефиците железа всасывание Fe в кишечнике увеличивается вследствие замедления трансляции ферритина (это возникает из-за связывания железорегулирующего белка IRP1 с мРНК ферритина) и уменьшения образования гепцидина.
При клинически явном дефиците железа (Fe сыворотки < 0,4 мг/л; снижение ферритина) синтез гемоглобина подавляется и развивается гипохромная микроцитарная анемия, характеризующаяся МСН < 26 пг, MCV < 70 фл, НЬ < 110 г/л.
Эта анемия может быть обусловлена следующими причинами: кровологеря(из ЖКТ, обильное менструальное кровотечение) бывает самой частой причиной дефицита железа у взрослых (с 1 мл крови теряется 0,5 мг железа); нарушение утилизации железа. Эта форма анемии (2-е место по частоте) развивается при хронических инфекционных заболеваниях, при которых провоспалительные цитокины (IL-1, IL-6, TNF-a и др.) стимулируют синтез гепцидина, который подавляет образование ферропортина, поэтому железо накапливается в макрофагах; недостаточное поступление железа (недостаточное питание, особенно в развивающихся странах); нарушение всасывания железа в результате ахлоргидрии (при атрофическом гастрите, после гастрэктомии) и мальабсорбции при заболеваниях верхних отделов тонкой кишки или при наличии в пище компонентов, связывающих железой препятствующих его всасыванию (фитаты в составе злаков и овощей, таниновая кислота в чае, оксалаты и др.); повышение потребности в железе (период интенсивного роста, беременность, грудное вскармливание); дефекты апотрансферрина (встречаются редко).
Если развивается перегрузка железа, происходит повреждение клеток печени, поджелудочной железы и миокарда (гемохроматоз).
- Рекомендуем ознакомиться со следующей статьей "Схема развития гемолитической анемии"
Оглавление темы "Патофизиология в схемах":- Схема развития мегалобластной анемии (В12-дефицитной анемии, анемии дефицита фолиевой кислоты)
- Схема развития анемии при нарушении синтеза гемоглобина
- Схема развития железодефицитной анемии
- Схема развития гемолитической анемии
- Схема организации иммунной системы человека
- Схема развития воспаления
- Схема развития аллергии - рекции гиперчувствительности первого типа
- Схема развития аллергической рекции второго типа (цитотоксического)
- Схема развития аллергической рекции третьего типа (иммунокомплексного)
- Схема развития аллергической рекции четвертого типа (замедленного)

