Заживление раны сердца после диафрагмопластики. Коллатеральное кровообращение сердца
Через 2 нед установлено сращение диафрагмального лоскута с эпикардом прослойкой молодой грануляционной ткани, которая содержала большое количество сосудов, макрофагов, гистиоцитов и лимфоидных клеток, изредка встречались фибробласты и соединительнотканные волокна. Раневой канал в мышце сердца был заполнен грануляционной тканью, характеризующейся разнообразным клеточным составом. Местами обнаруживались сосуды с эритроцитами в их просвете.
В миокарде по ходу раневого канала, встречались волокна с выраженными дистрофическими и некробиотическими изменениями, между которыми отмечено разрастание соединительной ткани.
В более поздние сроки после операции (спустя 2 мес и больше) в месте ранения обнаружена плотная фиброзная ткань, содержащая сосуды и отдельные клеточные элементы. Она разрасталась также и между волокнами сердечной мышцы. Со стороны эндокарда рубцовая ткань имела зндотелиальный покров. Диафрагмальный лоскут сохранял свою структуру и хорошую васкуляризацию. Прослойкой соединительной ткани он был сращен с миокардом.
Проведенные исследования свидетельствуют о том, что диафрагмальный лоскут на ножке может быть успешно использован для замещения дефекта сердечной стенки. Лоскут обеспечивает герметичность раны сердца, надежный гемостаз, не подвергается аневризматическому выпячиванию и не ограничивает амплитуду сердечных сокращений.
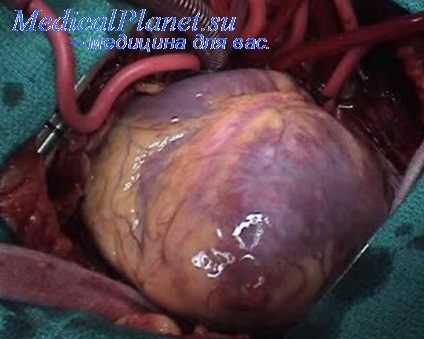
Заживление раны сердца при пластике диафрагмальный лоскутом происходит путем образования соединительнотканных сращений между тканями лоскута и миокарда, а изнутри развивается зндотелиальный покров. Сращения между миокардом и диафрагмальным лоскутом содержат обилие кровеносных сосудов.
Резекция ишемического участка миокарда значительно отягощает течение послеоперационного периода, что свидетельствует о необходимости применения комплекса медикаментозных средств и дальнейшей разработке техники оперативных вмешательств.
Коллатеральное кровообращение сердца
За последний период большим достижением восстановительной хирургии явилось внедрение в клинику операций, направленных на создание прямых аорто-коронарных анастомозов.
В настоящее время установлено, что главной причиной ангинозных болей и инфаркта миокарда является недостаточное количество крови в отдельном участке сердечной мышцы. При этом большое значение приобретает не столько фактор трофики миокарда вообще, сколько фактор равномерного поступления крови в каждую его часть.
Следовательно, в проблеме хирургического лечения нарушений венечного кровообращения важное значение приобретают операции, направленные на создание дополнительного притока крови к миокарду, а также способствующие равномерному перераспределению крови по внутриорганным анастомозам.
Учение о коллатеральном кровообращении и реваскуляризации миокарда имеет богатую экспериментальную базу и известный клинический опыт, подтверждающий эффективность различных операций (А. Н. Бакулев, В. И. Пронин, 1963; В. И. Колесов, 1966; Beck 1949; Bigelow с соавт., 1963, и др.). Однако существует немало разногласий среди исследователей в оценке органокардиопексий (Б. П. Кириллов, 1964).
Эти противоречия сводятся главным образом к таким моментам: травматичность операций, связанных с торакотомией, а нередко и со вскрытием брюшной полости; нефизиологичность вмешательства, сопряженного с подшиванием любой ткани к сердцу; отрицание образования анастомозов между коронарными артериями и артериями ткани-реваскуляризатора; недолговечность вновь созданных анастомозов и их облитерация в соединительнотканных сращениях с миокардом; рубцовая трансформация и обеднение сосудами любой ткани, используемой для реваскуляризации; преобладание оттока крови по венозным коллатералям в сращениях с миокардом и, следовательно, обеднение его кровью вместо предполагаемого обогащения; преобладание нервнорефлекторных влияний, а не сосудистых, при подшивании различных тканей; наличие сопутствующего воспалительного процесса в сращениях, его длительность и интенсивность; изменение физических условий работы сердца в связи с торако-, перикардиотомией или перикардиоперитонеостомией (абдоминализация сердца); изменение электрических потенциалов и ионного равновесия, вследствие создания сращений между эпикардом и другими тканями; зависимость эффекта операции от выбора ткани-реваскуляризатора и использования метода создания сращений (химического, физического, биологического, механического и др.); степень ишемии миокарда, скорость ее возникновения и выраженность внутриорганных анастомозов, наряду с состоянием компенсаторно-приспособительных механизмов организма.
- Читать далее "Реваскуляризация миокарда. Эффективность реваскуляризации миокарда"
Оглавление темы "Оперативное лечение аневризм сердца":1. Диафрагмопластика аневризмы сердца. Иссечение аневризмы сердца
2. Эксперименты диафрагмопластики аневризмы сердца. Течение диафрагмопластики аневризмы сердца
3. Зоны повреждения сердца. Морфология диафрагмопластики аневризмы сердца
4. Заживление раны сердца после диафрагмопластики. Коллатеральное кровообращение сердца
5. Реваскуляризация миокарда. Эффективность реваскуляризации миокарда
6. Лиенокардиопексия. Кардиоперикардиопексия и ее последствия
7. Оментокардиопексия и ее последствия. Оценка прогноза операций реваскуляризации миокарда
8. ЭКГ после реваскуляризации миокарда. Экспериментальный инфаркт после реваскуляризации миокарда
9. Подшивание тканей к миокарду. Эффективность подшивания мышц к миокарду для реваскуляризации
10. Трансмуральные пункции миокарда. Влияние пункций миокарда на величину некроза при инфаркте

