Минеральный обмен и питание кости
Кальций и фосфор играют важную роль в целом ряде физиологических процессов. Более 98 % кальция и 85 % фосфора организма сжаты в кристаллы гидроксиапатита кости и способны участвовать только в очень медленном обмене. В небольших количествах существуют быстро заменяемые формы либо в частично сформированных кристаллах, либо во внеклеточной жидкости и крови, где их концентрация поддерживается в очень узком диапазоне благодаря эффективному гомеостатическому механизму, включающему всасывание в кишечнике, экскрецию почками и минеральный обмен костной ткани.
Гораздо важнее баланс кальция, чем фосфатов. Транзиторные изменения уровня кальция в крови быстро компенсируется изменениями абсорбции в почечных канальцах. Более стойкое падение концентрации внеклеточного кальция может быть восстановлено за счет усиления костной резорбции. Все эти приспособительные реакции регулируются ПТГ, l,25-(OH)2D и множеством системных и местных факторов роста.
а) Кальций. Кальций необходим для нормального функционирования клеток и таких физиологических процессов, как свертывание крови, нервная проводимость и сокращение мышц. Некомпенсированное падение концентрации ионов кальция (гипокальциемия) может привести к тетании, а чрезмерное повышение (гиперкальциемия) — к замедлению нервно-мышечной передачи.
Основными источниками кальция являются молочные продукты, зеленые овощи и соя (или витаминизированные продукты питания). Рекомендуемая суточная доза для взрослых составляет 800-1000 мг (20-25 ммоль), а в период беременности и лактации, в идеале, ее следует увеличить до 1200 мг. Дети нуждаются в меньшем количестве, примерно 200-400 мг в сутки.
Около 50% получаемого с пищей кальция усваивается в основном в верхнем отделе кишечника, но по большей части выделяется обратно в кишечник, и только около 200 мг (5 ммоль) входит в кровообращение. Нормальная концентрация в плазме и внеклеточной жидкости составляет 2,2-2,6 ммоль/л (8,8-10,4 мг/дл). Большая часть из этого связана с белком, около половины (1,1 ммоль) ионизируется и участвует в метаболизме клеток и регуляции гомеостаза кальция.
Всасыванию кальция в тонком кишечнике способствуют метаболиты витамина D, в частности, 1,25-(ОН)2 витамин D, при этом необходимо также соответствующее соотношение кальция/фосфата. Абсорбция кальция подавляется чрезмерным потреблением фосфора, фосфатов (в основном безалкогольные напитки), оксалатов (содержатся в чае и кофе), солей фитиновой кислоты (мука для чапати, тонких пресных лепешек) и жиров, назначением некоторых лекарственных препаратов (в том числе кортикостероидов) и при нарушении всасывания в кишечнике.
Экскреция составляет 2,5-5 ммоль (100-200 мг) в сутки. Если концентрация ионизированного кальция в плазме падает, происходит выброс ПТГ и вызывается, во-первых, повышенная реабсорбция кальция в почечных канальцах, а, во-вторых, выработка 1,25-(ОН)2 витамина D и усиленная кишечная абсорбция кальция. Если концентрация кальция остается на низком уровне, кальций высвобождается из скелета при помощи повышения костной резорбции, что в свою очередь испытывает косвенное влияние па-ратгормона.
Гипокальциемия. Классическим проявлением гипо-кальциемии является развитие тетании. Пациенты могут жаловаться на потерю чувствительности, парестезию и мышечные спазмы. Более серьезными признаками являются судороги и спазм гортани.
Гиперкальциемия. Клинические проявления зависят от степени гиперкальциемии: небольшое повышение концентрации сывороточного кальция может привести не более чем к общей слабости, полиурии и полидипсии. При уровне в плазме крови от 3 до 3,5 ммоль/л пациенты могут жаловаться на анорексию, тошноту, мышечную слабость и усталость. При тяжелой гиперкальциемии (более 3,5 ммоль/л) имеется множество симптомов, в том числе боль в животе, тошнота, рвота, сильная усталость и депрессия. При длительном течении может развиться мочекаменная болезнь или нефрокальциноз из-за хронической гиперкальциурии; некоторые пациенты жалуются на симптомы со стороны суставов в связи с хондрокальцинозом. Клиническая картина безжалостно, но точно сформулирована в старой присказке: «стонет да охает, камни да кости»
Всегда следует иметь в виду возможные симптомы и признаки основных заболеваний (в подавляющем большинстве это будет гиперпаратиреоз, метастатическое поражение костей, миеломатоз, болезнь Педжета или почечная недостаточность).
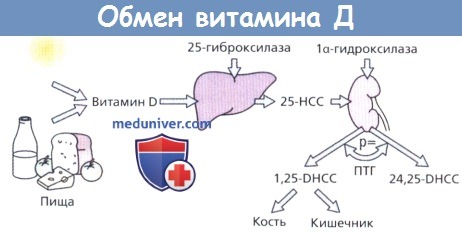
Активные метаболиты витамина D поступают из пищи или при превращении предшественников под воздействием солнечного света.
Неактивный витамин гидроксилируется сначала в печени, затем в почках, формируя активные метаболиты 25-НСС и 1,25-DHCC.
б) Фосфор. Помимо совместной с кальцием роли в составе кристаллов гидроксиапатита в костях, фосфор нужен для многих важных процессов обмена веществ, в том числе переноса энергии и внутриклеточных сигналов клетки. Он широко доступен в пище и всасывается в тонком кишечнике более или менее пропорционально количеству поглощаемых веществ, однако абсорбция уменьшается в присутствии антацидов, таких как гидроокись алюминия, связывающих фосфор в кишечнике. Экскреция фосфатов чрезвычайно эффективна, но 90 % реабсорбируется в проксимальных канальцах почек. Концентрация в плазме почти полностью представленная в виде ионизированного минерального фосфата (Pi), как правило, поддерживается на уровне 0,9-1,3 ммоль/л (2,8-4,0 мг/дл).
Уровень растворимых продуктов кальция и фосфатов всегда поддерживается достаточно постоянным, любое увеличение концентрации одной формы вызывает снижение другой. Основными регуляторами концентрации фосфатов плазмы являются ПТГ и 1,25-(OH)2D. При подъеме Pi выше нормы ответное падение концентрации кальция стимулирует секрецию ПТГ, который в свою очередь подавляет реабсорбцию Pi, что приводит к увеличению экскреции Pi и снижению Pi в плазме. Высокий уровень Pi также приводит к снижению продукции l,25-(OH)2D, что вызывает снижение всасывания фосфора в кишечнике.
В последние годы интерес сосредоточился на других группах гормонов или факторов роста, также вызывающих эффект подавления канальцевой реабсорбции фосфатов независимо от ПТГ. Эти так называемые «фосфотонины» связаны с редкими формами заболеваний с потерей фосфора и опухолями, вызывающими остеомаляцию. Их точная роль в нормальной физиологии все еще исследуется.
в) Магний. Магний играет небольшую, но очень важную роль в минеральном гомеостазе. Его катионы располагаются в клеточном и внеклеточном пространстве тела и обнаруживаются в высокой концентрации в костной ткани. Магний необходим для эффективной секреции и периферического воздействия паратгормона. Таким образом, если гипокальциемия сопровождается гипомагниемией, она не может быть полностью скорректирована до тех пор, пока не будет восстановлена нормальная концентрация магния.
г) Витамин D. Витамин D, его активные метаболиты, главным образом связаны с транспортом и поглощением кальция и (действуя совместно с ПТГ) с ремоделированием костной ткани. Органами-мишенями являются тонкая кишка и кость.
Природный витамин D (холекальциферол) образуется из двух источников: непосредственно из пищи и под опосредованным действием ультрафиолетового света на 7-дегидрохолестерин (провитамин D3) в коже. Для взрослых без адекватного воздействия солнечного света рекомендуемая суточная доза составляет 400-800 ME (10-20 мкг) в сутки, для людей старше 70 лет необходима более высокая доза. В большинстве стран его получают главным образом под воздействием солнечных лучей, а те, которые не имеют такого воздействия, вероятно, страдают от дефицита витамина D, если они не принимают пищевые добавки.
Витамин D сам по себе неактивен. Преобразование в активные метаболиты (действующие как гормоны) происходит вначале в печени с формированием 25-гидроксихолекальциферола [25 OHD], а затем
1,25-дигидрокси-холекальциферол [1,25-ОН)2D] производит дальнейшее гидроксилирование в почках. Фермент, ответственный за это превращение активируется в основном ПТГ, но также и другими гормонами (включая эстроген и пролактин) или аномально низкой концентрацией фосфата. Если концентрация ПТГ падает и фосфаты остаются высокими, 25-OHD преобразуется в альтернативную форму 24,25-(ОН)2D, которая является неактивной. С другой стороны, во время отрицательного баланса кальция продукция переключается на 1,25-(ОН)2D в ответ на секрецию ПТГ; увеличение 1,25-(ОН)2D, помогает восстановить концентрацию сывороточного кальция.
Конечный метаболит 1,25-(ОН)2D (кальцитриол) действует на выстилающие клетки тонкого кишечника, увеличивая всасывание кальция и фосфатов. В кости он способствует лизису остеокластами, но также повышает транспорт кальция через клеточные мембраны и косвенно способствует минерализации остеоида. Некоторые противоэпилептические препараты вмешиваются в обмен витамина D и могут привести к его дефициту.
Концентрация всех активных метаболитов может быть измерена в образцах сыворотки, лучшим показателем уровня витамина D является концентрация формы 25-OHD (в сыворотке l,25-(OH)2D имеет период полураспада всего 15 часов, и поэтому не может служить индикатором). Рекомендованная концентрация в сыворотке составляет 25-30 нг/л, уровень которой часто не достигается у пожилых людей, особенно в северном климате.
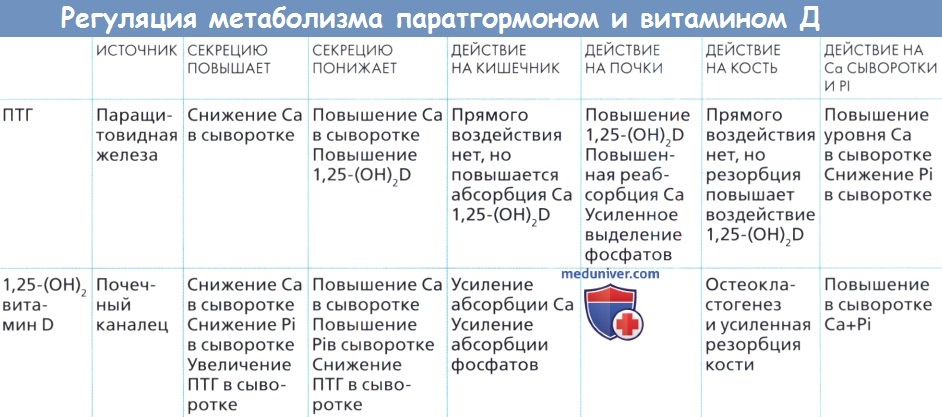
в) Паратгормон. Паратиреоидный гормон (ПТГ) обеспечивает точную регуляцию кальциевого обмена, контролируя концентрацию внеклеточного кальция в критических границах за счет прямого или непрямого воздействия на почечные канальцы, почечную паренхиму, кишечник и кости.
Продукция и секреция стимулируются падением и подавляются (до определенной степени) повышением концентрации в плазме ионизированного кальция. Количество активного конечного фрагмента молекулы ПТГ легко определяется в образце крови.
Действуя в почечных канальцах, ПТГ повышает экскрецию фосфата, ограничивая его реабсорбцию, и сохраняет кальций за счет увеличения реабсорбции. Эти ответы быстро компенсируют любое изменение в плазме ионизированного кальция.
При воздействии на паренхиму почек ПТГ контролирует гидрооксилирование витамина D в метаболит 25-OHD, рост концентрации ПТГ стимулирует превращение в активный метаболит l,25-(OH)2D, а падение ПТГ вызывает образование неактивного метаболита 24, 25-(OH)2D.
В кишечнике ПТГ косвенно стимулирует всасывание кальция, способствуя переходу 25-OHD в 1,25-(ОН)2D в почках.
В кости ПТГ действует совместно с остеокластами, высвобождая кальций и фосфаты в кровь. Это происходит не за счет прямого действия на остеокласты, а за счет стимуляции активности остеобластов, которые повышают экспрессию RANKL и снижают производство ОПГ, что приводит к улучшению дифференциации и созревания остеокластов. Кроме того, вызванное паратгормоном повышение продукции l,25-(OH)2D также имеет эффект стимуляции остеокластогенеза. Конечным результатом этих сложных взаимодействий является продолжительный рост кальция в плазме.
г) Кальцитонин. Кальцитонин, который вырабатывается С-клетками щитовидной железы, является в большей или меньшей степени антагонистом ПТГ: кальцитонин связывается рецепторами остеокластов, подавляет резорбцию костной ткани остеокластами и увеличивает почечную экскрецию кальция. Особенно часто это происходит при усиленном обмене костной ткани, как при болезни Педжета. Секреция кальцитонина стимулируется увеличением концентрации сывороточного кальция свыше 2,25 ммоль/л (9 мг/дл).
д) Половые гормоны. Помимо влияния на рост костей половые гормоны играют важную роль в поддержании костной массы и трабекулярной целостности. Эстрогены активируют и остеобласты, и остеокласты и в настоящее время предполагается что, они работают через систему RANK/RANKL/OPG. Они увеличивают продукцию и активность OPG, вследствие чего прерывается дифференциация остеокластов и костная резорбция. Также эстрогены предположительно увеличивают абсорбцию кальция в кишечнике. Хорошо известно, что потеря костной массы ускоряется после менопаузы и подобные эффекты наблюдаются при аменорее у молодых женщин, которые могут существенно терять костную массу в то время, когда их ровесницы достигают пика костной массы.
Андрогены также сдерживают костную резорбцию, хотя запускающий механизм их действия не совсем ясен. Потеря кости увеличивается после мужского климакса, который происходит на 15-20 лет позднее, чем у женщин.
е) Глюкокортикостероиды. Избыток кортикостероидов вызывает усиленный остеопороз вследствие комбинации факторов: подавление костеобразования остеобластами (наиболее важный эффект), нежелательное воздействие на коллаген, снижение кишечной резорбции кальция и повышение экскреции кальция. RANKL экспрессия остеобластов усиливается, а экспрессия OPG ей противодействует, приводя к увеличению остеокластогенеза и резорбции кости.
ж) Тироксин. Тироксин увеличивает как костеобразование, так и костную резорбцию, но в большей степени последнюю, гипретиреоз сочетается с повышенным костным обменом и остеопорозом.
з) Местные факторы. Глубинные связи остеокластов и остеобластов, восполнение и активация клеток, пространственная организация и транспорт минеральных веществ опосредуются местными факторами, создаваемыми костными клетками, компонентами матрикса и клетками иммунной системы. Некоторые из них служат посредниками между системными и локальными факторами либо между различными клетками, ответственными за ремоделирование кости; другая группа факторов отвечает за костную резорбцию при воспалительных заболеваниях и переломах и также может приводить к деструкции кости и гиперкальциемии при миеломатозе и метастатических поражениях костей.
и) Механическая нагрузка. Хорошо известно, что пространственная ориентация и утолщение трабекул в губчатой кости связаны с распределением силовых линий нагрузки. Об этом говорит закон Вульфа, который гласит, что внутренняя структура и масса скелета адаптируется в ответ на основные внешние силы, вызывающие соответствующие функциональные изменения или деформацию. Физиологическая нагрузка обеспечивается силой тяжести, весом тела, мышечной активностью и пульсацией сосудов. При постоянном изгибающем усилии больше костей будут иметь вогнутую поверхность (поскольку имеется компрессия), а на выпуклых поверхностях кости будут истончаться (находясь под напряжением). Невесомость, длительный постельный режим, отсутствие упражнений, мышечная слабость и иммобилизация конечностей способствуют остеопорозу. Неизвестно, как физические сигналы передаются на клетки кости, но это почти наверняка происходит посредством местных факторов роста.
к) Электрическая стимуляция. При нагрузке или деформации кости возникают небольшие электрические потенциалы — отрицательные на сжимаемой стороне и положительные на растягиваемой (Brighton и McCluskey). Это наблюдение привело к гипотезе, что генерируемые нагрузкой изменения костной массы могут вызываться электрическими сигналами; поэтому было бы логично предполагать, что индуцируемые электрические потенциалы могу влиять на костеобразование и костную резорбцию. Каким образом это происходит точно, остается неизвестным. Потенциалы электромагнитных полей используются при лечении замедленно срастающихся переломов и местного остеопороза пока еще с неоднозначными результатами.
л) Другие факторы окружающей среды. Умеренное повышение температуры или давления кислорода в эксперименте привели к стимуляции костеобразования. Кислотно-щелочное равновесие влияет на костную резорбцию, которая повышается при хроническом ацидозе и снижется при алкалозе.
Богатая фосфором или пирофосфатами пища ведет к замедлению костной резорбции. Аналоги пирофосфатов (бисфосфонаты) применяются при лечении остеопороза, для замедления как резорбции, так и костеобразования.
Фтористые соединения оказывают комплексные воздействия на костную ткань, наиболее важными из которых являются прямая стимуляция активности остеобластов, образование кристаллов фторапатитов (устойчивых к резорбции остеокластами) и отчасти увеличение минеральной плотности, не сопровождающееся увеличением прочности кости; еще один очевидный эффект фтора—повышение реабсорбции кальция и вторичный гиперпаратиреоидоз. Флюороз встречается в виде эндемического заболевания в Индии и в некоторых других частях света из-за повышенного содержания фтора в питьевой воде.
- Вернуться в оглавление раздела "Травматология"
Оглавление темы "Патофизиология кости":
