Значение внешней среды при аутоиммунном заболевании
а) Лекарства и аутоиммунитет. Определенные лекарственные препараты могут вызывать аутоиммунные заболевания с различными клиническими проявлениями. Среди препаратов, индуцирующих аутоиммунитет, наиболее известны прокаинамид и гидралазин, которые могут привести к лекарственной волчанке у небольшого количества пациентов, принимающих эти препараты.
Точные механизмы, которые вызывают прокаинамид- и гидралазин-индуцируемую волчанку, не вполне известны, однако согласно недавним исследованиям, причиной волчанки может быть изменение этими препаратами метилирования ДНК, которое крайне важно для генной регуляции. Прокаинамид и гидралазин могут уменьшать метилирование ДНК в Т-лимфоцитах, что усиливает экспрессию генов, в частности, лимфоцитарного ассоциированного с функцией антигена, который может вызывать аутоиммунитет.
Данные, полученные на мышах, также указывают на то, что прокаинамид может изменить центральную (тимическую) толерантность в Т-клеточной селекции, что позволяет аутореактивным Т-лимфоцитам выходить в периферические ткани.
б) Интерферон-α и аутоиммунитет. Парадоксально, но препараты, которые модулируют иммунную систему, например IFN-α, могут также стимулировать аутоиммунитет. У пациентов, которые получали IFN-α по поводу гепатита С или злокачественных опухолей, развивалась лекарственная волчанка с нефритом и васкулитом, ассоциированным с антинейтрофильными цитоплазматическими антителами. В действительности, потенциальную роль IFN-α в патогенезе волчанки стали рассматривать в конце 1970-х годов, когда было показано повышение уровня IFN-α в сыворотке при волчанке.
Это предположение недавно было пересмотрено несколькими научными группами, которые показали увеличение экспрессии IFN-индуцированных генов в периферических кровяных клетках пациентов с волчанкой при помощи анализа микрочипами.
IFN-α может влиять на врожденную и адаптивную функции иммунных клеток. Он оказывает на Т-лимфоциты антипролиферативный эффект, однако в то же время, он вызывает смену IG изотипов, стимулируя ДК. IFN-α также индуцирует созревание ДК и позволяет моноцитам более эффективно стимулировать Т-лимфоциты, в том числе потенциально аутореактивные. Результаты исследований на мышах также свидетельствует о роли этого цитокина в развитии волчанки. Введение поли(инозин-цитозина) — синтетической двухцепочечной РНК и мощного индуктора IFN-α ускоряет развитие заболевания у склонных к волчанке мышей линии (NZB х NZW) F1.
У склонных к волчанке мышей без рецепторов к IFN типа I, в том числе IFN-α, снижены количество антител anti-dsDNA и активность заболевания.
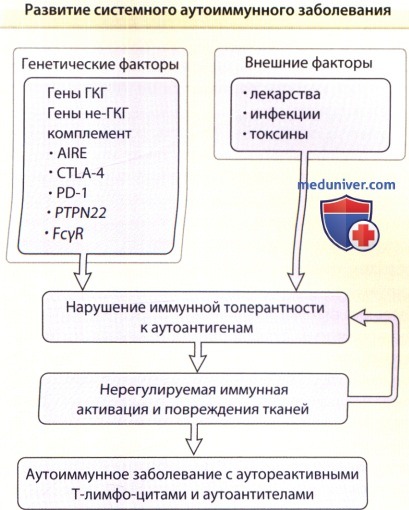
На рисунке показаны потенциальные механизмы инициации системных аутоиммунных заболеваний, в данном случае системной красной волчанки,
в том числе генетические и внешние факторы, которые действуют согласованно, нарушая иммунную толерантность к аутоантигенам.
В последующем наблюдаются нерегулируемая иммунная активация и повреждение тканей, что ведет к развитию аутоиммунного заболевания с аутореактивными Т-лимфоцитами и аутоантителами.
AIRE — autoimmune regulator (аутоиммунный регулятор); CTLA-4 — cytotoxic T-lymphocyte antigen-4 (цитотоксический Т-лимфоцитарный антиген-4; FcgR — рецептор к Fc-фрагменту иммуноглобулина G; ГКГ—главный комплекс гистосовместимости; PD-1 — programmed cell death 1 (ген программируемой смерти клетки-1); РТ-PN22 — proteintyrosinephosphatase 22 (протеинтирозин-фосфатаза 22).
в) Токсины и аутоиммунитет. Химикаты и токсины из внешней среды также могут быть причиной аутоиммунных заболеваний. Возможно, наиболее известный химикат, который связан с развитием системной склеродермии -— кристаллический кремний. Помимо этого состояния, некоторые пациенты с СКВ и РА подвергались воздействию кристаллического кремния, однако эти эпидемиологические данные не предоставляют достаточных доказательств для выводов о причине. С другой стороны, у склонных к волчанке мышей линии (NZB x NZW)F1, подвергавшихся действию кремния, был повышен уровень антинуклеарных антител и снижена выживаемость по сравнению с мышами, не подвергавшимися действию данного вещества.
Точный механизм развития аутоиммунных заболеваний после действия кристаллического кремния неизвестен, однако это вещество может служить адъювантом, усиливающим иммунный ответ за счет повышения продукции провоспалительных цитокинов, например ФНО-α. Несмотря на сообщения о случаях аутоиммунных заболеваний, связанных с действием токсинов, а также о животных с аутоиммунными заболеваниями, усиленными этими веществами, для определения причинно-следственных связей между действием вещества и аутоиммунитетом необходимы дальнейшие исследования.
г) Инфекции и аутоиммунитет. Инфекции считаются возможным этиологическим фактором для аутоиммунитета. Предполагаемые механизмы: 1) высвобождение воспалительных цитокинов, например IFN-a АПК, которые могут модулировать иммунный ответ, 2) продукция перекрестных антител или Т-лимфоцитов, которые могут распознавать как аутоантигены, так и чужеродные антигены (молекулярная мимикрия) и 3) поликлональная активация аутореактивных Т-клеток суперантигенами. Тем не менее эти вероятные механизмы до настоящего времени не доказаны.
Однако множество возбудителей инфекций, включая вирусы и бактерии, связанны с аутоимунными заболеваниями, например, вирус Эпштейна-Барр (ВЭБ) является триггером для развития СКВ. У пациентов с СКВ выше, чем у здоровых людей контрольной группы частота инфекции ВЭБ, что определялось путем измерения анти-ВЭБ антител, у пациентов с СКВ также повышена вирусная нагрузка ВЭБ в периферической крови и изменен Т-клеточный иммунный ответ на ВЭБ. Эти факты позволяют предположить, что иммунный контроль ВЭБ при СКВ изменен, однако неясно, является ли это изменение причиной или следствием СКВ. Вызывает интерес, почему только у небольшой части людей развивается аутоиммунитет, при том, что инфекции, которые могут быть связаны с ВЭБ, часто встречаются в популяции.
Один из вероятных ответов — разнообразие генетического материала, что может привести к различному иммунному ответу на одни и те же инфекционные агенты и возможному развитию аутоиммунных заболеваний.
д) Патогенез повреждения тканей при аутоиммунитете. Механизмы, задействованные в повреждении тканей при аутоиммунных заболеваниях, схожи с теми, которые направлены на уничтожение проникших чужеродных организмов. Аутоантитела могут непосредственно связываться с аутоантигенами, которые экспрессируются на клетках, что приводит к разрушению клеток (обусловленная антителами реакция гиперчувствительности II типа). Аутоиммунная гемолитическая анемия и аутоиммунная тромбоцитопения, которые могут наблюдаться при СКВ,— хорошие примеры разрушения клеток по этому механизму. Некоторые аутоантитела могут связывать аутоантигены и активировать каскад комплемента, что привлекает воспалительные клетки, повреждающие ткани (обусловленная иммунными комплексами реакция гиперчувствительности III типа).
Например, аутоантитела к хроматину и рибонуклеопротеинам, по-видимому, имеют патологическое значение при волчанке. Отложение иммунных комплексов из аутоантител, связанных с соответствующими аутоантигенами в пораженных органах, например почках, приводит к активации комплемента и связыванию с рецепторами к Fc с последующим повреждением тканей. Для развития аутоиммунных заболеваний и появления аутоантител требуются аутореактивные Т-лимфоциты, однако до настоящего времени неясно, участвуют ли аутореактивные Т-лимфоциты непосредственно в повреждении тканей при системных аутоиммунных синдромах, например СКВ. Их роль в непосредственной провокации повреждения тканей при органоспецифичных аутоиммунных синдромах, например СД 1 типа и рассеянном склерозе, изучена значительно лучше.
- Рекомендуем далее ознакомиться со статьей "Классификация кожных проявлений красной волчанки по Gilliam"
Редактор: Искандер Милевски. Дата публикации: 7.2.2019

