Генетика аутоиммунных заболеваний и их наследование
Механизмы аутоиммунных заболеваний - краткий обзор:
- Аутоиммунные заболевания — относительно частые расстройства, и могут классифицироваться на органоспецифичные и системные на основании аутоантигенов, на которые направлены иммунные клетки.
- Несмотря на то что этиология этих заболеваний до сих пор не выяснена окончательно, их рассматривают в контексте нарушения иммунной толерантности к собственным антигенам.
- Механизмы исчезновения иммунной толерантности к аутоантигенам, как генетические, так и обусловленные факторами внешней среды, по-видимому, разнообразны, что приводит к нерегулируемой иммунной активации против аутоантигенов и последующему разрушению тканей.
- При аутоиммунных заболеваниях Т- и В-лимфоциты распознают аутоантигены и преобладают в фенотипе, однако на различных стадиях от инициации аутоиммунного ответа до разрушения тканей задействованы другие иммунные компоненты, в том числе антиген-презентирующие клетки и комплемент.
Аутоиммунные заболевания, в том числе ревматоидный артрит (РА) и системная красная волчанка (СКВ) — относительно частые расстройства. Этиология этих заболеваний до настоящего времени неясна, однако они развиваются на фоне нарушения иммунной толерантности к собственным антигенам. Механизмы исчезновения иммунной толерантности к собственным антигенам, по-видимому, многофакторные, в том числе генетические и средовые, которые действуют совместно и вызывают отличительные признаки заболевания: нерегулируемую иммунную активацию против аутоантигенов и последующее разрушение тканей.
Иммунная активация против аутоантигенов клинически проявляется присутствием антител и аутореактивных Т-клеток. В зависимости от аутоантигенов-мишеней аутоиммунные заболевания можно классифицировать на органспецифичные и системные аутоиммунные процессы.
Например, болезнь Грейвса с аутоантителами к рецептору тиреотропного гормона — типичный пример орган-специфичного аутоиммунного заболевания, как и сахарный диабет (СД) 1 типа с аутоантителами и аутореактивными Т-клетками против компонентов β-клеток поджелудочной железы, тогда как СКВ с характерными аутоантителами к повсеместно распространенным ядерным антигенам — хороший пример системного аутоиммунного заболевания. Несмотря на то что при аутоиммунных процессах в фенотипе преобладают адаптивные иммунные клетки, а именно В-и Т-лимфоциты, распознающие аутоантигены, на различных стадиях от инициации аутоиммунного ответа до разрушения тканей участвуют другие иммунные компоненты, в том числе антиген-презентирующие клетки (АПК) и комплемент.
В статьях на сайте, уделяя особое внимание последним исследованиям, будет обсуждаться влияние этих компонентов на развитие аутоиммунных заболеваний.
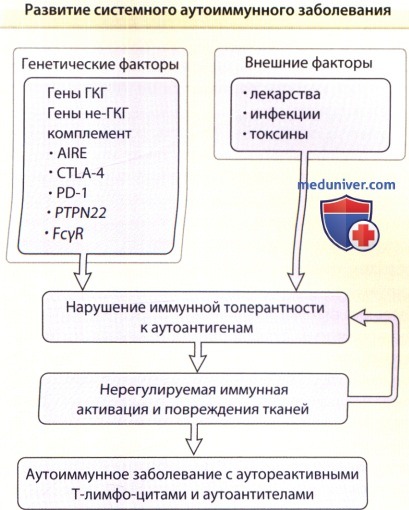
На рисунке показаны потенциальные механизмы инициации системных аутоиммунных заболеваний, в данном случае системной красной волчанки,
в том числе генетические и внешние факторы, которые действуют согласованно, нарушая иммунную толерантность к аутоантигенам.
В последующем наблюдаются нерегулируемая иммунная активация и повреждение тканей, что ведет к развитию аутоиммунного заболевания с аутореактивными Т-лимфоцитами и аутоантителами.
AIRE — autoimmune regulator (аутоиммунный регулятор); CTLA-4 — cytotoxic T-lymphocyte antigen-4 (цитотоксический Т-лимфоцитарный антиген-4; FcgR — рецептор к Fc-фрагменту иммуноглобулина G; ГКГ—главный комплекс гистосовместимости; PD-1 — programmed cell death 1 (ген программируемой смерти клетки-1); РТ-PN22 — proteintyrosinephosphatase 22 (протеинтирозин-фосфатаза 22).
а) Аутоиммунные заболевания полигенны. Аутоиммунные заболевания полигенны и задействуют как гены главного комплекса гистосовместимости (ГКГ), так и не относящиеся к нему гены. Тем не менее конкордантность аутоиммунных заболеваний у монозиготных близнецов составляет не 100%, а от 10 до 50%, в том числе для РА и СКВ, что свидетельствует о значимой роли негенетических факторов.
При этом генетическое влияние выражено. Вклад аллелей ГКГ в развитие аутоиммунного процесса известен уже 30 лет. У некоторых пациентов с РА наблюдается повышенная частота встречаемости лейкоцитарного антигена человека HLA-DR4. При помощи более сложных молекулярных методов была типирована последовательность локусов аллелей, кодирующих HLA, и было показано, что ген HLA-DRB1 высоко полиморфен, и этот полиморфизм может влиять на связывание пептидов с молекулами HLA и контакты между Т-клеточным рецептором (TCR) и молекулой HLA.
Таким образом, связь между аутоиммунными заболеваниями и определенными молекулами HLA можно объяснить при помощи модели, в которой подверженность заболеванию определяется различием в способности аллелей HLA презентировать аутоантигенные пептиды аутореактивным Т-лимфоцитам. Тем не менее, генетический вклад ГКГ в предрасположенность к развитию аутоиммунных заболеваний более значителен. Это утверждение иллюстрирует последнее исследование генотипирования панелей 1472 одиночных нуклеотидных полиморфизмов (SNPs) на протяжении 3,44 мегабаз (Mb) хорошо известного участка ГКГ в 10576 образцах ДНК пациентов с аутоиммунными заболеваниями, а именно СКВ, РА, рассеянным склерозом, и в группе контроля.
Результаты исследования показали наличие множественных аллелей риска в участках ГКГ I, II и III классов при вышеперечисленных аутоиммунных заболеваниях.
б) Связь с аутоиммунными заболеваниями генов, не относящихся к главному комплексу гистосовместимости. В настоящее время с помощью полногеномного сканирования (GWA), мощного инструмента определения новых генов, участвующих в аутоиммунитете, точно установлена связь между генами, не относящимися к ГКГ, и аутоиммунными заболеваниями. Это гены, участвующие в устранении аутоантигенов, апоптозе, клеточных сигналах, продукции цитокинов и экспрессии ко-стимулирующих молекул. Например, для нормального устранения иммунных комплексов требуются компоненты комплемента, и при СКВ с отложениями иммунных комплексов в пораженных органах, например почках, повышена частота гомозиготного дефекта С4.
в) Аутоиммунные регуляторы. Не так давно, в качестве гена-кандидата, ответственного за развитие аутоиммунных заболеваний, был определен ген, называемый «аутоиммунный регулятор» (AIRE). AIRE-фактор транскрипции, который регулирует эктопическую экспрессию белков, в норме экспрессируемых в периферических тканях, тимусе, обеспечивая экспрессию этих белков в тимусе и последующую негативную селекцию аутореактивных тимоцитов перед их миграцией как зрелых Т-клеток во вторичные лимфоидные органы, в частности, селезенку и лимфоузлы. Нарушение тимической экспрессии AIRE может вести к повышенному образованию аутореактивных Т-лимфоцитов по причине нарушения их негативной селекции.
В действительности, при мутациях гена AIRE развивается синдром, называемый аутоиммунная полиэндокринопатия-кандидоз-синдром эктодермальной дистрофии, или аутоиммунный полигландулярный синдром I (APS-1), который характеризуется хроническим кандидозом, гипопаратиреозом и болезнью Аддисона. Помимо этого, при данном состоянии часто наблюдаются другие орган-специфические аутоиммунные заболевания, в том числе сахарный диабет первого типа (СД 1), аутоиммунные заболевания щитовидной железы, недостаточность гонад, витилиго, гнездная алопеция, дистрофия ногтей и эмали зубов, а также пернициозная анемия.
г) Цитотоксический Т-лимфоцитарный антиген-4. У носителей определенного варианта генов, влияющих на активацию Т-лимфоцитов, выявляется повышенная частота аутоиммунных заболеваний. Эти гены — цитотоксический Т-лимфоцитарный антиген-4 (CTLA-4) и ген белковой тирозинфосфатазы 22 (PTPN22). CTLA-4 — основная иммунорегуляторная молекула, подавляющая активацию Т-лимфоцитов. Она экспрессируется на Т-лимфоцитах при стимуляции TCR антигеном на антиген-презентирующих клетках (АПК) и конкурирует с CD28 — молекулой положительной ко-стимуляции также на Т-лимфоцитах за связывание с CD80 и CD86, которые экспрессируются на АПК. В отличие от связывания CD80 и CD86 с CD28, взаимодействие этих молекул с CTLA-4 ингибирует активацию Т-лимфоцитов.
Была показана связь СКВ и РА с полиморфизмом одного нуклеотида (SNP) в промоторе и кодирующем участке CTLA-4. Эти сайты полиморфизма — позиция -1722 промотора CTLA-4 и позиция +49 экзона-1, однако функциональные последствия этих генных полиморфизмов в настоящее время неизвестны.
Полиморфизмы CTLA-4 также связаны с аутоиммунными эндокринопатиями: например, при SNP в CTLA-4CT60 G/G наблюдается снижение содержания продукта альтернативного сплайсинга CTLA-4 — растворимой формы CTLA-4, что связано с повышенной склонностью к болезни Грейвса, аутоиммунному гипотиреозу и СД1. Этот факт свидетельствует о возможной функциональной роли полиморфизмов CTLA-4 при аутоиммунных заболеваниях.
д) Ген программируемой смерти клетки 1. Так же как CTLA-4, белок программируемой смерти клетки 1 (PD-1) экспрессируется на Т-лимфоцитах и при активации обеспечивает ингибирующий сигнал. Эта молекула также экспрессируется на других иммунных клетках, в том числе В-лимфоцитах и миелоидных клетках. PD-1 кодируется геном PDCD1 и SNP в четвертом интроне связан с аутоиммунными заболеваниями, в том числе СКВ и РА. Интересно, что этот связанный с заболеваниями SNP нарушает связывание гематопоэтического фактора транскрипции 1 (RUNX1), что предположительно ведет к нарушению экспрессии гена PDCD1 и впоследствии к неконтролируемой активации Т-лимфоцитов. Связь генетических полиморфизмов CTLA-4 и PD-1 — молекул, регулирующих активацию Т-лимфоцитов, с аутоиммунными заболеваниями подтверждает мнение о том, что критическая точка для развития аутоиммунитета — регуляция активации Т-лимфоцитов этими ко-стимулирующими молекулами.
е) Белковая тирозинфосфатаза 22. Ген, кодирующий белковую тирозинфосфатазу 22 (PTPN22) — еще один недавно обнаруженный ген, связанный с аутоиммунными заболеваниями. Было обнаружено, что вариант гена PTPN22 с триптофаном в кодоне 620 (620W) вместо аргинина (дикий тип) связан с повышенным риском РА, СКВ, СД 1 и болезнью Грейвса. По-видимому, данная мутация имеет функциональные последствия, поскольку ген PTPN22 кодирует лимфоидную тирозинфосфатазу, которая модулирует активацию Lck и других киназ, участвующих в TCR сигнальном пути.
В действительности, аллель 620WPTPN22, по-видимому, может усиливать ингибирование активации TCR, уменьшая активацию Lck. Таким образом, еще необходимо выяснить, как данный аллель способствует развитию аутоиммунитета.
ж) Сигнальный путь рецептор фактора некроза опухоли. В последнее время установлено, что множество генов, кодирующих молекулы, участвующие в сигнальном пути рецепторов фактора некроза опухоли (ФНО) имеют отношение к аутоиммунитету. Среди них лучше всего изучен TNFAIP3, кодирующий индуцируемый белок ФНО А20, который является отрицательным регулятором индуцируемых ФНО NF-kB сигнальных путей. Ген, кодирующий белок 1, взаимодействующий с TNFAIP3 (TNIP1), ассоциирован с псориазом и СКВ. Также сообщалось о связи гена TRAF1 (фактор 1, ассоциированный с рецептором ФНО) с РА.
з) Рецепторы цитокинов. Полиморфизм некоторых рецепторов цитокинов связан с аутоиммунитетом. Рецепторный комплекс ИЛ-23 состоит из ИЛ-23R и ИЛ-12Rβ1, последний, в свою очередь, состоит из ИЛ-12Rβ1 и ИЛ-12Rβ2 субъединиц. Ген рецептора ИЛ-23R ассоциирован с воспалительными заболеваниями кишечника и псориазом. Этот факт представляет интерес, учитывая, что ИЛ-23 вовлечен в регуляцию созревания Т-хелперов 17 (Тh17), которые продуцируют активные провоспалительные цитокины ИЛ 17. Более того, ИЛ-17 обнаруживается в очагах псориаза на коже. Таким же образом обнаружено, что ген ИЛ 12В, кодирующий ИЛ-12 (р40 субъединица ИЛ-12), связан с псориазом.
и) Рецепторы к Fc-фрагменту иммуноглобулина G. Помимо генов, экспрессируемых Т-лимфоцитами, с аутоиммунитетом, по-видимому, связаны гены, задействованные в гуморальном иммунном ответе. Рецепторы к Fc-фрагменту иммуноглобулина G (IgG) (FcgyR: FC-GRIA, FCGRIB, FCGRIC, FCGRIIA, FCGRIIB, FCGRIIC, FC-GRIIIA, и FCGRIIIB. Связывание всех рецепторов Fcg R, за исключением FcRIIb, c IgG вызывает широкий спектр активирующих клеточных ответов, в том числе фагоцитоз, цитолиз, продукцию цитокинов и дегрануляцию, что ведет к воспалению. Напротив, Fcg Rllb в норме служит ингибирующим рецептором, который подавляет эффекторную функцию клеток. Сообщают о повышенной частоте некоторых вариантов генов FCGR у людей с аутоиммунными заболеваниями, в том числе СКВ и РА. Fcg Rlla с аргинином является фактором предрасположенности к СКВ в некоторых этнических группах.
Сходным образом, вариант Fcg RIIa с фенилаланином в положении 158 может быть фактором предрасположенности к СКВ и РА. Помимо этого, при СКВ обнаружены генетические полиморфизмы ингибирующего Fcg RIIb. Наиболее известный из подобных полиморфизмов — замена изолейцина в положении 232 (187 от N-конца зрелого белка) на треонин. Указанный генотип чаще всего обнаруживается у пациентов с СКВ. Биологическое влияние этого изменения на развитие СКВ неясно, однако при волчанке у мышей ингибирующее действие рецепторов Fcg R необходимо для подавления аутоиммунитета.
В целом генетические исследования генов как относящихся, так и не относящихся к ГКГ подтверждает, что у некоторых пациентов с аутоиммунными заболеваниями повышен генетический риск развития аутоиммунных расстройств в результате генетических изменений, нарушающих функции иммунных клеток. Тем не менее эти изменения не всегда наблюдаются у пациентов с аутоиммунными заболеваниями, и в генетической предрасположенности часто встречаются этнические различия. Эти факты указывают на то, что аутоиммунные заболевания полигенны, и в их развитии участвуют факторы окружающей среды.
- Рекомендуем далее ознакомиться со статьей "Толерантность при аутоиммунных заболеваниях"
Редактор: Искандер Милевски. Дата публикации: 7.2.2019

