Саркома Капоши - этиология, патогенез, гистогенез
Саркома Капоши - краткий обзор:
- Системная многоочаговая опухоль эндотелиального происхождения с характерными для каждой стадии гистопатологическими признаками.
- Описано четыре клинических варианта:
1. Классическая саркома Капоши (СК) — у пожилых мужчин, начинается как локализованная форма, медленно прогрессирует.
2. Эндемическая африканская саркома Капоши (СК) — наиболее частое новообразование в некоторых странах центральной Африки; включает в себя быстропрогрессирующий лимфаденопатический вариант.
3. Саркома Капоши (СК)-ассоциированная с иммуносупрессивной терапией — чаще всего встречается после трансплантации органов.
4. Саркома Капоши (СК), ассоциированная со СПИД — быстро прогрессирующая форма заболевания у ВИЧ-позитивных пациентов, которая характеризуется ранним формированием внекожных очагов.
- Развитие саркомы Капоши (СК) непременно связано с инфекцией вирусом герпеса человека 8 типа.
- Несмотря на то, что патогенез болезни обусловлен действием вируса, саркома Капоши (СК) хорошо отвечает на химиотерапию и лучевую терапию.
В 1872 г. австро-венгерский дерматолог Мориц Капоши описал пятерых пациентов с множественными кожными и внекожными новообразованиями, поражающими в основном лиц старшего возраста. Заболевание, изначально описанное как идиопатическая множественная пигментная саркома, позже получило название по имени своего первооткрывателя — саркома Капоши (СК). Различные варианты этой опухоли имеют своеобразные эпидемиологические характеристики и клиническое течение, но обладают сопоставимыми гистопатологическими признаками.
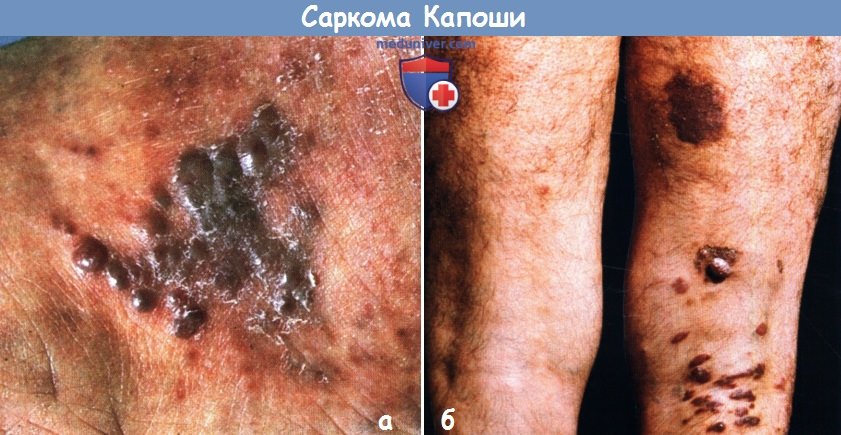
б - Опухолевые узлы более запущенного случая классической саркомы Капоши (средиземноморский вариант) с тяжелым поражением конечностей.
а) Этиология и патогенез. HHV-8 и саркома Капоши (СК). Эпидемиологические данные и результаты электронной микроскопии, полученные за несколько десятилетий, позволили предположить вовлечение в этиологию саркомы Капоши инфекционного агента. Эта гипотеза была укреплена в 1994 г., когда Chang и соавт. обнаружили ДНК неизвестного вируса в элементах саркомы Капоши. Это открытие привело к клонированию, выделению и описанию нового вируса герпеса человека, который в настоящее время рассматривается как вирус герпеса, ассоциированный с саркомой Капоши (KSHV) или, иначе, вирус герпеса человека 8 типа (HHV-8).
HHV-8 относится к подсемейству γ-Herpesviridae, роду Rhadinovirus, Его геном с ДНК размером 165 kb был полностью секвенирован и, как было показано, содержит почти 90 открытых рамок считывания. Многие из регуляторных генов HHV-8 гомологичны генам других радиновирусов, а некоторые гомологичны генам человека, вовлеченным в регуляцию процессов апоптоза, клеточной пролиферации и ангиогенеза. Как и при других герпес-вирусах, экспрессия гена HHV-8 тщательно контролируется и связана либо с вирусной латентностью, представленной такими антигенами, как латентный ядерный антиген LANA-1, v-циклин и v-FLIP-онкопротеин, либо с лизирующей вирусной репликацией [вирусные рецепторы (vGPCR), вирусный интерлейкин 6 (vIL 6) и вирусный белок (v-bcl-2)].
Было показано, что некоторые продукты репликации генов, как литического, так и латентного циклов жизнедеятельности вируса, трансформируют клетки в условиях in vitro и на животных моделях in vivo.
Таким образом, общепринятым является факт, что ННV-8 представляет собой трансформирующий герпесвирус и, что этот факт играет непосредственную роль в развитии саркомы Капоши.
Вирус HHV-8 в условиях как in vivo, так и in vitro обладает наибольшей тропностью к сосудистым и лимфатическим эндотелиальным клеткам, а также к различным видам гемопоэтических клеток. Широко экспрессируемая 12-трансмембранная легкая цепь транспортной системы обмена цистин/глутамат недавно была предложена в качестве специфического рецептора вируса герпеса 8 типа. Последние представляют особый интерес, так как в отличие от первых экспрессируются активированными В-клетками, которые играют важную роль в качестве хозяев ВГЧ-8 in vivo.
Пути передачи вируса HHV-8 неизвестны. Значительное количество случаев саркомы Капоши среди мужчин гомо- и бисексуальной ориентации, а также взаимосвязь развития опухоли с определенными типами полового акта очень рано позволили предположить половой путь передачи вируса. В более поздних эпидемиологических исследованиях половой акт, как механизм передачи HHV-8, был подтвержден, и было показано, что риск заражения повышается с увеличением числа половых партнеров и использованием суррогатных видов полового акта — орально-генитального и орально-анального.
Напротив, в областях, где вирус широко распространен, таких как Средиземноморье и Африка, существуют надежные доказательства того, что передача неполовым путем играет главную роль среди членов семьи. Ротоглотка является местом наиболее выраженной репликации вируса и большое число копий вируса HHV-8 находится в слюне. На основе этих открытий неполовой механизм передачи вируса через слюну является общепризнанным, как играющий наиболее важную роль в заражении детей в эндемических областях. Вертикальный путь передачи от матери к плоду во время беременности или родов, по-видимому, не имеет большого значения для распространения вируса. Медицинским работникам важно помнить, что вирус HHV-8 также может передаваться через кровь и продукты крови, точно так же, как и через донорские органы после трансплантаций.
Вирус HHV-8 присутствует во при всех вариантах саркомы Капоши, получены многочисленные данные о причинной взаимосвязи между инфицированием HHV и развитием этой опухоли. Среди наиболее значимых аргументов в пользу роли HHV-8 в патогенезе саркомы Капоши следующие: (1) вирусный геном HHV-8 обнаруживается во всех элементах саркомы Капоши при всех стадиях заболевания, в независимости от клинического варианта;5,6,21,22 (2) в пределах патологических элементов саркомы Капоши вирус HHV-8 присутствует в латентной форме практически во всех опухолевых клетках; и (3) опухолевые клетки саркомы Капоши демонстрируют моноклональную интеграцию вирусной ДНК. Более того, распространение HHV-8-инфекции полностью соответствует распространенности саркомы Капоши: в областях с низкой частотой встречаемости саркомы Капоши, таких как США и страны Северной Европы, HHV-8-инфекция является очень редкой (менее 0,1%).
И наоборот, в областях с высокой частотой саркомы Капоши, таких как Южная Италия, как сообщалось, распространение HHV-8 намного выше и достигает 20%. Как ожидалось, наибольшая частота встречаемости HHV-8 была выявлена в странах центральной Африки в регионах, известных как очаги африканской эндемической саркомы Капоши. В этом регионе серологическое обнаружение вируса у взрослых варьирует от 22 до 71%. Также, в развитых странах у пациентов, инфицированных вирусом иммунодефицита человека (ВИЧ)-1, частота встречаемости HHV-8 наиболее высока среди мужчин гомо- и бисексуальной ориентации и отражает распространение саркомы Капоши в данной группе риска.
Период от инфицирования HHV-8 до развития саркомы Капоши зависит от клинического варианта опухоли. Иммуносупрессия/дисрегуляция имеет важное усугубляющее воздействие и ведет к манифестации болезни у пациентов, перенесших трансплантацию органов, в течение 1-2 лет, а у пациентов, инфицированных ВИЧ в течение 5-10 лет от момента инфицирования. При классическом варианте саркомы Капоши этот период намного более продолжительный, однако способствующих факторов, как внутренних, так и внешних пока не установлено.
Помимо саркомы Капоши, вирус HHV-8 был вовлечен в патогенез лимфомы с плевральным выпотом, редкого В-клеточного новообразования, наблюдаемого в первую очередь у пациентов с синдромом приобретенного иммунодефицита (СПИД), и мультицентрической болезни Кастельмана (МБК). В первом случае вирус HHV-8 присутствует постоянно и является диагностически значимым, а в последнем — обнаруживается у большинства (боле 95%) ВИЧ-инфицированных пациентов с мультицентрической болезнью Кастельмана, но лишь приблизительно у 40% ВИЧ-негативных пациентов с МБК. В прошлом болезнь Кастельмана была также связана с классической саркомой Капоши.
б) Гистогенез. Гистогенез опухолевых клеток саркомы Капоши (например, клеток, выстилающих неравномерные сосудоподобные участки ранних и ангиоматозных поражений, и клеток, составляющих переплетающиеся пучки солидных опухолей) был предметом активного исследования в течение двух последних десятилетий. Иммунофенотип этих клеток (например, vWF+/-, PAL-E-, CD31+, CD34+, VEGFR3+) характеризует их как часть линии лимфатической эндотелиальной дифференцировки. Последние данные, показывающие, что вирус HHV-8 значительно лучше реплицируется в лимфатических, а не в кровеносных сосудистых эндотелиальных клетках, являются еще одним аргументом в пользу этого предположения.
Так или иначе, открытие того факта, что инфицирование эндотелиальных клеток кровеносных сосудов вирусом HHV-8 приводит к фенотипическому переключению на эндотелиальные клетки лимфатических сосудов, допускает вероятность того, что незрелые ангиобласты, либо находящиеся в коже, либо циркулирующие в крови и способные к дифференцировке на обе линии эндотелиальных клеток, являются первоначальными предшественниками опухолевых клеток саркомы Капоши.
Вопрос о том, на самом ли деле саркома Капоши обратимое пролиферативное заболевание или истинное злокачественное новообразование, является противоречивым. Исследования модели метилирования гена рецептора андрогена человека показали, что могут выявляться нарущения как в клональной, так и поликлональной пролиферации. Аналогичным образом и при исследовании последовательностей концевых повторов HHV-8 была показана как моно-, так и олигоклональность вируса в очагах саркомы Капоши. В сумме полученные данные указывают, что саркома Капоши начинается как поликлональное заболевание, т.е. как реактивный процесс, а по мере прогрессирования может трансформироваться в моноклональную опухоль.
- Рекомендуем далее ознакомиться со статьей "Клиника и варианты саркомы Капоши (СК)"
Редактор: Искандер Милевски. Дата публикации: 16.11.2018

