Онкоген RAS и его характеристика
Гены RAS, представленные в геноме человека тремя видами (HRAS, KRAS, NRAS), первоначально были обнаружены в трансформирующих ретровирусах. Точечные мутации генов семейства RAS относятся к наиболее часто встречающимся изменениям протоонкогенов в опухолях человека. Около 1520% всех опухолей человека содержат мутантный белок RAS.
Частота обнаружения мутаций в разных опухолях варьирует, но в некоторых видах злокачественных опухолей оначрезвычайно высока. Например, точечные мутации RAS выявляются в 90% случаев аденокарцином поджелудочной железы и холангиокарцином, в « 50% случаев рака толстой кишки, эндометрия, щитовидной железы, а также в 30% аденокарцином легкого и миелоидной лейкемии.
В целом для карцином характерны мутации KRAS, для опухолей мочевого пузыря — HRAS, а для опухолей системы кроветворения — NRAS. Мутации RAS встречаются в ряде других опухолей, например при раке молочной железы и раке шейки матки, но редко.
RAS выполняет важную роль в передаче сигнала роста в каскаде реакций, исходящих от рецепторов факторов роста и приводящих к делению клеток. Например, прекращение функционирования RAS приводит к блокированию пролиферативного ответа при воздействии EGF, PDGF и CSF-1.
Нормальные белки RAS прикрепляются на цитоплазматической поверхности плазматической мембраны, а также к эндоплазматическому ретикулуму и аппарату Гольджи. Белки RAS могут активироваться факторами роста, связывающимися с рецепторами на плазматической мембране.
RAS является членом семейства маленьких G-белков, связывающих гуанозиннуклеотиды (гуанозинтрифосфат [ГТФ] и гуанозиндифосфат [ГДФ]) подобно тому, как делает большой тримолекулярный G-белок. Нормальные белки RAS переходят из активного состояния, передающего сигнал, в неактивное. Белки RAS неактивны, когда связаны с ГДФ.
Стимуляция клеток факторами роста приводит к замене ГДФ на ГТФ и последующим конформационным изменениям RAS, обусловливающим его активацию. Активированный RAS, в свою очередь, стимулирует расположенные далее регуляторы пролиферации, например каскад МАРК, передающий пролиферативный сигнал в ядро клетки.
Упорядоченное функционирование белка RAS зависит от двух реакций:
(1) замены нуклеотидов (ГТФ на ГДФ), что приводит к активации белка RAS;
(2) гидролиза ГТФ, при котором происходит превращение ГТФ-связанного активного белка RAS в ГДФ-связанный неактивный белок RAS.
Оба эти процесса регулируются извне другими белками. Удаление ГДФ и замена его на ГТФ при активации RAS катализируется семейством гуаниннуклеотид-рилизинг белков. Напротив, активность ГТФазы сильно стимулируется семейством белков-активаторов гуанозинтрифосфатазы (GAP). Эти широко распространенные белки связываются с RAS и увеличивают его активность более чем в 1000 раз, что завершает передачу сигнала. Таким образом, GAP выступает в качестве «тормозов» и предотвращает безудержную активацию RAS.
В опухолевых клетках определены несколько точечных мутаций гена RAS. Обычно вовлечены локусы в ГТФ-связывающей области или генов ферментов, участвующих в гидролизе ГТФ, в результате значительно снижается ГТФазная активность белка RAS. Мутантный RAS, таким образом, находится в активированной ГТФ-связанной форме и постоянно стимулирует клетку к пролиферации.
Если следовать данному сценарию дальше, то последствия, аналогичные мутациям в белке RAS, должны наблюдаться и при мутациях в генах GAP, измененные белки которых не в состоянии возвращать онкопротеин RAS в неактивное состояние. Действительно, блокирующая мутация нейрофибромина 1 ассоциируется с семейным нейрофиброматозом типа I.
Другие участники сигнального пути RAS/RAF/МАРК в опухолевых клетках также могут быть изменены, что в результате приводит к таким же фенотипическим изменениям. Так, мутации BRAF, одного из членов семейства RAF, обнаружены более чем в 60% случаев меланомы и более чем в 80% доброкачественных невусов.
На основе полученных данных можно высказать предположение, что дисрегуляция сигнального пути RAS/RAF/MAPK может быть одним из инициальных событий при развитии меланомы, хотя только этого вряд ли достаточно для развития злокачественной опухоли. В самом деле, изолированные мутации BRAF ведут только к онкоген-индуцированному старению, вызывая развитие скорее доброкачественных невусов, нежели меланом.
Таким образом, онкоген-индуцированное старение является барьером для канцерогенеза, который может быть преодолен за счет мутаций и блокирования ключевых защитных механизмов, как те, которые регулирует ген р53.
Поскольку RAS в злокачественных опухолях человека часто мутирует, было предпринято множество попыток создать анти-RAS методы таргетной терапии. К сожалению, не была доказана клиническая эффективность ни одного из этих методов.
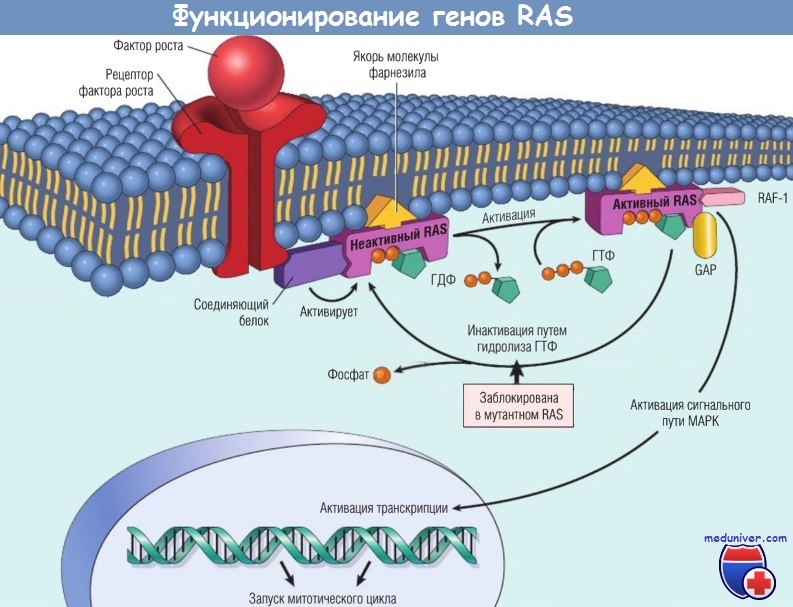
Активированный RAS вовлекает онкопротеин RAF и стимулирует сигнальный путь МАРК, по которому сигнал роста передается в ядро.
Мутантный белок RAS постоянно находится в активированном состоянии, т.к. не способен гидролизовать ГТФ, что приводит к непрерывной стимуляции деления клеток без какого бы то ни было внешнего триггера.
Прикрепление RAS к мембране клетки частью молекулы фарнезила является существенным моментом для его функционирования.
GAP — белки-активаторы гуанозинтрифосфатазы; МАРК — митоген-активируемая протеинкиназа; ГДФ — гуанозиндифосфат; ГТФ — гуанозинтрифосфат.
- Рекомендуем ознакомиться со следующей статьей "Изменения нерецепторных тирозинкиназ при развитии рака"
Оглавление темы "Патофизиология онкологических заболеваний":- Онкоген RAS и его характеристика
- Изменения нерецепторных тирозинкиназ при развитии рака
- Протоонкоген MYC в развитии опухолей
- Циклины и циклин-зависимые киназы в развитии опухолей
- Гены-супрессоры опухоли и их характеристика
- Ген RB и его значение в развитии опухоли
- Ген p53 и его значение в развитии опухоли
- Ген APC и его значение в развитии опухоли
- Ген INK4a/AKF (локус CDKN2A) и его значение в развитии опухоли
- Сигнальный путь TGF-b и его значение в развитии опухоли

