Канцерогенез. Генетические аспекты канцерогенеза. Протоонкогены. Гены-супрессоры.
Одна из наиболее распространенных групп мультифакториальных заболеваний — злокачественные новообразования. Их распространенность у детей составляет 1:160, а среди лиц среднего и старшего возраста этот показатель увеличивается до 1:10.
Генетические аспекты этиологии и патогенеза злокачественных новообразований у человека изучаются очень давно. Первым предположил роль наследственности, как одного из механизмов канцерогенеза, французский хирург Брока, описавший в 1869 г. родословную семьи своей жены, где из 24 женщин 10 умерли от рака молочной железы.
Как и для всех мультифакториальных заболеваний реализация механизмов канцерогенеза обеспечивается совместным действием целого ряда генетических и средовых факторов.
Основными генетическими механизмами, запускающими процесс канцерогенеза, у человека являются мутации генов двух групп семейств, контролирующих процессы жизнеобеспечения клетки: протоонкогенов и антионкогенов (генов-супрессоров опухолевого роста).
Протоонкогены представляют собой группу семейств генов, которые играют ключевую роль в пролиферации и дифференцировке клеток, функционировании клеточных рецепторов, репарации ДНК и формировании ответа на внешние регуляторные сигналы. Продукты этих генов в норме регулируют многостадийный процесс сигнальной трансдукции. Передача сигналов опосредована тремя механизмами:
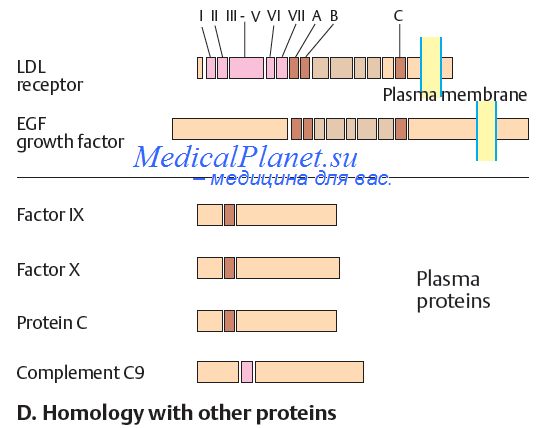
1) фосфорилированием серина, треонина и тирозина в остатках белков путем отщепления фосфатной группы от АТР, в результате чего изменяется конфигурация белка-фермента и его активность;
2) регуляцией активности GTPазы, осуществляющей GDP/GTP-преврашенис и выполняющей роль молекулярного медиатора мембрано-ассоциированных тирозин-киназы и серин-треонин-киназы;
3) регуляцией репликации ДНК, экспрессии ядерных генов и процессов агюптоза. Гены-супрессоры опухолевого роста в норме отвечают за подавление клеточной пролиферации на определенных стадиях онтогенеза, т.е. регулируют (тормозят) экспрессию протоонкогенов.
Трансформация нормальной клетки в опухолевую представляет собой длинную цепь событий, инициируемых каскадом мутаций в протоонкогенах и генах-супрессорах. Механизмы канцерогенеза, запускаемые мутациями в генах этих двух групп семейств, несколько различаются.
Мутации в протоонкогенах, обусловливающие их трансформацию в так называемые клеточные (целлюлярные) онкогены (с-опс), могут 1) затрагивать структурную часть гена и приводить к изменению его продукта или 2) повышать уровень экспрессии гена за счет хромосомных перестроек и/или мутаций в регуляторной части (в области промотора или энхансера) или амплификации (увеличения числа копий).
Мутации в структурной части гена - это, как правило, точковые мутации, меняющие конфигурацию белка, в результате чего активируется аутофосфорилирование, увеличивается активность фермента и, следовательно, усиливается клеточный рост. Эти мутации аутосомно-доминантные, так как для злокачественной трансформации клетки не нужен второй сопутствующий онкоген. Такие мутации описаны для семейства протоонкогенов ras: так в гене c-Ha-ras в кодоне, соответствующем 12-й аминокислоте белка p21ras, замена G -> Т (в белке - замена глицина на валин) приводит к развитию карциномы мочевого пузыря; точковая мутация в гене c-N-ras, приводящая к замене лизина на глицин в 61-м положении белка р21ras, обусловливает развитие меланом и ряда карцином; активация протонкогена c-Ki-ras2 вследствие двух различных точковых мутаций в одном и том же кодоне, соответствующем 12-й аминокислоте белка р21 ras (замена глицина на валин или цистеин), приводит к развитию острого миелоидного лейкоза или карциномы щитовидной железы, соответственно. Точковые мутации выявлены и в гене erbA: замена ряда аминокислот в аминотерминальных положениях на валин в белке P75erb приводит к развитию эритробластозов.
При анализе кариотипа больных с различными типами опухолей часто выявляются транслокации, делеции и инсерции. В результате этих хромосомных перестроек протоонкоген может попасть в зону действия активного промотора, при этом транскрипция протоонкогена увеличится. Так протоонкогены c-mos, с-тус и с-аbl активируются вследствие транслокаций t(8;21), t(8;14), t(9;22), соответственно, что приводит к развитию следующих опухолей: острого миелоидного лейкоза, лимфомы Беркитта, хронического миелоидного лейкоза. Делеции 11р рядом с областью расположения гена c-ras - Пр13, могут привести к развитию аниридии или опухоли Вилмса. Результатом транслокации может быть и амплификация гена (см. ниже), например, амплификация протонкогена аЫ при хроническом миелолейкозе.
Предполагается, что инсерции в регуляторные участки гена представлены преимущественно последовательностями генома некоторых ДНК-содержащих вирусов или провирусной ДНК ретровирусов (РНК-содержащие). Встраивание в определенные участки генома регуляторных ДНК-последовательностей ретровирусов и/или активация провирусами промоторов клеточных онкогенов может привести к резкому усилению экспрессии протоонкогенов и развитию опухоли.
Возникновение опухолей, ассоциированных с ДНК-содержащими вирусами, обусловлено тем, что вирусная ДНК становится частью клеточного генома и вместе с ним передается дочерним клеткам. При этом репликация и экспрессия вирусной ДНК частично или полностью регулируются клеточными механизмами, в зависимости от степени интеграции генома вируса. Механизм регуляции экспрессии интегрированного генома вируса зависит от вида клеток. Некоторые типы ДНК-вирусов и обусловленные ими опухоли представлены в таблице.
У большинства протоонкогенов человека выявлено некоторое сходство с нуклеотидной последовательностью дополнительных генов ретровирусов, обладающих онкогенным эффектом при внедрении в клетку-хозяина (вирусные онкогены - v-onc). Предполагают, что онкогены ретровирусов имеют клеточную природу и возникли вследствие рекомбинации провирусной ДНК с генами, регулировавшими процессы деления, дифференцировки и метаболизма клетки. Становясь вирусными (лишенными интронов), эти гены «уходят» от клеточного контроля регуляции экспрессии, постоянно функционируют и амплифицируются. Следствием этих событий является их повышенная экспрессия, приводящая к трансформации нормальной клетки в опухолевую. Гомология протоонкогенов с провирусными ДНК-последовательностями ретровирусов объясняет роль вирусов в некоторых возможных механизмах злокачественного перерождения клеток. При рекомбинации и внедрении в геном вируса последовательности, соответствующей протоонкогену, вследствие высокого уровня мутирования ретровирусов, вероятность трансформации протоонкогена в онкоген возрастает. Далее процесс трансформации клетки может идти двумя путями: либо при последующей рекомбинации происходит обратное встраивание онкогена в клетку и экспрессия измененного белка, либо увеличение дозы аномального гена путем амплификации.
Гомология протоонкогенов и вирусных онкогенов лежит в основе и их обозначения. Для этого используется аббревиатура, состоящая из первых букв названия вируса, в котором впервые был обнаружен данный ген, а иногда индуцируемой им опухоли и поражаемого вида.
Механизм амплификации гена имеется и в норме, гак как необходим для защиты клетки от стрессовых ситуаций. Например, резистентность опухолевых клеток к химиотерапии мегатрексатом при миелоидном лейкозе обусловлена амплификацией гена дигидрофолат-редуктазы - фермента, блокируемого этим препаратом.
Наиболее часто наблюдается амплификация протоонкогенов тус-семейства. Этот механизм активации протоонкогена обнаружен при таких опухолях как нейробластома, около половины случаев которой обусловлено амплификацией гена N-тус, и мелкоклеточная карцинома легких, возникающая вследствие амплификации генов с-тус: N-myc и L-myc.
Амплификация гена может быть выявлена в виде малых добавочных хромосом, известных как минихромосомы, гомологичные соответствующим участкам хромосом. Увеличение числа копий некоторых протоонкогенов, например, N-myc при нейробластомах, характерно для поздних стадий малигнизации (озлокачествления) и предположительно может служить тестом для определения стадии развития рака и прогноза течения заболевания.
Повышение экспрессии протоонкогена возможно и вследствие других механизмов, приводящих к эффекту дозы гена. Так усиление транскрипции гена может быть обусловлено эпигеномными изменениями: снижением/отсутствием действия специфического репрессора и гиперметилированием.
- Читать далее "Генетические предпосылки развития опухоли. Трансформации клетки в опухоль."
Оглавление темы "Диагностика наследственных заболеваний.":1. Пероксисомные болезни. Синдром Цельвегера.
2. Генетика широко распространенных заболеваний. Механизмы развития предрасположенных болезней.
3. Болезни с наследственной предрасположенностью. Маркеры наследственно предрасположенных болезней.
4. Анализ сцепления наследственно предрасположенных болезней с маркерами. Особенности наследственных болезней.
5. Эссенциальная гипертензия и гены. Атеросклероз и генетика. Бронхиальная астма и гены.
6. Канцерогенез. Генетические аспекты канцерогенеза. Протоонкогены. Гены-супрессоры.
7. Генетические предпосылки развития опухоли. Трансформации клетки в опухоль.
8. Медико-генетическое консультирование. Профилактика наследственной патологии.
9. Пренатальная диагностика наследственных заболеваний. Дородовая диагностика наследственной патологии.
10. Преимплантационная диагностика наследственных заболеваний. Диагностика наследственной патологии до имплантации.

