Механизмы развития (патогенез) острого повреждения легких и ОРДС
Острое повреждение легких (ОПЛ) (также называемое некардиогенным отеком легких) проявляется внезапной значительной гипоксемией и диффузной легочной инфильтрацией при отсутствии сердечной недостаточности. Острый респираторный дистресс-синдром (ОРДС) является тяжелым ОПЛ.
ОПЛ и ОРДС характеризуются увеличенной сосудистой проницаемостью и гибелью эпителиальных и эндотелиальных клеток, ассоциированными с воспалительным процессом. Гистологически эти состояния проявляются диффузным альвеолярным повреждением. В большинстве случаев ОПЛ связаны с сепсисом. ОПЛ неустановленной этиологии обозначают термином «острая интерстициальная пневмония».
ОРДС — хорошо распознаваемое осложнение различных заболеваний, возникающее вследствие прямого повреждения легких и при системных нарушениях. Во многих случаях ОРДС развивается вследствие сочетания различных предрасполагающих факторов (например, шока, кислородотерапии и сепсиса). В тяжелых случаях может возникнуть дисфункция не только легких, но и других органов.
а) Морфология. В острой стадии заболевания легкие плотные, красного цвета и заполнены жидкостью. При микроскопическом исследовании в них обнаруживаются полнокровие, интерстициальный и внутриальвеолярный отеки, воспаление, отложение фибрина и диффузное альвеолярное повреждение. Альвеолы покрыты восковидными гиалиновыми мембранами, морфологически похожими на те, которые выявляются при болезни гиалиновых мембран у новорожденных.
Гиалиновые мембраны образованы конденсированной отечной жидкостью, богатой фибрином, смешанным с цитоплазматическими и липидными остатками некротизированных эпителиальных клеток. В стадии организации наблюдаются пролиферация пневмоцитов II типа и образование грануляционной ткани в стенках и просветах альвеол. В большинстве случаев грануляционная ткань элиминируется, но остаются минимальные функциональные нарушения.
Иногда наблюдается фиброзное утолщение альвеолярных стенок в результате пролиферации интерстициальных клеток и отложения коллагена. При летальных исходах часто обнаруживаются признаки бронхопневмонии.

б) Патогенез. Альвеолярная мембрана состоит из двух слоев — сосудистого эндотелия и альвеолярного эпителия. При ОРДС целостность этого барьера нарушается в результате повреждения эндотелия либо эпителия (чаще и того и другого одновременно). В сыворотке крови могут присутствовать в высоких концентрациях маркеры повреждения и активации эндотелия — эндотелии и фактор Виллебранда.
На ранних стадиях патологического состояния также выявляют признаки повреждения эпителия (набухание клеток, вакуолизация, образование пузырьков) вплоть до некроза. Вследствие повреждения альвеолярных мембран повышается их проницаемость, усиливается альвеолярный отек, теряется диффузионная способность, а также возникает дефицит сурфактанта, вызванный повреждением пневмоцитов II типа.
Повреждение эндотелия приводит к образованию микротромбов, что добавляет к картине диффузного альвеолярного повреждения ишемическое повреждение легочной паренхимы. Гиалиновые мембраны, характерные для ОПЛ/ОРДС, образуются в результате концентрации богатой белком отечной жидкости и захвата фрагментов некротизированных альвеолярных эпителиальных клеток.
Клеточная биология и молекулярные механизмы ОПЛ/ОРДС остаются областью активного научного исследования. Уже известно, что повреждение легких при ОРДС вызвано дисбалансом провоспалительных и противовоспалительных медиаторов, однако инициирующий сигнал, ведущий к неконтролируемой острой воспалительной реакции, еще не установлен. Вероятным кандидатом, сдвигающим баланс в сторону провоспалительных цитокинов, считают фактор транскрипции NF-кВ, активация которого жестко регулируется при нормальных условиях.
Уже через 30 мин после острого воздействия альвеолярные макрофаги усиливают синтез IL-8 — мощного хемотаксического фактора и фактора, активирующего нейтрофилы. Секреция IL-8 и подобных соединений (IL-1 и TNF) приводит к активации эндотелия, а также секвестрации и последующей активации нейтрофилов в капиллярах легких.
Нейтрофилы, как полагают, играют важную роль в патогенезе ОРДС. Гистологическое исследование легких в начале заболевания показывает увеличение числа нейтрофилов в сосудистом пространстве, интерстиции и альвеолах. Как нейтрофилы накапливаются в легких — еще не совсем понятно. Вероятно, есть 2 механизма.
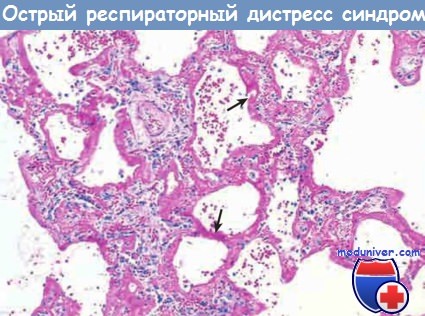
Некоторые из альвеол спавшиеся, другие расширены; поверхность многих покрыта гиалиновыми мембранами (стрелки).
Во-первых, нейтрофилы, активированные такими цитокинами, как IL-8 и TNF, экспрессируют молекулы адгезии, позволяющие нейтрофилам связываться с их лигандами на активированных эндотелиальных клетках. Во-вторых, активированные нейтрофилы, становясь более «жесткими» и менее подверженными деформации, застревают в узкой капиллярной сети легких. Активированные нейтрофилы секретируют множество продуктов (например, оксиданты, протеазы, факторы активации тромбоцитов, лейкотриены), которые повреждают альвеолярный эпителий и поддерживают воспалительный каскад.
Сочетанное повреждение эндотелия и эпителия приводит к повышению проницаемости капилляров, а потеря сурфактанта блокирует расправление альвеол.
Следует отметить, что деструктивным факторам, высвобождаемым нейтрофилами, могут противодействовать эндогенные антипротеазы, антиоксиданты и противовоспалительные цитокины (например, IL-10), активируемые провоспалительными цитокинами.
Для ОРДС также характерно нарушение регуляции системы коагуляции. В сыворотке крови и в бронхиолоальвеолярном лаваже повышается уровень тканевого фактора, а уровни антикоагулянтов и С-белка снижаются. Сам каскад коагуляции является мощным провоспалительным сигналом. Тромбин, например, способствует адгезии нейтрофилов к эндотелию. Следует подчеркнуть, что баланс между деструктивными и защитными факторами и определяет степень повреждения тканей и клиническую тяжесть ОПЛ/ОРДС.
В исходе ОРДС наступает его разрешение, которое заключается в рассасывании экссудата, удалении мертвых клеток и репарации ткани с заменой погибших клеток новыми эндотелиальными и альвеолярными эпителиальными клетками. Удаление экссудата и тканевого детрита осуществляют макрофаги (как при любом другом повреждении ткани). Эпителиальные клетки регенерируют за счет пролиферации сохранившихся пневмоцитов II типа, которые покрывают оголенную базальную мембрану.
Недавно было обнаружено, что в репарации участвуют стволовые клетки бронхоальвеолярного эпителия. Пневмоциты II типа дифференцируются в пневмоциты I типа, составляющие большинство клеток альвеолярной выстилки.
Репарация эндотелия происходит как за счет миграции эндотелиальных клеток из неповрежденных капилляров, так и за счет костномозговых эндотелиальных клеток-предшественников; последние могут быть обнаружены в кровотоке в фазу восстановления после ОРДС.
в) Клинические признаки. Лиц с ОПЛ, как правило, госпитализируют вследствие развития одного из проявлений заболевания. Тяжелая одышка и тахипноэ являются предвестниками ОПЛ. Вслед за ними развиваются, постепенно усиливаясь, цианоз, гипоксемия, дыхательная недостаточность. При рентгенографии определяются двухсторонние диффузные инфильтраты. Гипоксемию не всегда удается скорригировать с помощью кислородотерапии из-за вентиляционно-перфузионного несоответствия, тем самым создаются условия для развития респираторного ацидоза.
На ранних стадиях заболевания легкие становятся «жесткими» из-за потери сурфактанта. У небольшого количества пациентов экссудат и тканевый детрит не рассасываются, что в конечном итоге приводит к фиброзу легких. В таких случаях интерстициальный фиброз является причиной уплотнения легочной ткани и хронической легочной недостаточности.
При ОПЛ наблюдаются функциональные нарушения всей легочной ткани разной степени тяжести в отдельных участках. В легких могут быть как участки с уплотнением ткани, воспалительным инфильтратом и коллапсом (в связи с этим плохо вентилируемые, со сниженной эластичностью), так и сохранные участки, имеющие почти нормальные перфузию и вентиляцию. Перфузия плохо вентилируемых областей сохраняется, что приводит к вентиляционно-перфузионному несоответствию и гипоксемии.
Благодаря усовершенствованию терапии сепсиса, искусственной вентиляции легких и поддерживающей терапии смертность при ОПЛ снизилась с 60 до 40% (в год в США регистрируют 190 тыс. новых случаев ОПЛ). Большинство летальных исходов при ОПЛ обусловлено сепсисом, полиорганной недостаточностью, а в отдельных случаях — прямым повреждением легких.
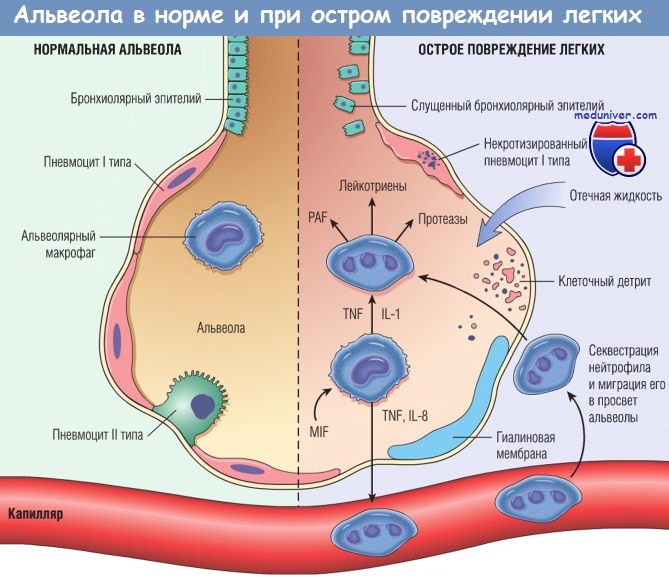
Провоспалительные цитокины, такие как интерлейкин-8 (IL-8), интерлейкин-1 (IL-1) и фактор некроза опухоли (TNF),
продуцируемые макрофагами, вызывают краевое стояние нейтрофилов в легочных капиллярах и экстравазацию этих клеток в просвет альвеол, где клетки активируются.
Активированные нейтрофилы секретируют множество факторов, таких как лейкотриены, оксиданты, протеазы и фактор активации тромбоцитов (PAF),
которые способствуют местному повреждению тканей, накоплению отечной жидкости в воздушном пространстве, инактивации сурфактанта и формированию гиалиновых мембран.
Фактор, ингибирующий миграцию макрофагов (MIF), секретируемый местно, поддерживает продолжающийся провоспалительный ответ.
Впоследствии продукция макрофагами фиброгенных цитокинов, таких как TGF-b и PDGF, стимулирует рост фибробластов и отложение коллагена на стадии репарации повреждения.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) острой интерстициальной пневмонии"
Оглавление темы "Патогенез болезней легких":- Механизмы развития (патогенез) отека легких
- Механизмы развития (патогенез) острого повреждения легких и ОРДС
- Механизмы развития (патогенез) острой интерстициальной пневмонии
- Классификация хронических диффузных болезней легких
- Классификация обструктивных болезней легких
- Механизмы развития (патогенез) эмфиземы легких
- Механизмы развития (патогенез) хронического бронхита
- Механизмы развития (патогенез) астмы
- Механизмы развития (патогенез) бронхоэктатической болезни
- Классификация рестриктивных болезней легких

