Применение стволовых клеток в неврологии. Преформация нейральных стволовых клеток
Нет сомнений, что плюрипотентные стволовые клетки, выделенные из эмбрионов или ЦНС взрослого человека, могут рассматриваться как источник новых нейронов и использоваться в клинике с целью лечения неврологической патологии. Однако основным препятствием для развития практической клеточной нейротрансплантации является тот факт, что большинство нейральных стволовых клеток не дифференцируются в нейроны после имплантации в ненейрогенные зоны зрелой ЦНС.
В обход этого препятствия предлагается весьма оригинальный новаторский метод, позволяющий in vitro получить чистую популяцию нейронов из фетальных нейральных стволовых клеток человека после трансплантации в ЦНС половозрелой крысы (Wu et al., 2002). Авторы доказывают, что дифференцировка имплантированных по данному методу клеток заканчивается формированием нейронов холинергического фенотипа, что обусловлено влиянием факторов окружающей микросреды.
Предлагаемая технология представляет интерес с точки зрения разработки новых видов терапии на основе стволовых клеток и замены поврежденных вследствие травмы или нейродегенеративного заболевания нейронов, поскольку холинергические нейроны играют ведущую роль в становлении моторных функций, функций памяти и обучения. В частности, холинергические нейроны, выделенные из стволовых клеток человека, могут использоваться для замены мотонейронов, потерянных при амиотрофическом латеральном склерозе или травмах спинного мозга.
В настоящее время нет сведений о способах наработки значительного количества холинергических нейронов из популяции преформированных митогеном стволовых клеток. Авторы предлагают достаточно простой, но эффективный метод стимуляции преформированных митогеном первичных зародышевых неиральных стволовых клеток человека в направлении развития в практически чистые нейроны после имплантации как в ненейрогенные, так и в нейрогенные зоны ЦНС половозрелой крысы. Наиболее важным результатом их работы является превращение достаточно большого количества трансплантированных клеток в холинергические нейроны при имплантации в среднюю мембрану и спинной мозг.
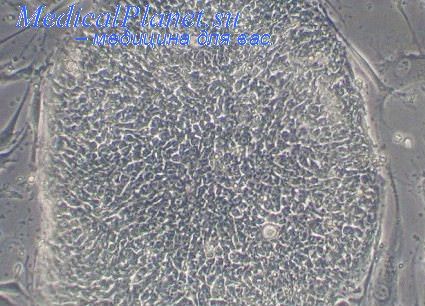
Кроме того, для преформации нейральных стволовых клеток коры головного мозга 8-недельного эмбриона человека в холиыергические нейроны in vitro предлагается использовать различные комбинации следующих трофических факторов и химических элементов: рекомбинантный основной FGF, EGF, LIF, амино-терминальный звуковой пептид мыши (Shh-N), трансретиноевая кислота, NGF, BDNF, NT3, NT4, естественный ламинин и гепарин мыши. Изначальная линия нейральных стволовых клеток человека (К048) поддерживалась in vitro в течение двух лет и выдержала 85 пассажей без изменений пролиферативных и дифференцировочных свойств при сбережении нормального диплоидного кариотипа.
Недиспергированные нейросферы 19-55-го пассажей (38-52-е недели) высаживались на поли-д-лизин и ламинин, а затем обрабатывались вышеупомянутыми факторами в различной концентрации, комбинации и последовательности. Комбинация, состоящая из основного FGF, гепарина и ламинина (в аббревиатуре FHL), дала уникальный эффект. Через одни сутки культивирования нейральных стволовых клеток эмбриона в среде FHL с или без Shh-N (комбинация Shh-N + FHL в аббревиатуре SFHL) наблюдалось стремительное размножение крупных планарных клеток.
Все другие однодневные протоколы (например такие, как основной FGF + ламинин), наоборот, привели к ограниченному радиальному распространению веретенообразных клеток, причем эти клетки не покидали сердцевину нейросфер. Через 6 суток активации и последующей десятидневной дифференциации в среде, содержащей В27, у края FHL-активированных сфер были обнаружены крупные полиполярные нейроноподобные клетки. При этом в других протокольных группах большинство нейроноподобных клеток оставались маленькими и биполярными или однополярными.
Иммуноцитохимический анализ показал, что небольшие (> 20 мкм) биполярные или однополярные клетки являлись или GABA-ергическими, или глутаматергическими, тогда как большинство крупных полиполярных клеток, локализованных у края FHL-активированных нейросфер, оказались холинергическими, поскольку экспрессировали маркеры, характерные для холинергических нейронов (Islet-1 и ChAT). Некоторые из этих нейронов одновременно экспрессировали синапсин 1. В результате пяти серий независимых экспериментов авторы установили, что общая популяция клеток в однослойных зонах на 45,5% дифференцировалась в нейроны TuJl+, r- то время как холинер-гические (ChAT+) нейроны составили всего 27,8% клеток той же популяции. Через 10 суток дополнительной дифференцировки in vitro, помимо холинергических нейронов, в FHL-активированных нейросферах было обнаружено значительное количество малых нейронов — глутаматергических (6,3%), GABA-ергических (11,3%), а также астроцитов (35,2%) и нестинпозитивных клеток (18,9%).
При использовании других комбинаций факторов роста холинергические нейроны отсутствовали, а краевые клетки нейросфер формировали или астроциты, или небольшие глутаматергические и GABA-ергические нейроны. Мониторинг резервного и активного потенциалов с применением техники whole-cell patch clamp показал, что через семь дней FHL-активирования большая часть крупных полиполярных клеток обладала потенциалом покоя, составляющим -29,0±2,0 mV, при отсутствии потенциала действия. Через 2 недели потенциал покоя возрастал до -63,6±3,0 mV, причем потенциалы действия наблюдались в момент индукции деполяризующих токов и блокировались 1М тетродотоксином, что свидетельствует о функциональной активности холинергических незрелых нейронов (Wu et aL, 2002).
- Читать далее "Имплантация нейральных стволовых клеток. Миграция нейральных стволовых клеток"
Оглавление темы "Применение стволовых клеток в неврологии":1. Митогены нейральных стволовых клеток. Реагрегация нейральных стволовых клеток
2. Культивирование нейральных прогениторных клеток. Нейротрофические факторы
3. Применение стволовых клеток в неврологии. Преформация нейральных стволовых клеток
4. Имплантация нейральных стволовых клеток. Миграция нейральных стволовых клеток
5. Трансплантация эмбриональной нервной ткани. Трансплантация клеток в спинной мозг
6. Трансплантация нервов. Трансплантация при черепно-мозговых травмах
7. Посттравматические осложнения. Трансплантация при детском церебральном параличе
8. Эффективность трансплантации эмбриональной нервной ткани. Апаллический синдром
9. Эффекты эмбриональной нервной ткани. Эмбриональная ткань как стимулятор роста аксонов
10. Гемопоэтические стволовые клетки. Особенности гемопоэтических стволовых клеток

