Температура получения меченых зондов. Технология получения меченных зондов с помощью ПЦР
Используемое для смены температур оборудование может быть как очень простым (водяные бани с разной температурой при неавтоматизированном режиме), так и весьма сложным (блоки для нагревания с быстрой сменой температуры, контролируемой с помощью микропроцессора, при автоматизированной амплификации; их производят фирмы Perkin—Elmer Cetus Instruments, Techne, Koch-Light и другие).
Процедура получения меченых зондов с помощью ПЦР описана в протоколе. Частой причиной неудач бывает недостаточное прогревание реакционной смеси на этапе денатурации. Для успешной денатурации смесь должна быть нагрета до примерно 93 С и затем быстро охлаждена до температуры отжига. Чтобы уменьшить испарение, на реакционную смесь наслаивают 50 мкл минерального масла.
Температура отжига зависит от длины праймера и его GC-содержания.
Однако на практике для каждого набора олигонуклеотидных праймеров (обычно длиной примерно 20 п.н.) эта температура подбирается экспериментально. Поскольку праймеры присутствуют в реакционной смеси в большом избытке, их отжиг происходит практически мгновенно, так что время отжига может быть очень небольшим.
Удлинение праймера при 72 С происходит в условиях, близких к температурному оптимуму для ДНК-полимеразы Taq. Время инкубации при этой температуре зависит от длины амплифицируемого фрагмента ДНК: копирование каждых 1000 п.н. занимает ~ 1 мин. Если длина фрагмента менее 150 п.н., то этап удлинения праймера можно вообще опустить, поскольку для полного удлинения отожженного праймера в этом случае вполне достаточно тех нескольких секунд, которые образец находится при 70—75 С во время перехода от температуры отжига к температуре денатурации.
Описаны также эффективный метод получения с помощью ПЦР зондов, меченных дигоксигенином, и простой метод очистки неизотопно меченных фрагментов с помощью электрофореза в легкоплавком агарозном геле.
При полимеразной цепной реакции может происходить амплификация всего одной молекулы ДНК, поэтому необходимо исключить загрязнение реактивов следовыми количествами посторонней ДНК, которая могла бы служить матрицей.
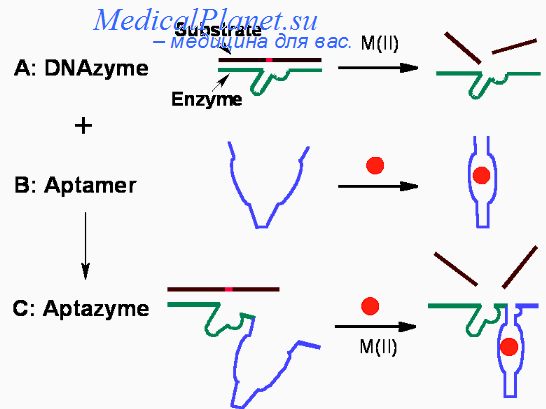
Получение меченых зондов с помощью ПЦР
А. Радиоактивное мечение
Материалы
• 20 х реакционный буфер (20 х РБ): 1 М КС1, 200 мМ трис-НС1, рН 8,3, 30 мМ MgCl2, 0,2% (в/о) желатина, по 4 мМ dATP, dTTP, dGTP
• ДНК-матрица
• Смесь праймеров: по 20 мкМ каждого из 5 - и 3 -праймеров
• dCTP (удельная радиоактивность >3000 Ки/ммоль; 110 ТБк/ммоль; 10 мкКи/мкл)
• ДНК-полимераза Taqr. 2 ЕД/мкл
• Минеральное масло
• Стоп-буфер: 300 мМ ЭДТА, рН 8,0
Методика
1. В микроцентрифужную пробирку на 500 мкл вносят при комнатной температуре в указанном порядке следующие реактивы:
• 20 х РБ 1 мкл
• Вода 1 мкл
• Смесь праймеров 2 мкл
• dCTP 15 мкл (150мкКи)
• ДНК-матрица 1 мкл (2 нг)
2. Инкубируют смесь при 93 °С 10 мин и добавляют ДНК-полимеразу Tag 0,5 мкл (1 ЕД)
3. Проводят 30-35 циклов ПЦР при эмпирически подобранных для данных праймеров температурах отжига, удлинения и денатурации, например:
Отжиг 1 мин при 50 °С
Удлинение 2 мин при 72 °С
Денатурация 1 мин при 93 °С
4. Инкубируют 10 мин при 72 °С, чтобы обеспечить полное удлинение.
5. Останавливают реакцию, добавив 2 мкл стоп-буфера. Очищают зонд от невключившихся нуклеотидов переосаждением этанолом или хроматографией на сефадексе.
6. Перед гибридизацией денатурируют меченую ДНК прогреванием в течение 5 мин при 95-100 °С с последующим резким охлаждением во льду в течение 5 мин.
Б. Нерадиоактивное мечение
Материалы
Все, как описано выше для радиоактивного мечения, со следующими изменениями: Для биотина:
• 20 х РБ: 1 М КС1, 200 мМ трис-HCl, рН 8,3, 30 мМ MgCl2, 0,2% (в/о) желатина, по 4 мМ dATP, dCTP, dGTP, 2,6 мМ dTTP, 1,4 MMbio-ll-dUTP
Для дигоксигенина:
• 20 х РБ: 1 М КС!, 200 мМ трис-HCl, рН 8,3, 30 мМ MgCh, 0,2% (в/о) желатина, по 4 мМ dATP, dCTP, dGTP, 2,6 мМ dTTP, 1,4 MMdig-11-dUTP
Методика
1. В микроцентрифужную пробирку на 500 мкл вносят в указанном порядке следующие реактивы:
• 20 х РБ (с dig-11 -dUTP или bio-11 -dUTP) 1 мкл
• Смесь праймеров 2 мкл
• ДНК-матрица 1 мкл (2 нг)
• Вода 16 мкл
2. Далее — как для радиоактивного мечения, начиная с п. 2.
- Читать далее "Кодируемые бактериофагами ДНК-зависимые РНК-полимеразы. Получение ДНК-матрицы"
Оглавление темы "Мечение нуклеиновых кислот":1. Основные методы мечения нуклеиновых кислот. Определение уровня включения нуклеотидтрифосфатов в ДНК
2. Очистка от невключившихся нуклеотидов. Центрифугирование на колонках с сефадексом
3. Мечение двухцепочечной ДНК. Метод нуклеотидного замещения
4. Метод рассеянной затравки двухцепочечной ДНК. Получение меченых зондов методом рассеянной затравки
5. Мечение ДНК с использованием фрагментов. Получение зондов с помощью ПЦР
6. Температура получения меченых зондов. Технология получения меченных зондов с помощью ПЦР
7. Кодируемые бактериофагами ДНК-зависимые РНК-полимеразы. Получение ДНК-матрицы
8. Получение РНК-зондов. Нерадиоактивное мечение РНК зондов
9. Преимущества РНК-зондов. Типы олигонуклеотидных зондов и их применение
10. Мечение 5'-концов. Мечение 5-концов при участии полинуклеотидкиназы фага Т4

