Эпидермис при нарушении барьерной функции кожи
Экспериментальное нарушение кожного барьера приводит к изменениям в кератине эпидермиса и в экспрессии белков эпидермального рогового конверта; в свою очередь, избыточная экспрессия и дефицит данных белков у мыши ведут к дефектам кожного барьера.
Ряд заболеваний, сопровождающихся нарушением барьерной функции эпидермиса, являются результатом генетических дефектов синтеза кератина, белков рогового конверта либо фермента, перекрестно связующего трансглютаминазу-1.
Ингибиция гидроксиметилглютарил СоА-редуктазы при местном применении ловастатина—препарата, понижающего уровень липидов, приводит к нарушению барьерной функции и гиперпролиферации эпидермиса. Это послужило основой для изучения специфической связи между барьерной функцией и синтезом эпидермальной ДНК. В случаях острого нарушения барьерной функции (в результате местного действия ацетона или при помощи липкой ленты), а также в модели хронической барьерной дисфункции (дефицит эссенциальных жирных кислот в питании) было выявлено увеличение синтеза ДНК, приводящее к гиперплазии эпидермиса. Увеличению синтеза ДНК и липидов частично препятствовала окклюзия.
Описанное острое или хроническое нарушение барьерной функции кожи обусловливает специфические изменения в эпидермальном кератине и в экспрессии белков рогового конверта. Отмечается повышенная экспрессия базальных кератиноцитов К5 и К14 и уменьшение кератинов дифференцировки К1 и К10. Кроме того, наблюдается экспрессия ассоциированных с пролиферацией кератинов К6 и К16 и связанного с воспалением кератина К17. Значимость кератинов для барьерной функции кожи была подтверждена на примерах мышей с дефицитом кератина К10.
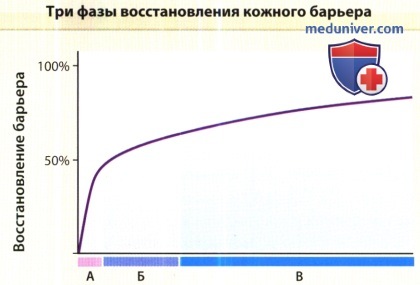
А = Секреция предварительно сформированного пула ламеллярных телец (от О до 30 минут).
Б = Увеличение синтеза липидов (свободных жирных кислот, церамида и холестерина) (от 30 минут до 5 часов); ускоренное образование ламеллярных телец и их секреция (от 2 до 6 часов).
В = Активизация глюкозилцерамида (от 9 до 24 часов), возрастание пролиферации и дифференцировки кератиноцитов (от 16 до 24 часов).
У гетерозиготного и гомозиготного потомства отмечались соответственно незначительные и тяжелые нарушения функции барьера проницаемости. Необходимо отметить, что гомозиготные новорожденные мыши с дефицитом кератина К10 имели крайне хрупкий эпидермис и умирали через несколько часов после рождения. В свою очередь у гетерозиготного потомства при рождении кожа была нормальной, однако по мере роста у животных развивался все более выраженный гиперкератоз. У гетерозиготных мышей с дефицитом К10 замедлялось восстановление барьера и нарушалась гидратация кожи.
Также отмечались изменения в составе церамидов, уменьшение глюкозилцерамида и сфингомиелина, а также снижение активности кислотной сфингомиелиназы наряду с увеличением концентрации инволюкрина. Все перечисленные факты свидетельствуют о том, что генетически обусловленные изменения в структурных белках приводят к нарушению функции кожного барьера и изменениям в дифференцировке и составе липидов. Подробности протекания данных процессов исследователям еще предстоит выяснить.
Заболевания, обусловленные моногенетическими дефектами кератинов, также подтверждают важную роль структурных белков в осуществлении барьерной функции кожи. При простом буллезном эпидермолизе наблюдается мутация кератинов базального слоя К5 или К14. Генетические дефекты супрабазальных кератинов приводят к гиперкератозу и незначительному нарушению барьерной функции.
При эпидермолитическом гиперкератозе (ЭГК) имеются дефекты кератина К1 или К10 в шиповатом слое, при эпидермолитической ладонно-подошвенной кератодермии (ЭЛПК) дефекты кератина К9 присутствуют в зернистом слое (поскольку этот кератин экспрессируется только в коже ладоней и подошв, заболевание ограничивается этими областями), при буллезном ихтиозе Сименса (ИБС) дефектным является кератин К2 (ранее обозначался как К2е) зернистого слоя.
Экспериментальное нарушение барьера проницаемости вызывает преждевременную экспрессию инволюкрина, однако экспрессия лорикрина при этом не наблюдается. Избыточная экспрессия филаггрина в супрабазальном эпидермисе мышей обусловливает задержку восстановления кожного барьера. Низкие уровни профилаггрина и филаггрина приводят к «чешуйчатому хвосту» (ft/ft) — аутосомно-рецессивной мутации у мышей, являющейся причиной сухой шелушащейся кожи и кольцевидных сокращений хвоста и лапок в неонатальный период. Целевое удаление гена инволюкрина у мышей никак не сказывалось на барьерной функции нормальной кожи, однако если кожный барьер был поврежден, его восстановление замедлялось.
Кроме того, на моделях кожи человека обнаружено, что нокдаун гена филаггрина вызывает повышение чувствительности к УФ-излучению. У мышей с дефицитом лорикрина не было нарушений барьерной функции, однако их кожа оказывалась более уязвимой для механических воздействий, что может косвенно влиять и на выполнение барьерной функции.
Изменения в пролиферации и дифференцировке эпидермиса наблюдаются также при воспалительных заболеваниях с нарушением барьерной функции кожи. Повышенная пролиферация — одна из основных характеристик псориаза; значительное возрастание эпидермальной пролиферации происходит также и в очаговой коже атопического дерматита. Следовательно, изменения кератинов и белков рогового конверта отмечаются и при воспалительных заболеваниях кожи. Таким образом, несомненным является наличие связи между эпидермальной пролиферацией, дифференцировкой и барьерной функцией кожи.
- Рекомендуем далее ознакомиться со статьей "Строение и функции субкорнеальных слоев эпидермиса"
Оглавление темы "Гистология, физиология кожи.":
