Болезнь Адамантиадиса-Бехчета: частота встречаемости, причины, механизмы развития
Болезнь Адамантиадиса-Бехчета - краткий обзор:
- Редкое заболевание, распространенное по всему миру, но с различной частотой; в основном поражаются определенные этнические группы.
- Генетически предопределенное расстройство с вероятным провоцирующим фактором внешней среды.
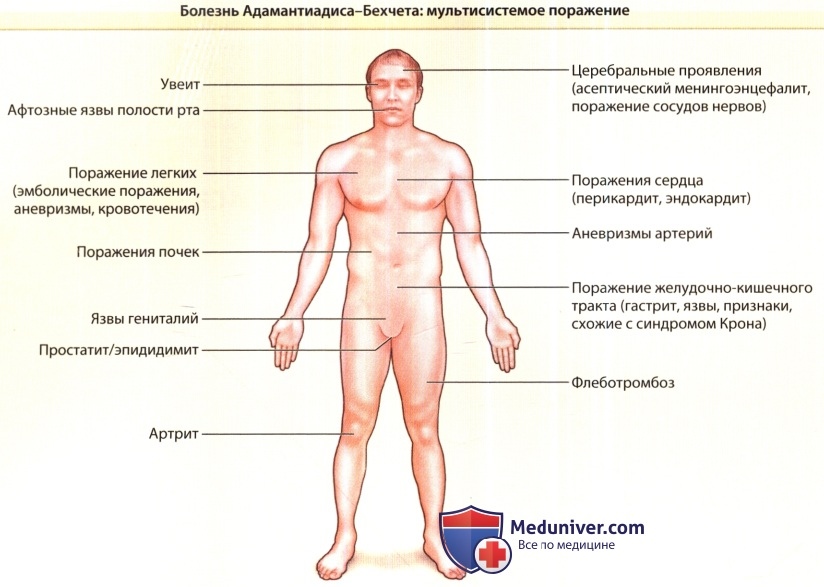
- Полисистемное поражение с афтозными язвами рта, язвами гениталий, папуло-пустулами, поражениями, подобными узловатой эритеме, увеитом и артропатией.
- Воспалительное заболевание, представленное нейтрофильной сосудистой реакцией или васкулитом.
- Хроническое рецидивирующее прогрессирующее течение и потенциально неблагоприятный прогноз (особенно у мужчин с системными поражениями; смертность от 0 до 6%).
Болезнь Адамантиадиса-Бехчета — полисистемное воспалительное заболевание неизвестной этиологии. Оно классифицируется как системный васкулит, поражающий кровеносные сосуды любого типа и калибра и характеризующийся рецидивирующими афтами рта и язвами гениталий, кожной сыпью и иридоциклитом/задним увеитом, иногда сопровождающимися артритом, а также сосудистыми, желудочно-кишечными, неврологическими или другими проявлениями.
а) История. Гиппократ из Коса (460-377 до н.э.) вероятно первым описал пациента с этим заболеванием, которое он назвал афтозные язвы в полости рта («Эпидемии» книга III, случай 7). Заболевание названо в четь Бенедиктоса Адамантиадиса, греческого офтальмолога, и Хулучи Бехчета, турецкого дерматолога, которые соответственно в 1931 и 1937 годах описали пациентов с характерным клиническим комплексом, считая его отдельной нозологической единицей.
Первая международная мультидисциплинарная конференция была организована двумя дерматологами, докторами М. Monacelli и Р. Nazarro в Риме, Италия, в 1964 году.
б) Эпидемиология. Болезнь Адамантиадиса-Бехчета распространена по всему миру с различной частотой и эндемична для восточной и центральной Азии, а также стран Средиземноморья (вдоль так называемого Шелкового пути) и редко встречается в странах Северной Европы, Центральной и Южной Африке, Северной и Южной Америке и Австралии. Распространенность заболевания в Турции оценивается в 80-420 случаев на 100000 человек, в остальных странах Азии — 7-30:100000 (в Японии 14-30:100000; в Корее 7,3:100000; в Северном Китае 14:100000; в Саудовской Аравии 20:100000; в Иране 17:100000) и 1,5:100000 в Южной Европе. В Северной Европе (0,27-1,18:100000) и США (0,12-0,33:100000) заболевание встречается редко.
В странах с несколькими этническими популяциями, в том числе потомками туркменов и монголов заболевают в основном последние. Увеличение распространенности заболевания связано с его хроническим течением. Ежегодная заболеваемость низка: в Японии (1990 г.) и Германии (2005 г.) она составляла 0,75-1,0 новых случаев на 100000 человек. Болезнь Адамантиадиса-Бехчета чаще всего поражает пациентов в возрасте 20-40 лет, однако сообщалось о более ранних и поздних случаях (от первого года жизни до 72 лет). В различных этнических группах частота ювенильных случаев составляет 2-21%; распространенность во Франции 0,17:100000. В отличие от сообщений из Турции и Японии о преобладании мужчин, заболеваемость среди женщин за последние годы значительно возросла. В настоящее время оба пола поражаются с равной частотой; преобладание мужчин до сих пор наблюдается в популяции арабов, тогда как в Корее, Китае, некоторых странах северной Европы и США чаще заболевают женщины.
в) Этиология и патогенез. Этиология заболевания остается неизвестной, однако в качестве предполагаемых причин изучают генетические факторы, инфекционные агенты, загрязнение окружающей среды, иммунологические механизмы, а также эндотелиальные факторы и факторы свертывания крови. Эндемическое распространение по Великому шелковому пути, поражение в основном определенных этнических групп (в основном туркменов и монголов), а также иммуногенетические данные подтверждают гипотезу о том, что заболевание следовало за миграцией древних кочевых племен.
С другой стороны, широкий разброс распространенности заболевания в одних и тех же этнических группах в различных районах проживания указывает на дополнительные провоцирующие факторы среды. Таким образом, в распространении заболевания может участвовать перенос генетического материала, наряду с неизвестным экзогенным фактором.
1. Генетика и иммуногенетика. Не наблюдается специфического менделевского типа наследования болезни Бехчета. Получены сообщения о семейных случаях с региональными отличиями, чаще в Корее (15%), чем в Японии и Китае (2-3%), а также чаще в арабских странах, Израиле и Турции (2-18%), чем в Европе (0-5%). Наблюдается более раннее развитие заболевания у детей, чем у их родителей, и более высокая частота семейных случаев при ювенильном заболевании.
Существует отчетливая связь между заболеванием и лейкоцитарным антигеном человека (HLA)-B51 в Японии, на Среднем Востоке и странах Средиземноморья, однако эта связь не так сильна в западных странах. Аллель также, по-видимому, связан с менее благоприятным прогнозом. Его роль в развитии заболевания точно неизвестна, тем не менее он может быть задействован в механизме заболевания за счет презентации специфических антигенов, молекулярной мимикрии с микробными антигенами или участия в нарушении связей при наличии неизвестного в настоящее время гена. Среди 24 недавно описанных аллелей, с болезнью Адамантиадиса-Бехчета чаще всего ассоциируются HLA-B5101 и -В5108.
Совокупность аминокислотных остатков (образующая эпитоп Bw4) имеет решающее значение для связывания антигена и взаимодействий естественных киллерных клеток; сообщалось также о влиянии Bw4 на усиление тяжести заболевания. Гены, предположительно связанные с болезнью, локализованы на хромосоме 6 в области между геном фактора некроза опухоли и генами HLA-B или HLAC, включая ген цепи А класса I главного комплекса гистосовместимости (аллель А6) и гены белков теплового шока. Кроме того, был обнаружен новый локус восприимчивости, картированный на участке 6р22-23. Позднее методом полногеномного поиска ассоциаций были обнаружены ассоциации на хромосомах 1р31.3[интерлейкин (IL) 23R-IL12RB2] и 1q32.1 (IL10). Была также выявлена ассоциация с болезнью Адамантиадиса-Бехчета гаплотипов гена IL-8. Полиморфизм в кодировании генов эффекторных молекул организма может способствовать восприимчивости к заболеванию и/или увеличению степени его тяжести, как, например, IL-23R в китайской популяции хань.
2. Инфекционные и предрасполагающие факторы. Болезнь Адамантиадиса-Бехчета не считается контагиозной, поскольку сообщения о горизонтальной трансмиссии отсутствуют. Тем не менее полагают, что вирусные и бактериальные инфекции инициируют иммунопатологические механизмы, приводя к заболеванию.
- Вирусные агенты. В ранних теориях патогенеза болезни Бехчета предполагалась вирусная или другая инфекционная этиология. Сообщали о парциальной транскрипции ДНК вируса простого герпеса типа 1 (ВПГ-1) в лимфоцитах периферической крови. ДНК ВПГ-1 выявлялась в слюне и язвах полости рта и гениталий, в крови пациентов также обнаруживались антитела к ВПГ-1.
- Бактериальные агенты. Известно, что активность заболевания коррелирует с бактериальной инфекцией, особенно стрептококковой. Streptococcus sanguinis преобладает во флоре слизистой рта у пациентов с болезнью Адамантиадиса-Бехчета и, по-видимому, является штаммом, который играет наибольшую роль в провокации заболевания. Антигены стрептококка и антистрептококковые антитела часто обнаруживаются в слизистой рта и сыворотке пациентов. Хроническую инфекцию, инициирующую болезнь Бехчета, объясняют наличием S. sanguinis, продуцирующего иммуноглобулин А протеиназу. У пациентов выявляются высокие титры иммуногенного антигена S. sanguinis КТН-1. Кроме этого, контакт с антигенами стрептококка может быть основным провоцирующим фактором активации заболевания.
В сыворотке пациентов с болезнью Адамантиадиса-Бехчета был обнаружен липопротеин Mycoplasma fermentas MALP-404. Интересно, что MALP-404 содержит пептидный мотив, который может быть презентирован ВИЧ-В51. Недавно была выявлена предположительная роль в бактериальной стимуляции моноцитов при болезни Адамантиадиса-Бехчета толл-подобного рецептора-2, продуцирующего провоспалительные, стимулирующие нейтрофилы факторы.
3. Иммунопатологические механизмы. Принято считать, что иммунологические механизмы играют ведущую роль в патогенезе болезни Адамантиадиса-Бехчета. В настоящее время заболевание классифицируется как аутоиммунное, вызванное первичным нарушением системы врожденного иммунитета.
- Аутоиммунные механизмы. Основные микроскопические изменения в большинстве участков активного заболевания — окклюзивный васкулит иммунной природы. Патергическая реакция вызвана быстрым накоплением нейтрофилов (гиперхемотаксисом), а позднее и Т-лимфоцитов и мо-ноцитов/макрофагов в участках укола иглой. Количество Т-клеток в периферической крови и пораженной ткани накапливается, недавно был обнаружен иммунный ответ с преобладанием Т-хелперов 1, вызванный интерлейкином (IL)-12. При активном заболевании лимфоциты экспрессируют молекулы CD29 и связываются с эндотелиальными клетками. Помимо нарушения Т-клеточного иммунитета, также страдает активация В-клеток. Могут быть задействованы циркулирующие иммунные комплексы наряду с усиленной миграцией нейтрофилов; разнообразие Т-клеток указывает на то, что специфические Т-клеточные ответы на несколько антигенов могут вызывать различные симптомы.
При болезни Адамантиадиса-Бехчета обнаруживаются в качестве аутоантигенов тропомиозины и полипептид молекулярной массы 160 кДн кинектин.
- Белки теплового шока. При болезни Адамантиадиса-Бехчета в сыворотке обнаружен повышенный уровень антител к белку теплового шока (HSP — heat shock protein). Т-лимфоциты отвечают на HSP массой 60 кДн, и при картировании эпитопа Т-клеток выявлено, что в патогенез заболевания включены четыре белковые детерминанты в составе HSP массой 60 кДн.
- Цитокины-медиаторы. В крови у пациентов с болезнью Адамантиадиса-Бехчета повышено содержание различных провоспалительных цитокинов, например, IL-1, -8, -12 и -17, а также фактора некроза опухолей α. В частности, IL-8, который, по-видимому, играет важную роль, может также выделяться эндотелиальными клетками, оказывать значительное влияние на воспалительный ответ и служить чувствительным маркером активности заболевания. Выделение цитокинов зависит от пораженного органа.
- Эндотелиальные клетки. По-видимому, основной мишенью поражения является эндотелий, однако он может быть всего лишь объектом ненормального функционирования иммунной системы. В крови пациентов с болезнью Адамантиадиса-Бехчета обнаружен иммуноглобулин М-типа (поверхностный HSP массой 47 кДн) к эндотелиальной α-енолазе. Выявлено значительное повышение концентрации эндотелина-1, что, возможно, указывает на вазоконстрикцию и является прямым результатом повышенного синтеза поврежденными эндотелиальными клетками. Тромбомодулин (гликопротеин поверхности клетки сосудистого эндотелия), количество которого также увеличивается в крови пациентов с обострением заболевания, может повреждать эндотелиальные клетки.
- Рекомендуем далее ознакомиться со статьей "Симптомы и клиника болезни Адамантиадиса-Бехчета"
Редактор: Искандер Милевски. Дата публикации: 20.2.2019

