Тканевая гипоксия. Причины и патогенез тканевой гипоксии.
Причины тканевой гипоксии: факторы, снижающие эффективность утилизации кислорода клетками тканей и/или сопряжения окисления и фосфорилирования.
Патогенез тканевой гипоксии
• Снижение эффективности усвоения кислорода клетками наиболее часто является результатом ингибирования активности ферментов биологического значительного изменения физико-химических параметров в тканях, торможения синтеза ферментов биологического окисления и повреждения мембран клеток.
- Подавление активности ферментов биологического окисления наблюдается при:
- Специфическом ингибировании ферментов. Примером могут служить ионы циана (CN-), препятствующие окислению цитохрома. В результате блокируется восстановление железа дыхательного фермента и транспорта кислорода к цитохрому. При этом реакции тканевого дыхания, активируемые другими агентами (не содержащими железо), не ингибируются. Однако эффективность этих реакций весьма мала и не предотвращает развития гипоксии и нарушений жизнедеятельности.
Аналогичные последствия вызывает блокада активных центров ферментов тканевого дыхания антимицином А, соединениями, содержащими сульфид-ион S2-, и некоторыми другими веществами.
- Неспецифическом ингибировании ферментов биологического окисления ионами металлов (Ag2+, Hg2+, Cu2+). При этом указанные металлы обратимо взаимодействуют с SH-группами фермента с образованием его неактивной мер-каптоидной формы.
- Конкурентном ингибировании ферментов биологического окисления. Оно заключается в блокировании активного центра фермента веществом, имеющим структурную аналогию с естественным субстратом реакции. Эффект конкурентного ингибирования фермента может быть устранён или снижен при возрастании содержания в клетке истинного субстрата. В роли конкурентных ингибиторов могут выступать оксалат и малонат, блокирующие взаимодействие сукцината с сукцинатдегидрогеназой в цикле трикарбоновых кислот; фторлимонная кислота, конкурирующая за активный центр аконитазы с цитратом.
- Изменения физико-химических параметров в тканях (температуры, электролитного состава, рН, фазового состояния мембранных компонентов) в более или менее выраженной мере снижают эффективность биологического окисления. Отклонение от нормы указанных и других параметров наблюдается при многих болезнях и патологических состояниях: гипертермиях и гипотермиях, недостаточности различных органов (сердца, почек, печени), анемиях и ряде других.
- Торможение синтеза ферментов биологического окисления может наблюдаться при общем или частичном (особенно белковом) голодании; при большинстве гипо- и дисвитаминозов; нарушении обмена минеральных веществ, необходимых для синтеза ферментов.
- Повреждение мембран. В наибольшей мере это относится к мембранам митохондрий. Повреждение и деструкция мембран являются результатом:
- Чрезмерной интенсификации свободнорадикальных и липопероксидных процессов.
- Активации гидролаз лизосом.
- Детергентного действия избытка амфифильных соединений.
- Перерастяжения и разрыва набухших клеток и их митохондрий.
Указанные механизмы повреждения клеточных мембран реализуются при многих патологических процессах и болезнях неинфекционного и инфекционного генеза, сопровождающихся расстройствами дыхания, кровообращения, питания, развитием иммунопатологических реакций и ряда других состояний. Важно, что выраженная гипоксия любого типа сама по себе активирует многие механизмы, приводящие к повреждению мембран и ферментов клеток с развитием тканевой гипоксии.
• Снижение степени сопряжения окисления и фосфорилирования макроэргических соединений в дыхательной цепи.
- В этих условиях увеличиваются расход кислорода тканями и интенсивность функционирования компонентов дыхательной цепи. Однако большая часть энергии транспорта электронов трансформируется в тепло и не используется для ресинтеза макроэргов. Эффективность биологического окисления снижается. Клетки не получают энергетического обеспечения. В связи с этим нарушаются их функции и жизнедеятельность организма в целом.
- Выраженной способностью разобщать процессы окисления и фосфорилирования обладают многие эндогенные агенты (например, избыток Са2+, Н+, ВЖК, йод содержащие гормоны щитовидной железы), а также экзогенные вещества (2,4-динитрофенол, дикумарин, пентахлорфенол, грамицидин и др.).
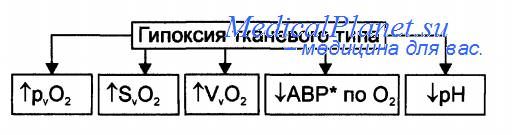
Изменения газового состава и рН крови при тканевой гипоксии
Изменения газового состава и рН крови при тканевой гипоксии представлены на рисунке.
• Увеличение парциального напряжения кислорода в венозной крови.
• Повышение сатурации Нb кислородом в венозной крови.
• Увеличение объёмного содержания кислорода в венозной крови.
• Нормальный диапазон р02, S02 и V02 в артериальной крови (в типичных случаях).
• Уменьшение артериовенозной разницы по кислороду (исключение — тканевая гипоксия, развившаяся при действии разобщителей окисления и фосфорилирования).
• Негазовый ацидоз.
- Читать далее "Субстратный тип гипоксии. Перегрузочный тип гипоксии."
Оглавление темы "Виды гипоксии. Патогенез гипоксии.":1. Гемический тип гипоксии. Причина и патогенез гемической гипоксии.
2. Тканевая гипоксия. Причины и патогенез тканевой гипоксии.
3. Субстратный тип гипоксии. Перегрузочный тип гипоксии.
4. Смешанный тип гипоксии. Причины и патогенез смешанной гипоксии.
5. Адаптивные реакции организма при гипоксии. Экстренная адаптация к гипоксии.
6. Долговременная адаптация при гипоксии.
7. Расстройства при гипоксии. Расстройства обмена веществ при гипоксии.
8. Резистентность органов к гипоксии.
9. Нарушения функций почек при гипоксии. Расстройства функций печени при гипоксии.
10. Система пищеварения, имунная система при гипоксии. Принципы устранения и профилактики гипоксии.

