УЗИ в неонатологии у постели больного (на месте, point-of-care)
Оглавление:- Центральные катетеры
- Установка эндотрахеальной трубки
- Ультразвуковое исследование сердца
- Ультразвуковое исследование легких и плевры
- Неврологическое ультразвуковое исследование
- Нюансы
- Клинические примеры
- Контрольные вопросы
- Список литературы и сокращений
Ключевые моменты:
• Ультразвуковой контроль может сократить количество попыток манипуляции и время процедуры при установке пупочных венозных и артериальных катетеров, а также периферических имплантируемых центральных катетеров.
• Хрящевые части грудины и ребра новорожденных не препятствуют ультразвуковой визуализации сердца в грудной клетке, легких и структурах средостения.
• Большинство неонатологов знакомы с тем, как интерпретировать ультразвуковые изображения головного мозга, полученные специалистами радиологии, и могут быстро научиться выполнять УЗИ головы.
УЗИ давно используется в лечении тяжелобольных новорожденных. Это неотъемлемая часть неврологического мониторинга внутрижелудочкового кровотечения, а также постоянного кардиологического мониторинга врожденных пороков сердца начиная с пренатального периода. В последние годы неонатологи все чаще используют УЗИ, отдавая ему центральную роль в медицине матери и плода как безопасному методу визуализации, который не подвергает пациентов воздействию ионизирующего излучения. Все больше неонатологов для того, чтобы руководствоваться клиническими решениями, получают и интерпретируют базовые ультразвуковые изображения в сотрудничестве со специалистами по первичной визуализации, и с увеличением доступности ультразвуковых аппаратов базовые навыки работы с ультразвуком в конечном итоге станут стандартным набором навыков для большинства неонатологов.
1. Катетеризация пупочных вен и артерий. ЦВК необходим новорожденным для адекватного парентерального питания и введения внутривенных препаратов. Новорожденным чаще всего вводят пупочные катетеры и периферические имплантированные ЦВК (peripherally inserted central catheters — PICC). Введение временных центральных венозных катетеров в подключичную, внутреннюю яремную или бедренную вены новорожденных в последние годы увеличилось в связи с доступностью ультразвуковой навигации.
Во время введения пупочного венозного катетера (ПВК) у новорожденных для проверки точного положения кончика катетера на слиянии ПП и НПВ используется УЗИ у постели больного. Использование УЗИ сокращает количество попыток манипуляции, время процедуры и количество рентгенограмм. Для идентификации пупочной вены и артерий у новорожденных УЗИ не требуется, и, следовательно, основной его функцией является позиционирование кончика катетера. ПВК вводится в пупочную вену, проходит крани-ально по направлению к левой воротной вене и венозному протоку и располагается на месте слияния ПП и НПВ. Пупочный артериальный катетер (ПАК) вводится каудально в соответствующую внутреннюю подвздошную артерию через одну из общих подвздошных артерий и располагается в нисходящей аорте (рис. 1).
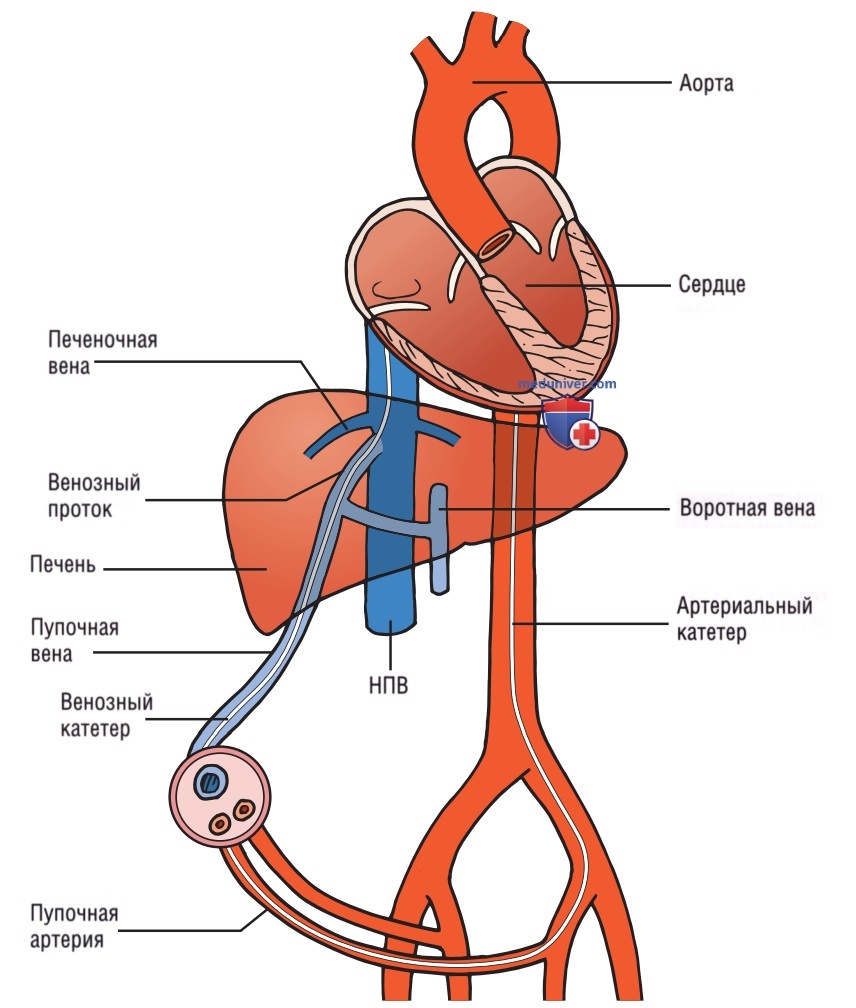
- МЕТОДИКА. Обычно предпочтитают использование датчика с фазированной решеткой, но другие типы датчиков, способные генерировать секторообразное изображение, например микроконвексный или линейный, установленные в трапециевидном режиме, могут использоваться для оценки положения кончика катетера, установленного через пупочную вену у новорожденных. Настройки сердца чаще всего используются с индикатором ориентации экрана в правом верхнем углу.
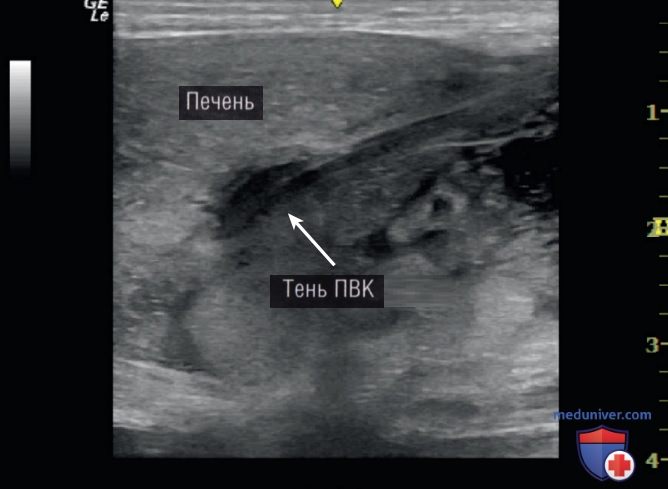
Для установки ПВК под контролем УЗИ в идеале необходимы два специалиста: один — для продвижения катетера, а второй — для проведения ультразвуковой визуализации под стерильными простынями. При выполнении одним специалистом поверхность живота обрабатывают от пупка до мечевидного отростка, и датчик покрывают стерильной оболочкой. Датчик помещают на верхнюю часть живота так, чтобы маркер ориентации («точка») указывал краниально. Ультразвуковой луч направлен параллельно позвоночнику, чтобы определить внутрипеченочный сегмент НПВ в продольном сечении. Прежде чем ПВК будет виден в НПВ, внутри вен видна только темная тень ПВК, и эта тень отслеживается по мере продвижения катетера (рис. 2). Тень ПВК в педиатрии является наиболее очевидным признаком положения катетера.
Как только ПВК попадает в НПВ, его легко увидеть с помощью УЗИ (рис. 3).
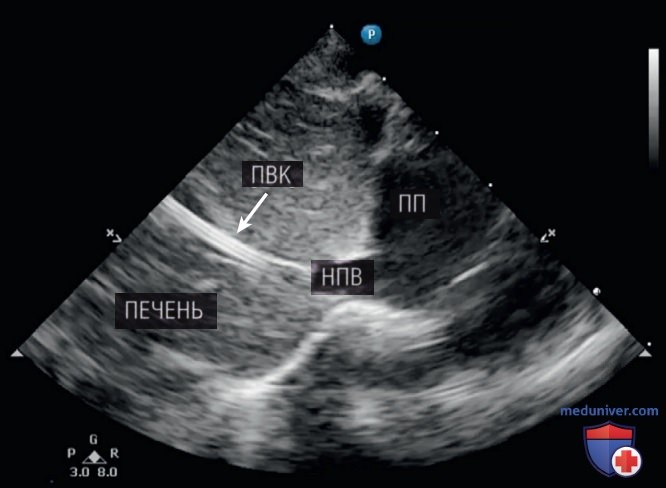
Катетер следует разместить немного дальше краниально над переходом НПВ-ПП (около 0,5 см), подальше от печени, где может возникнуть экстравазация инфузии.
Для введения ПАК под контролем УЗИ управлять датчиком оптимально второму специалисту. Сначала определите нисходящую брюшную аорту, установив датчик по срединной линии выше пупка так, чтобы маркер ориентации датчика был направлен краниально. Мышечную пульсирующую аорту относительно легко идентифицировать с помощью УЗИ. При продвижении ПАК кончик становится легко визуализируемым по мере приближения к печени. В целом ПАК легче визуализируется, чем ПВК, и он находится слева от срединной линии и дорсальнее ПВК (рис. 4). Кончик катетера должен располагаться немного краниальнее диафрагмы, что соответствует уровню Т6—Т9.
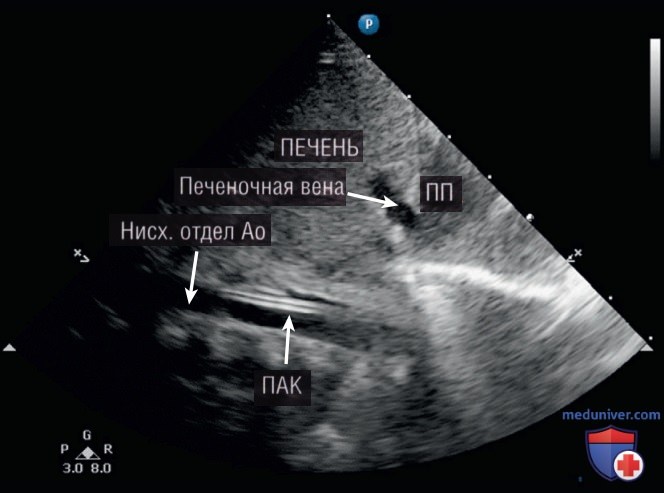
Ориентируясь на размещение кончика катетера немного выше уровня диафрагмы, кончик можно продвигать под прямой визуализацией до тех пор, пока он не окажется в правильном положении. Позиционирование ПАК под ультразвуковым контролем в низком положении ниже чревного ствола и почечных артерий может быть невозможно из-за газов в кишке.
2. Периферические имплантированные центральные венозные катетеры. Периферические имплантированные центральные венозные катетеры (PICC) широко используются для венозного доступа у новорожденных. PICC вводятся новорожденным сразу после рождения вместо ПВК, когда отсутствует венозный проток, и после удаления ПВК, как правило, на 7-10-й день жизни. Каждому ребенку с массой тела при рождении <1500 г PICC требуется обычно для доставки жидкости, питания и лекарств. Данные о диаметре катетера и риске тромбоза ограничены; однако ретроспективные серии случаев предполагают, что ограничение диаметра катетера до половины диаметра сосуда может снизить частоту возникновения тромбоза.
Ретроспективно PICC вводятся в вены как верхней, так и нижней конечности с помощью кончиков катетера в ВПВ или НПВ. Для новорожденных PICC были разработаны до минимального значения в 1 Fr и имеют различные методы введения. Небольшой размер этих катетеров затрудняет их просмотр на простых рентгенограммах и иногда требует введения контрастных веществ для определения местоположения кончика. Катетеры PICC определяются с помощью УЗИ в виде гиперэхогенных структур. При использовании ультразвукового контроля для введения PICC время процедуры и количество попыток сокращаются.
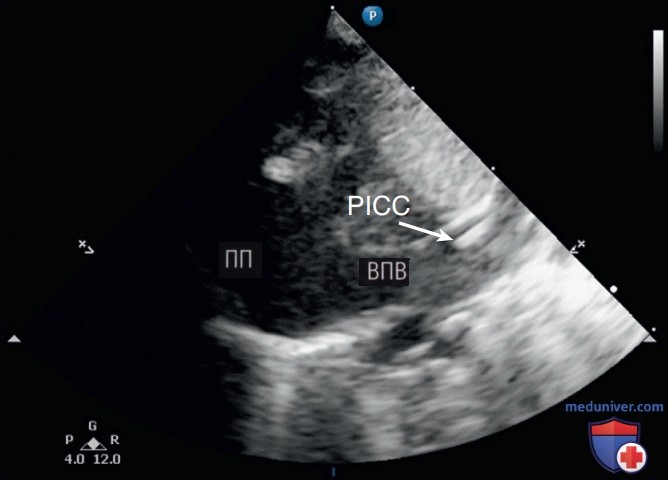
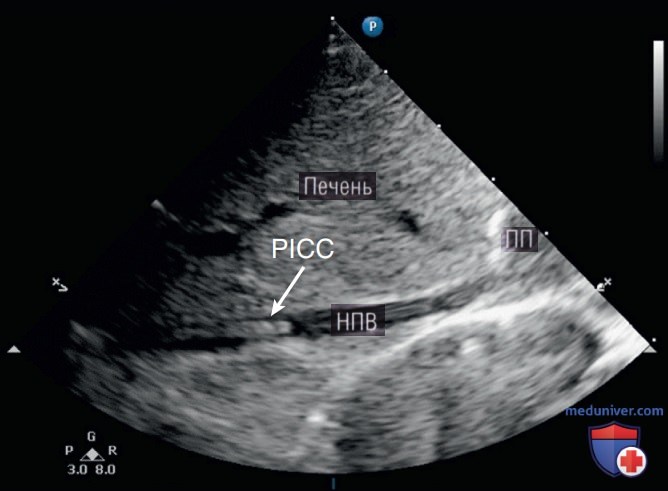
- МЕТОДИКА. Методы визуализации и контроля введения иглы в реальном времени, используемые у новорожденных, такие же, как и у детей. Предпочтительно управление датчиком вторым специалистом под стерильными простынями, в то время как основной оператор продвигает катетер. ВПВ можно определять у новорожденных благодаря наличию хрящевых стенок в грудной клетке. Поместите датчик слева от середины грудины так, чтобы маркер ориентации датчика был направлен краниально для определения ВПВ. Из данного положения наклоните датчик к правой стороне пациента, чтобы вывести ВПВ глубже выступающей аорты. Катетер может быть визуализирован в ВПВ и должен быть расположен чуть выше или в месте соединения ВПВ с ПП (рис. 5). Для PICC нижних конечностей НПВ определяют в субкостальном продольном сечении аналогично размещению ПВК. Датчик должен быть отцентрирован строго продольно над НПВ для оптимальной визуализации (рис. 6).
Для PICC верхних конечностей идентифицируйте кончик при положении руки, согнутой на 45° в локте и подмышке, чтобы убедиться, что видно самое дальнее и глубокое положение кончика, но при этом убедитесь, что катетер не входит в ПП. Также при позиционировании PICC нижних конечностей идентифицируйте кончик катетера в положении пациента с коленом и бедром, согнутыми примерно на 90°, чтобы убедиться, что видна его самая глубокая позиция.
Когда возникают трудности с поиском кончика катетера, оператор может промыть катетер небольшим количеством физиологического раствора, и турбулентный поток покажет местоположение. Кончики PICC, установленных через верхние и нижние конечности, должны располагаться на верхнем и нижнем кавоатриальных соединениях соответственно, чтобы обеспечить адекватный кровоток вокруг катетера и снизить риск тромбоза или сердечной аритмии. Катетер может стать менее видимым или полностью невидимым, если кончик будет находиться за пределами соединения ВПВ—ПП, потому что турбулентный поток ПП будет постоянно перемещать катетер. Если PICC, установленный через нижнюю конечность, не определяется, то кончик катетера может находиться в средней части брюшной полости, и его визуализация может быть затруднена из-за газа в кишке.
б) Установка эндотрахеальной трубки. Эндотрахеальные трубки (ЭТТ) вводят через носовой ход или рот и проводят через голосовые складки, заканчиваясь на полпути между входом в дыхательные пути и килем трахеи. Локализация ЭТТ с помощью УЗИ может представлять техническую проблему, поскольку воздух вокруг трубки мешает прямой ее визуализации. Однако установка ЭТТ в трахею по сравнению с пищеводом может быть с уверенностью распознана с помощью небольшого линейного датчика, установленного поперек гортани у взрослых и детей. У новорожденных распознавание ЭТТ проходит легче, чем у взрослых или детей, благодаря их хрящевому строению грудины и ребер и более высокому содержанию жидкости в организме. Подтверждение местоположения кончика ЭТТ в продольном сечении с помощью линейного датчика было показано у недоношенных и доношенных новорожденных.
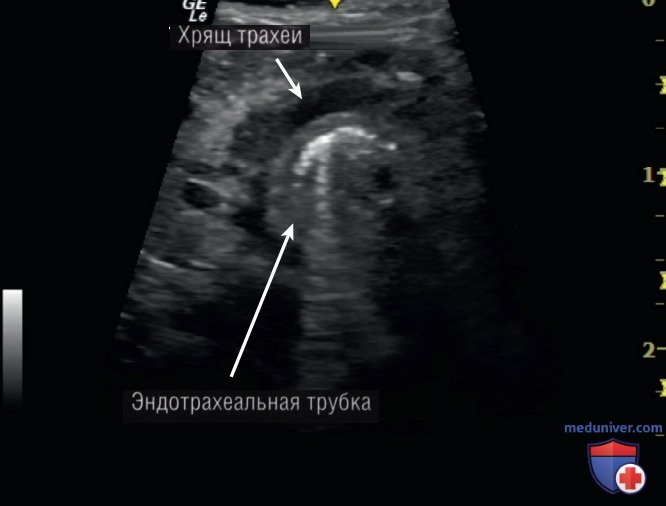
- Методика. С помощью УЗИ можно оценить два важных аспекта интубации: подтверждение и глубину размещения ЭТТ в трахее. Подтверждение успеха интубации требует идентификации ЭТТ в трахее. Во время или сразу после процедуры линейный датчик размещается в поперечной ориентации над яремной ямкой у основания шеи. ЭТТ выглядит как гиперэхогенная изогнутая линия в трахее, и воздух в ее просвете затрудняет определение других структур глубже ЭТТ (рис. 7). Если ЭТТ неправильно помещается в пищевод, трахея будет пустой, и гиперэхогенная ЭТТ будет видна в соседнем пищеводе слева от трахеи. После подтверждения установки ЭТТ в трахее важно определить глубину введения. Поверните голову новорожденного в одну сторону, а датчик поместите в продольном сечении от срединной линии до верхней трети грудины так, чтобы маркер датчика был направлен краниально. У новорожденных грудина хрящевая, сквозь нее легко проходит ультразвук.
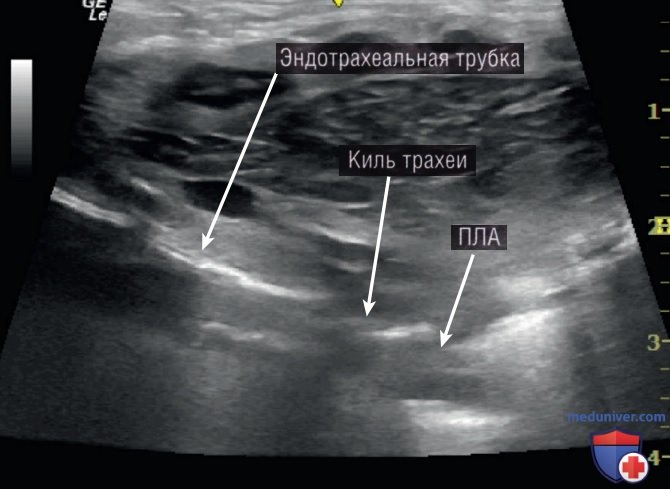
Кольца трахеи представляют собой прямоугольные эхогенные сегменты. Определите отметки трахеи по диагонали на экране, а затем найдите кончик ЭТТ в виде гиперэхогенной линии или пятна в трахее. Чтобы подтвердить, что гиперэхогенная структура является ЭТТ, осторожно сдвиньте трубку не более чем на 0,5 см внутрь и наружу, при этом на экране должно быть видно движение ее края или манжеты (рис. 8). Киль не так легко увидеть с помощью УЗИ, но правая ЛА является сосудистым ориентиром, который можно использовать для определения киля трахеи, поскольку эта артерия находится каудально к нему.
в) Ультразвуковое исследование сердца. Неонатологи все чаще проводят УЗИ сердца или эхокардиографию у постели больного для оценки гемодинамики доношенных и недоношенных детей. УЗИ позволяет оценить сложное и динамическое переходное кровообращение, вариабельные реакции незрелого миокарда в раннем неонатальном периоде и наличие внутри- и внесердечных шунтов в виде открытого овального отверстия или артериального протока (ОАП) соответственно. Отсутствие надежных измерений для оценки системного кровотока побудило неонатологов использовать УЗИ сердца у постели больного, которое предлагает новое понимание влияния АП и легочной гемодинамики у пациентов с клинической нестабильностью. Ультразвуковое исследование сердца у постели больного позволяет быстро оценить размер, функцию и гемодинамику камер сердца, обеспечивая быструю диагностическую интерпретацию в самых разных условиях, от амбулаторных клиник до ОИТ.
УЗИ у постели больного предоставляет важные клинические данные в режиме реального времени для принятия клинических решений, обеспечивая лучшее понимание основных физиологических процессов и отслеживая реакцию на лечение. Некоторые исследования продемонстрировали, что рутинное использование УЗИ сердца в неонатальном периоде может привести к раннему выявлению сердечно-сосудистых заболеваний, что может ускорить клиническое лечение и потенциально улучшить краткосрочные результаты.
Важным аспектом УЗИ сердца у постели больного является обучение медицинских работников, которые его используют. Получение точных изображений и интерпретация изображений сердца являются важными навыками в клинической практике, позволяющими медицинским работникам улучшить свою клиническую деятельность. Сотрудничество с детской кардиологией рекомендуется для обучения, поддержания навыков и постоянной клинической поддержки.
1. Регистрация изображения. УЗИ сердца у постели больного преимущественно ориентировано на использование двумерного (2D) режима для оценки состояния сердца, а ИВД, постоянно-волновой допплер (ПВД), цветовое допплеровское картирование кровотока и М-режим используются только для решения определенных кардиальных задач. У доношенных и недоношенных детей датчик с фазированной решеткой в диапазоне частот от 8 до 12 МГц обеспечивает отличное разрешение и адекватное проникновение в ткани. Эхокардиографические окна у новорожденных могут быть более сложными из-за их небольшого размера и раздутия легких, особенно у недоношенных детей и новорожденных с бронхолегочной дисплазией.
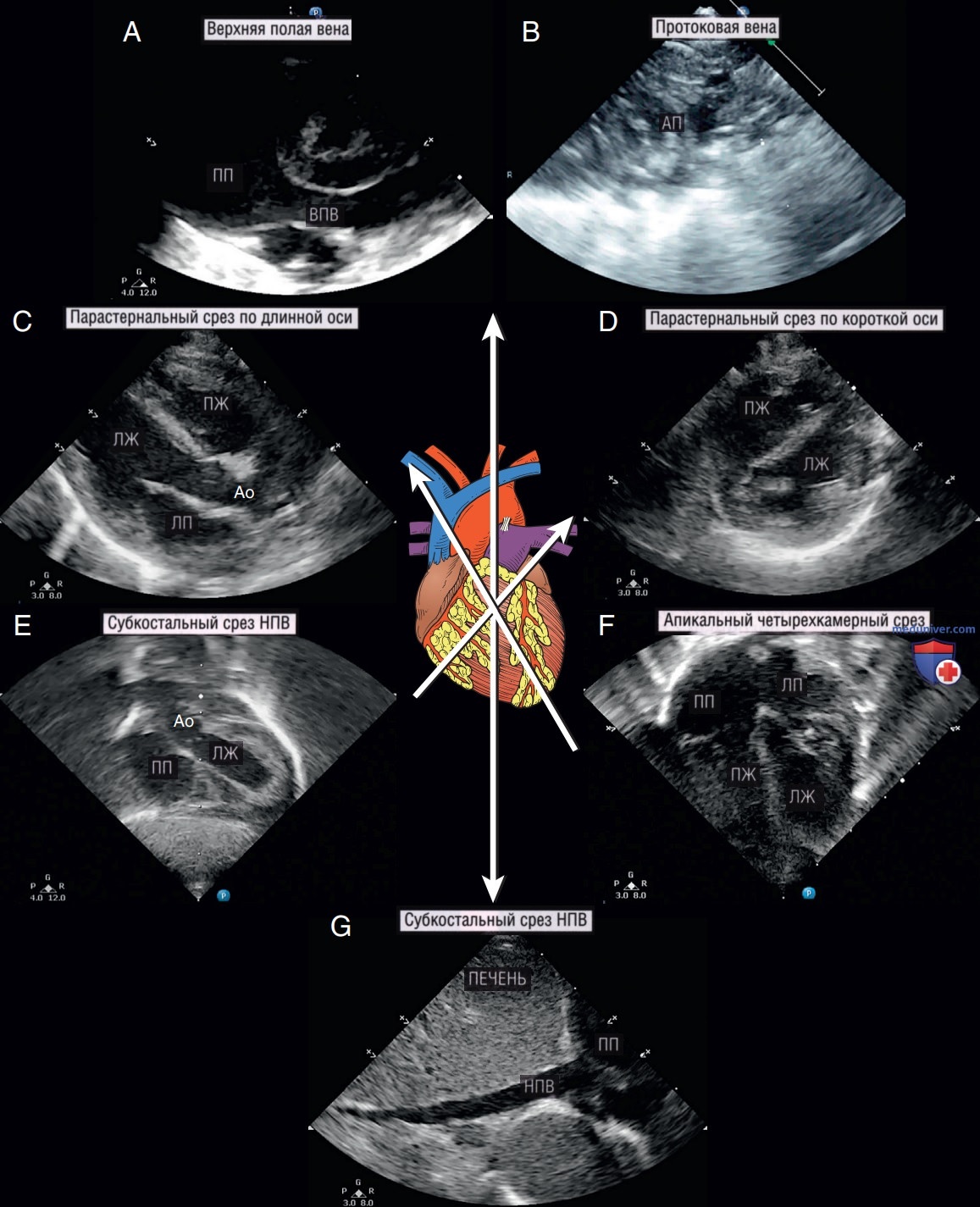
Основные эхокардиографические окна и позиции сердца в неонатологии такие же, как и у взрослых пациентов, с добавлением двух уникальных позиций ОАП и ВПВ (рис. 9).
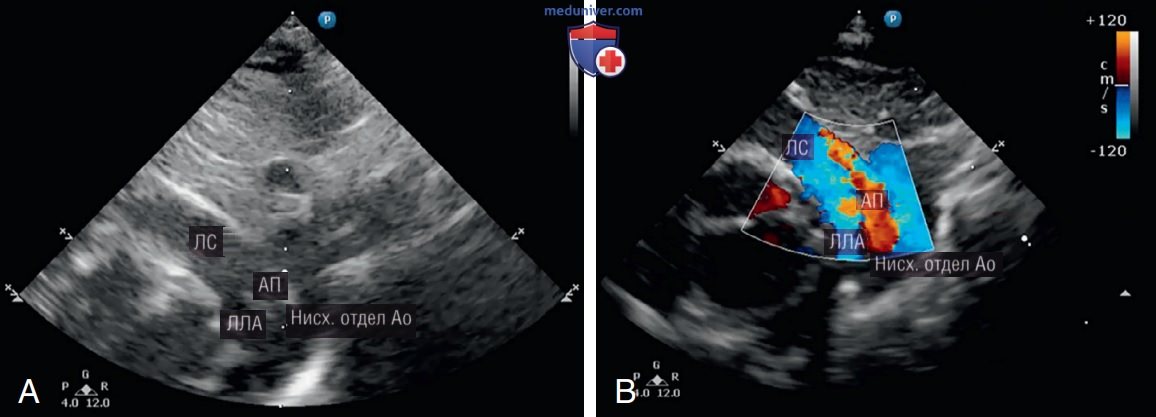
• Изображение ОАП (рис. 10): установите датчик на верхнюю треть грудины или в яремную вырезку с маркером краниально и направьте ультразвуковой луч немного левее срединной линии, чтобы визуализировать корень левой ЛА, которая будет выглядеть как дивертикул на дистальном конце легочного ствола. АП простирается от легочного ствола чуть выше корня левой ЛА до дуги аорты.
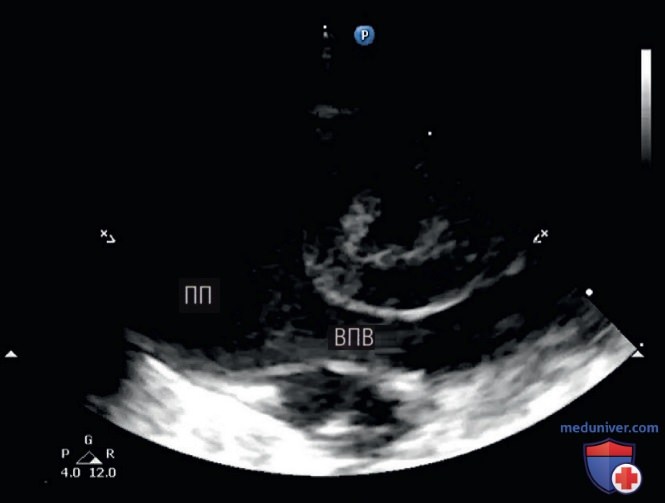
• Изображение ВПВ (рис. 11): поместите датчик над серединой грудины в продольной плоскости, немного левее срединной линии, так, чтобы маркер был направлен краниально. Слегка наклоните датчик вправо, пока не появится восходящая аорта. Продолжайте наклонять вправо, пока не появится в поле зрения ВПВ, соединяющаяся с ПП глубже восходящей аорты. Данное сечение преимущественно используется для измерения максимального и минимального диаметров ВПВ. Субкостальное сечение ВПВ используется для измерения скорости кровотока ВПВ с использованием ПВД, как будет описано ниже.
2. Интерпретация изображения. УЗИ сердца у постели больного обычно направлено на решение конкретного клинического вопроса. В следующих разделах рассматриваются некоторые из общих вариантов клинического использования в ОИТ новорожденных.
- СЕРДЕЧНЫЙ ВЫБРОС. Системная гипотензия является распространенной проблемой у новорожденных, особенно у недоношенных. Артериальное давление служит ненадежным суррогатным маркером системной перфузии органов, поскольку оно не может фиксировать сложную сердечно-сосудистую гемодинамику во время переходного кровообращения. Последовательное УЗИ сердца у постели больного дает преимущество в выявлении физиологической природы сердечно-сосудистых нарушений, будь то преднагрузка, постнагрузка или сократимость миокарда.
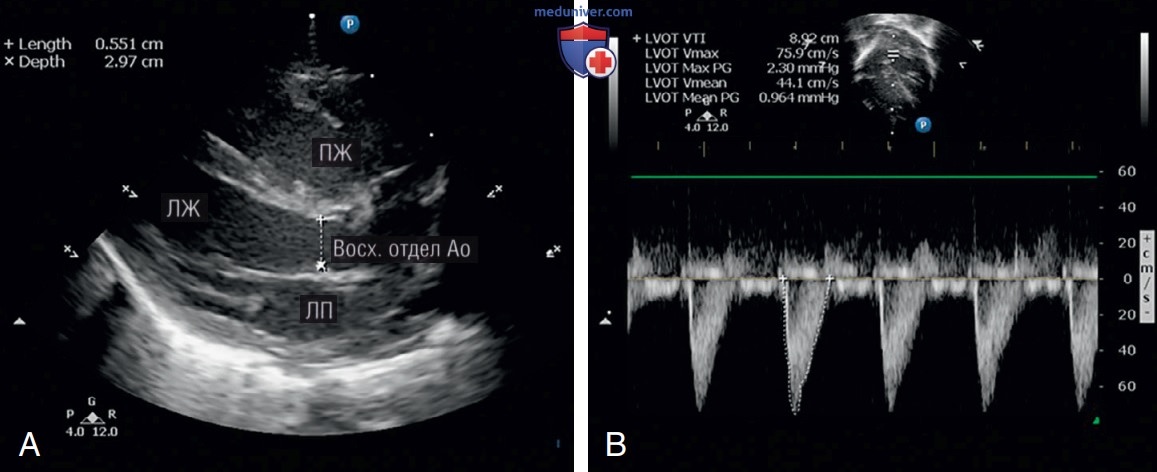
Оценка состояния внутрисосудистого объема и показателей миокарда была описана ранее. У детей и новорожденных используются одинаковые методы. Оценка ударного объема левого желудочка (УО ЛЖ) включает измерение средней скорости кровотока через АК в апикальной 5-камерной проекции с использованием ПВД, а затем определение диаметра основания аорты с парастернальной длинной оси (рис. 12). Площадь под формой волны в режиме ИВД используется для вычисления интеграла скорости-времени, который является мерой расстояния, пройденного кровью во время каждого сокращения ЛЖ. Умножение интеграла скорости-времени на площадь поперечного сечения аорты дает УО, а умножение УО на частоту сердечных сокращений (ЧСС) дает сердечный выброс (СВ). СВ делят на массу тела пациента и выражают в миллилитрах на килограмм (мл/кг) в минуту. У новорожденных исследование СВ следует применять с осторожностью. Оно может быть неверно истолковано при наличии большого ОАП со значительным синдромом обкрадывания.
Выброс ПЖ определяется с использованием того же принципа, но измеряется кровоток через клапан ЛА и с использованием диаметра легочной артерии. Выброс ПЖ характеризует кровь, возвращающуюся из большого круга кровообращения, но, как и СВ, выброс ПЖ может быть ошибочен из-за наличия межпредсердного шунта.
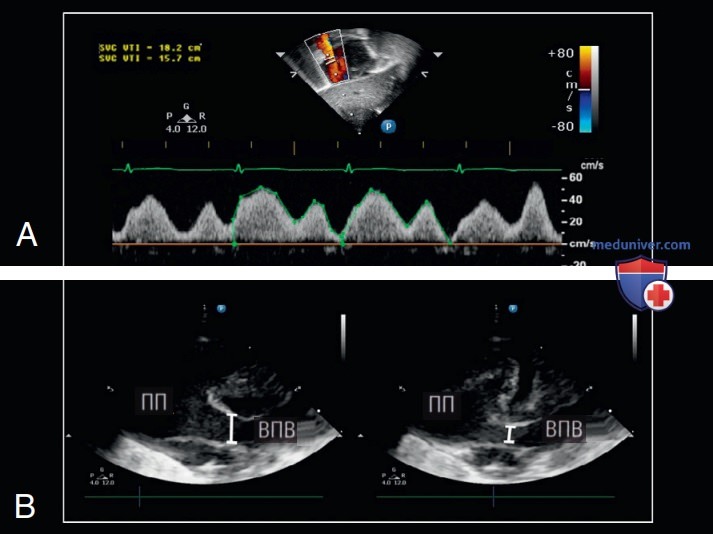
Поток ВПВ был предложен в качестве альтернативы для измерения венозного возврата из головного мозга и верхней части тела и не зависит от каких-либо шунтов. Поток ВПВ рассчитывается с использованием тех же концепций, которые описаны выше для СВ. Субкостальный доступ используется для измерения скоростей ВПВ с помощью ПВД, потому что ультразвуковой луч может быть выровнен по направлению потока. Угол инсонации можно оптимизировать, сдвинув датчик вниз на брюшную полость, чтобы максимально визуализировать поток внутри ВПВ перед его входом в ПП. Продольное сечение середины грудины используется для измерения максимального и минимального диаметров ВПВ для расчета среднего диаметра ВПВ (рис. 13). Нормальный поток ВПВ составляет от 40 до 120 мл/кг в минуту.
- ОТКРЫТЫЙ АРТЕРИАЛЬНЫЙ ПРОТОК. У недоношенных новорожденных в раннем неонатальном периоде АП обычно не закрывается, вызывая шунтирование крови слева направо, часто с неблагоприятными гемодинамическими последствиями. До появления эхокардиографии диагноз ОАП основывался на клинических данных. Однако корреляция между результатами физикального обследования и наличием ОАП по данным эхокардиографии в течение первой недели жизни недостаточна. Эхокардиография стала стандартным методом диагностики ОАП.
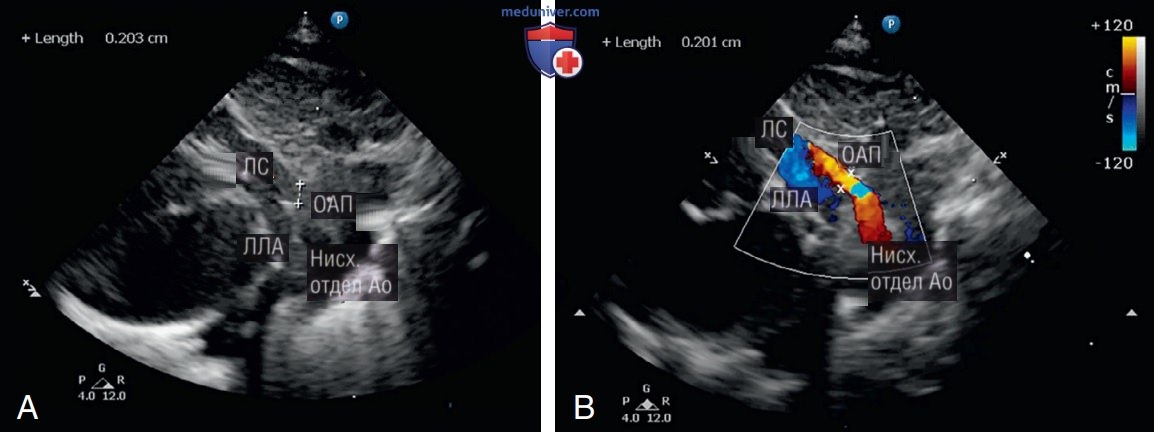
Характеристика ОАП включает измерение диаметра протока и оценку картины кровотока. Внутренний диаметр ОАП измеряется в его самом узком месте с помощью 2D и цветового допплеровского картирования кровотока (рис. 14). Несколько исследований показали, что диаметр протока более 2 мм определяет гемодинамически значимый ОАП, который вряд ли закроется спонтанно, но это предположение остается спорным. Хотя размер протока, по-видимому, является наиболее предсказуемым из всех маркеров, его значение сомнительно, поскольку 2D-оценка в одной точке может не отражать архитектуру протока по всей его длине. Размер протока также может варьировать в зависимости от насыщения кислородом и введения сурфактанта.
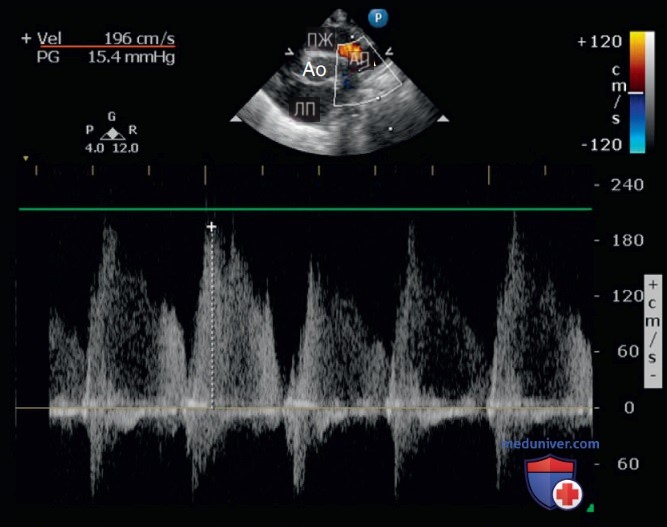
Вторая оценка артериального протока — измерение скорости трансдуктального кровотока (рис. 15). Используйте ИВД для скоростей менее 2 м/с и ПВД для скоростей более 2 м/с, скорость в канале от 1,5 до 2 м/с коррелирует с ОАП среднего размера, а скорости менее 1,5 м/с коррелируют с большим ОАП.
Увеличение эффективного легочного кровотока можно оценить по соотношению левого предсердия к аорте (ЛП:Ао) и СВ. Однако ни одно из измерений не является надежным при наличии межпредсердного шунта.
Влияние протокового «обкрадывания» на системную перфузию также может быть количественно оценено с использованием потока ВПВ в качестве суррогатного маркера системного кровотока. Трансдуктальное шунтирование большого объема связано с низким потоком ВПВ, а низкий поток ВПВ коррелирует с повышенным риском внутрижелудочкового кровоизлияния. ПВД можно использовать для оценки кровотока в нисходящей аорте, чревных артериях и артериях брыжейки, обеспечивая данные о дистальной перфузии нижней части тела.
Однако, несмотря на многолетние исследования, до сих пор существуют разногласия о роли АП в неблагоприятных исходах и о лучших эхокардиографических методах для прогнозирования этих исходов.
- ЛЕГОЧНАЯ ГИПЕРТЕНЗИЯ. Стойкая легочная гипертензия является ведущей причиной гипоксемической дыхательной недостаточности у новорожденных и диагностируется и клинически, и эхокардиографически. Детальное анатомическое обследование для исключения структурных врожденных пороков сердца является обязательным до проведения какой-либо функциональной оценки. Количественная оценка легочного артериального давления может быть проведена с использованием следующих методик.
1. Измерение систолического давления ПЖ (СДПЖ). При наличии трикуспидальной недостаточности СДПЖ можно рассчитать с помощью модифицированного уравнения Бернулли (рис. 16):
СДПЖ = давление в ПП + [4 х (максимальная скорость регургитации при трикуспидальной недостаточности)2].
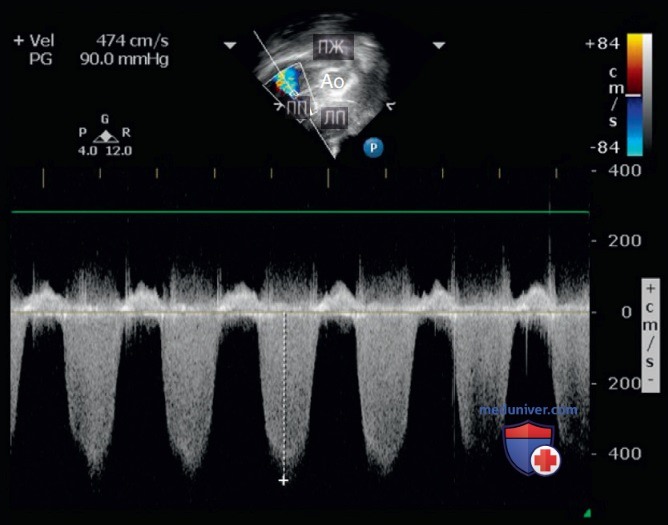
Считается, что СДПЖ эквивалентно систолическому давлению в ЛА, потому что легочный клапан открыт во время систолы ПЖ, а ПЖ и ЛА непрерывны.
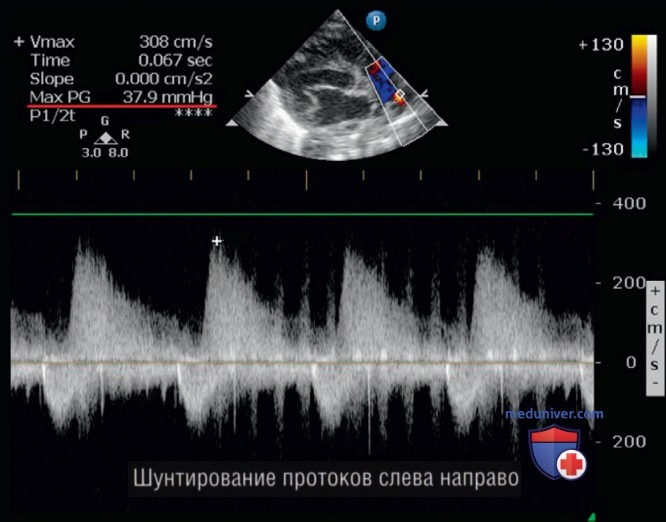
2. Оценка легочного давления при наличии неограниченного проточного кровотока: пиковая скорость трансдуктального кровотока используется для расчета разницы давления между легочным и системным кровотоком с использованием модифицированного уравнения Бернулли (рис. 17). Направление кровотока в протоке может быть использовано для оценки степени тяжести легочной гипертензии.
3. Время ускорения в ЛА: недавние исследования показали, что время ускорения в легочной артерии (ВУЛА) коррелирует с давлением в легочной артерии и сопротивлением легочных сосудов. У взрослых линейная обратная зависимость между ВУЛА и средним давлением в легочной артерии была описана в литературе 1980-х гг. Эти отношения только недавно были исследованы у детей. Одно исследование показало, что ВУЛА может точно предсказать легочную гипертензию у детей в возрасте от 1,3 до 12,6 года.
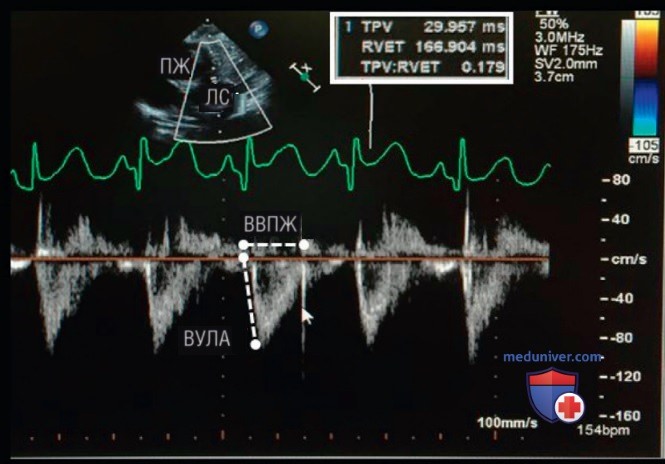
Давление в легочной артерии можно оценить по формам потока допплера в ЛА, используя отношение ВУЛА к времени выброса правого желудочка (ВВПЖ) для корректировки ЧСС. Время ускорения измеряется в виде интервала времени от начала потока на базовой линии допплеровского сигнала до пиковой скорости. ВВПЖ — общий интервал времени выброса ПЖ (рис. 18). Соотношение ВУЛА/ВВПЖ от 0,2 до 0,3 было связано с умеренно повышенным давлением в ЛА, а отношение менее 0,2 — с сильно повышенным давлением. Несколько исследований показали, что раннее выявление легочной гипертензии с помощью ВУЛА/ВВПЖ у недоношенных детей является хорошим предиктором начала хронических заболеваний легких.
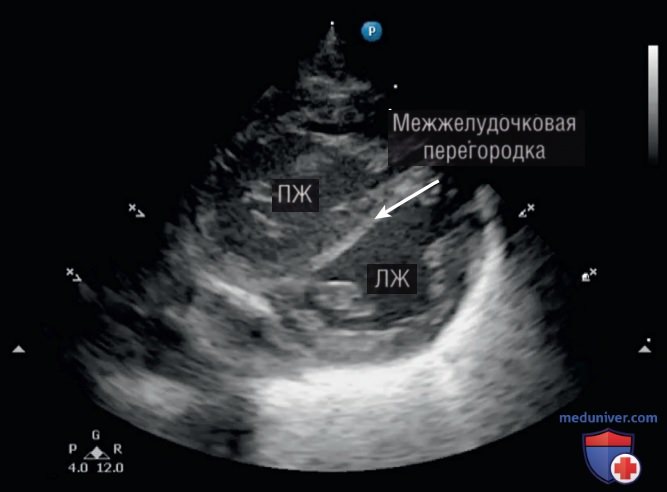
При отсутствии трикуспидальной недостаточности и ОАП давление в легочной артерии можно оценить с помощью качественных показателей, включая оценку контура и движения стенки межжелудочковой перегородки. Качественная оценка выполняется в парастернальной короткой оси. Межжелудочковая перегородка кажется плоской из-за повышенного давления в ПЖ (рис. 19) или изогнута в сторону ЛЖ в тяжелых случаях повышенного давления в ЛА.
г) Ультразвуковое исследование легких и плевры. Высокое содержание внесосудистой воды и отсутствие окостенения грудной клетки новорожденных обеспечивают оптимальное проникновение ультразвуковой волны для визуализации грудной клетки. Преходящее тахипноэ новорожденных (ПТН) независимо от гестационного возраста встречается нередко и является наиболее частой причиной неонатальной одышки. ПТН возникает в результате отека легких из-за задержки у плода абсорбции альвеолярной жидкости. Данный клинический диагноз часто подтверждается рентгенографией грудной клетки. ПТН обычно представляет собой самоограничивающийся процесс, требующий коротких периодов респираторной поддержки.
Важно дифференцировать ПТН от других неонатальных легочных процессов, включая респираторный дистресс-синдром (РДС) новороженных или синдром аспирации мекония (САМ). РДС часто, но не всегда, наблюдается у более недоношенных детей с незрелыми легкими, которым не хватает сурфактанта. Клинически подозрение на САМ возникает у новорожденных, в легкие и дыхательные пути которых внутриутробно и во время родов попадает меконий. Раннее выявление РДС и САМ позволяет начать своевременное и целенаправленное лечение, включая введение сурфактанта и эмпирических антибиотиков. Хотя существует небольшое количество исследований, описывающих использование УЗИ легких у новорожденных, текущие данные предполагают, что оно может использоваться для характеристики и дифференциации этих патологических процессов.
Кроме того, УЗИ позволяет быстро выявить пневмоторакс, еще одну частую и опасную для жизни причину тахипноэ у новорожденных (см. отдельные статьи на сайте для обсуждения УЗИ легких - просим вас пользоваться формой поиска по сайту выше).
1. Регистрация изображения. Важно использовать систематический подход к УЗИ легких, сравнивая правое и левое легкие на предмет нормальных и патологических процессов. Для ультразвуковой визуализации легких у новорожденных могут использоваться высокочастотные линейные, микроконвексные или фазированные датчики. Маркер ориентации датчика направлен краниально, и в целом легкие определяются в продольном сечении для максимальной визуализации скольжения плевры. Поперечные изображения легких могут быть получены для дополнительных изображений при фокусировании на конкретной обнаруженной патологии.
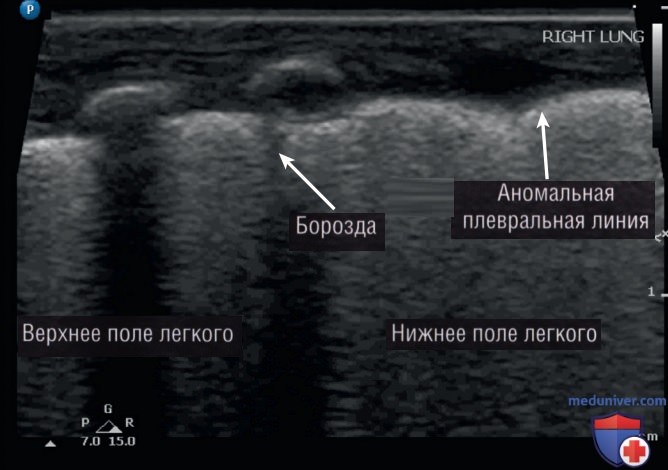
2. Интерпретация изображения. При УЗИ легких ПТН характеризуется высокой специфичностью с помощью признака «двойная точка легкого»: компактные сливающиеся В-линии в нижних полях легких и нормальные А-линии в верхних полях легких. Также можно увидеть демаркацию верхней и нижней долей легких за счет жидкости в плевральной щели. Признак «двойной точки легкого» имеет высокую чувствительность и специфичность для ПТН и не определяется у здоровых новорожденных, новорожденных с РДС, ателектазом, пневмотораксом, пневмонией или легочными геморрагиями (рис. 20). Причем легочная консолидация не распространена у пациентов с ПТН, и распознавание данного показателя предполагает альтернативный диагноз.
РДС является наиболее частой причиной дыхательной недостаточности и смертности новорожденных. На УЗИ при РДС часто выявляются консолидирующие процессы с воздушными бронхограммами и сливающимися В-линиями. Такие результаты отличают РДС от ПТН с высокой степенью чувствительности и специфичности. Ультразвуковая характеристика САМ показывает гетерогенные аномалии, включающие В-линии, консолидацию и воздушные бронхограммы.
д) Неврологическое ультразвуковое исследование. УЗИ головного мозга новорожденного возможно через открытые мягкотканные окна передних и задних родничков и открытые швы между костями черепа. Большинство неонатологов знакомы с ультразвуковыми изображениями головного мозга, полученными специалистами диагностической радиологии. Ультразвук у постели больного может обеспечить отличное представление об общей архитектуре мозга, особенно двух боковых желудочков при оценке кровотечения или кальцификации, а также паренхимы при раннем определении ишемии. Ультразвуковая визуализация головного мозга у постели больного полезна, когда внутрижелудочковое кровотечение может быть причиной острого ухудшения или гемодинамической нестабильности, особенно когда недоступны услуги диагностической сонографии.
Определение повышенного ВЧД, экстрааксиального кровотечения (то есть субдурального кровоизлияния), отека головного мозга и артериального или венозного инсульта с помощью УЗИ у постели больного изучено недостаточно, поэтому рекомендуются другие методы визуализации, такие как КТ или МРТ.
- РЕГИСТРАЦИЯ ИЗОБРАЖЕНИЯ. Стандартные изображения УЗИ головного мозга: 1) корональные сечения от лобной доли до затылочного бугра и 2) сагиттальные сечения от левой до правой теменной коры (рис. 21).
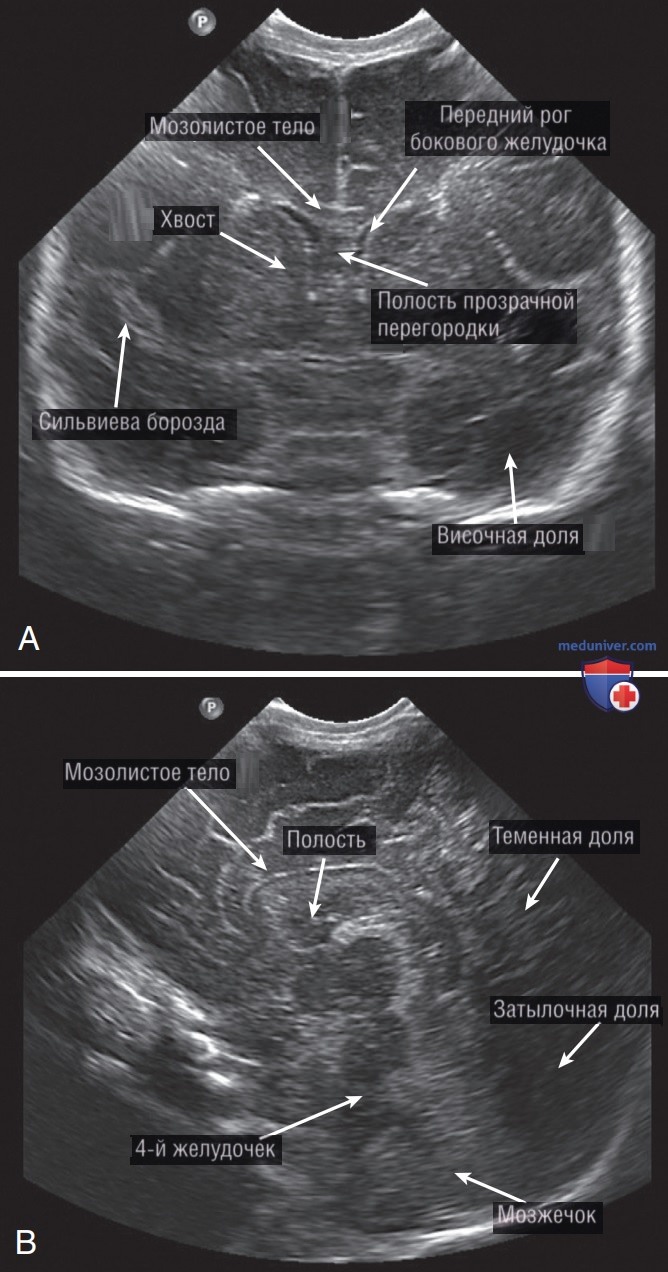
Для корональной проекции поместите датчик в поперечном положении над центром переднего родничка так, чтобы маркер датчика был направлен в правую сторону от пациента. Отцентрируйте изображение мозга на экране. Чтобы получить последовательность корональных сечений, начните с наклона датчика кпереди, чтобы захватить фронтальные изображения головного мозга, а затем наклоните датчик назад к затылку пациента. Сделайте как минимум шесть неподвижных изображений, постепенно наклоняя или перемещая датчик назад к затылку. Затем, чтобы получить сагиттальные изображения, поверните датчик на 90° в сагиттальную плоскость так, чтобы маркер датчика был направлен вперед, к передней части головы.
Держите датчик по центру родничка. Принято считать, что задний мозг должен быть виден в правой части экрана. От срединной линии наклоните датчик влево и вправо, чтобы увидеть оба полушария мозга, и сделайте не менее четырех неподвижных изображений с каждой стороны. Дополнительные изображения можно получить через задний родничок для визуализации затылочной коры, используя те же шаги, которые описаны выше.
- ИНТЕРПРЕТАЦИЯ ИЗОБРАЖЕНИЯ. Неонатологи должны знать нормальные варианты архитектуры мозга в зависимости от гестационного возраста. В то время как поверхность мозга у недоношенных детей кажется гладкой, извилины и борозды в мозге доношенных детей должны быть хорошо выражены (рис. 22).
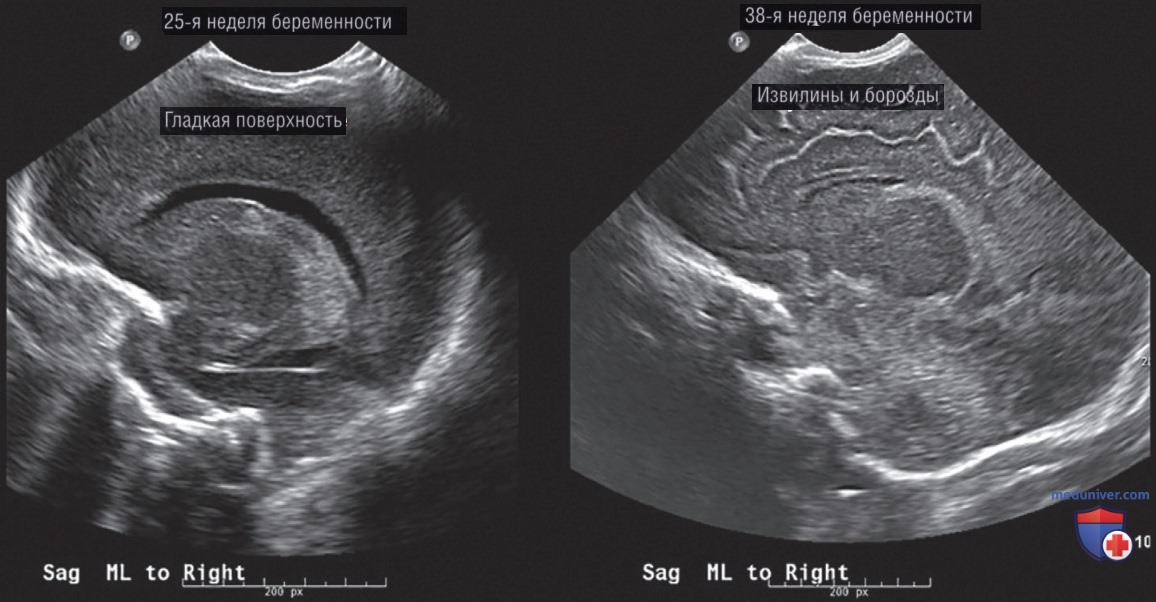
Интерпретация ультразвуковых изображений головного мозга является обычным навыком для неонатологов, потому что просмотр изображений является рутинной частью рабочего процесса большинства медиков при раннем и позднем неврологическом повреждении у пациента. Большинство неонатологов имеют обширный опыт интерпретации ультразвуковых изображений головного мозга для выявления распространенных патологий, таких как перивентрикулярная лейкомаляция (рис. 23), внутрижелудочковое кровоизлияние (рис. 24) и внутричерепное кровоизлияние (рис. 25).
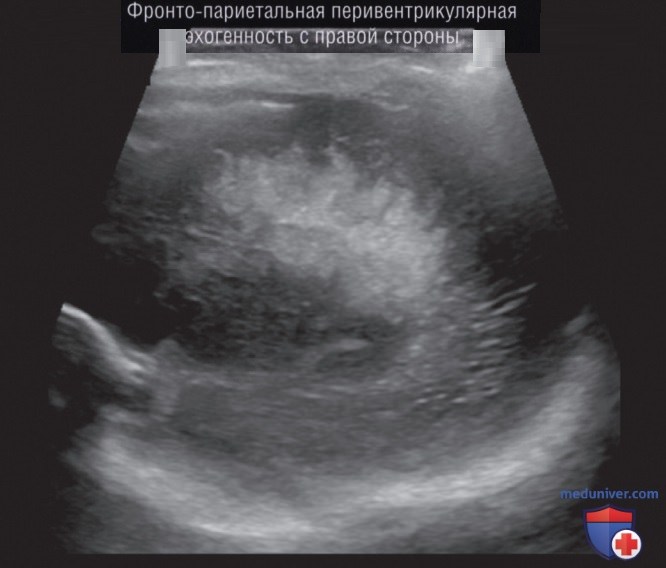
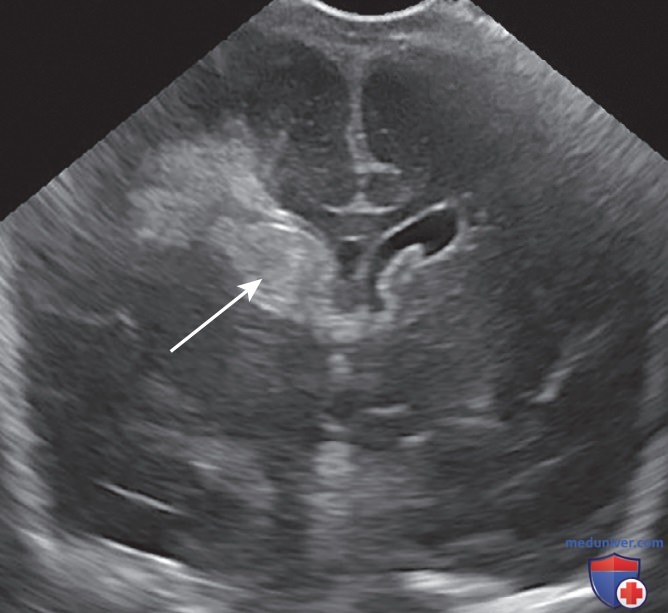
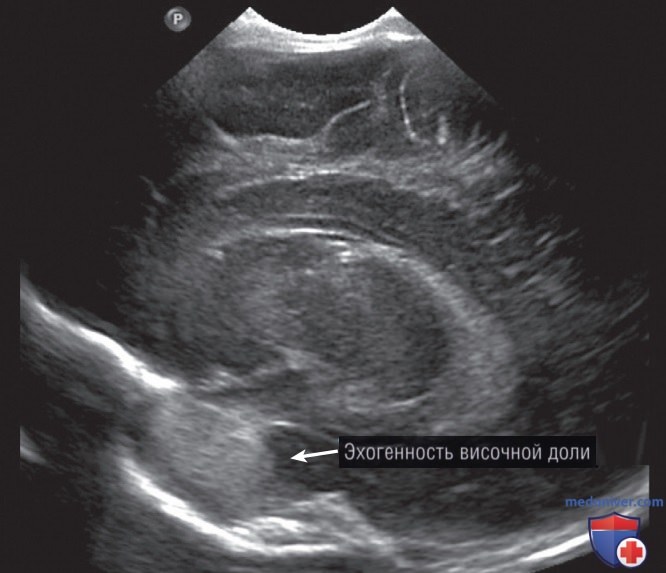
Из-за небольшого размера родничков лучше всего получать широкие изображения головного мозга, наклоняя датчик в обоих направлениях для получения сечений. Важно помнить, что визуализация ограничена клиновидным следом датчика, а поражения в теменных областях латеральнее окна визуализации можно не заметить.
е) Тонкости и ловушки:
• Пупочные катетеры:
- Идентификация кончика катетера в пупочной вене: как только будет видна часть тени катетера, слегка поверните датчик, чтобы создать самую длинную тень вдоль плоскости изображения, чтобы катетер был максимально виден. Ищите кончик катетера, приближающийся к ПП из нижней полой вены. Перемещение катетера на несколько миллиметров внутрь и наружу может обеспечить уверенность в том, что кончик был идентифицирован.
- Позиционирование датчика для верификации кончика пупочного артериального катетера (ПАК, UAC): поместите кончик катетера ПАК кзади от ПП, приблизительно на уровне Т8.
• Периферически вводимые центральные катетеры (PICC):
- Кончик может быть трудно локализовать, и, если вы не уверены в его местонахождении, потяните катетер назад, пока он не будет уверенно идентифицирован.
- Определение низкорасположенных PICC может быть затруднено из-за наличия газа в кишке; слегка повернув новорожденного влево или вправо, можно улучшить обзор.
• Эндотрахеальные трубки (ЭТТ):
- Поверните голову в одну сторону, чтобы получить доступ к верхней части груди и шеи, но избегайте слишком большого поворота, сгибания или разгибания шеи, поскольку эти движения могут сместить положение ЭТТ.
- Если вам сложно найти структуры срединной линии, поищите ствол аорты, который является наиболее видимым и значимым сосудистым ориентиром на срединной линии. Чтобы определить местонахождение киля трахеи, обратите внимание на поперечное сечение правой ЛА по малой кривизне аорты.
- Кончик ЭТТ бывает трудно определить, но осторожное перемещение ЭТТ внутрь и наружу менее чем на 5 мм помогает облегчить его идентификацию.
• УЗИ сердца:
- Измерьте максимальный и минимальный диаметры верхней полой вены (ВПВ) во время сердечного цикла и используйте среднее значение для расчета кровотока ВПВ. Низкий кровоток ВПВ связан с увеличением частоты внутрижелудочковых кровоизлияний.
- Скорость выброса при трикуспидальной недостаточности может недооценивать систолическое давление в ПЖ при отсутствии полного допплеровского параметра.
• УЗИ легких:
- У новорожденных с нарастающей дыхательной недостаточностью не следует подозревать преходящее тахипноэ новорожденного, если УЗИ легких показывает консолидацию.
- Плевральный выпот может наблюдаться у пациентов с преходящим тахипноэ новорожденных, РДС и САМ и не может использоваться для отличия данных форм заболевания.
• Неврологическое УЗИ:
- Чтобы получить изображения высокого качества, максимально сфокусируйтесь на переднем родничке. Наклон датчика, а не его скольжение является ключом к получению изображений лучшего качества.
- Чтобы не упустить важные результаты, следует выполнить множественные корональные изображения обоих полушарий головного мозга и сагиттальные сечения структур задней черепной ямки.
ж) Случай 1:
- Клиническая картина. Доношенный новорожденный поступает в ОИТ с пренатальным диагнозом «врожденная диафрагмальная грыжа». Во время реанимации ПВК был установлен без ультразвукового контроля для обеспечения длительного доступа к сосудам на фоне дыхательной недостаточности, требующей высокочастотной осцилляторной вентиляции.
- Результаты УЗИ. На рентгенограмме кончик ПВК оказался ниже диафрагмы. Однако, учитывая анатомическое искажение поддиафрагмальной сосудистой сети из-за врожденной диафрагмальной грыжи, расположение кончика катетера было неясным (рис. 26). УЗИ у постели больного было выполнено для оценки положения кончика катетера (рис. 27). Кончик ПВК визуализируется в венозном протоке.
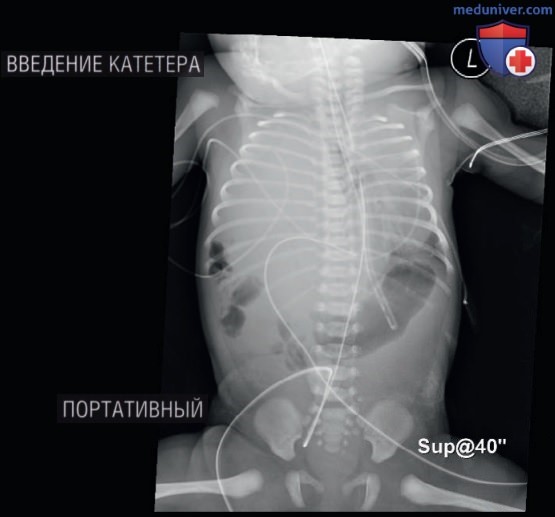
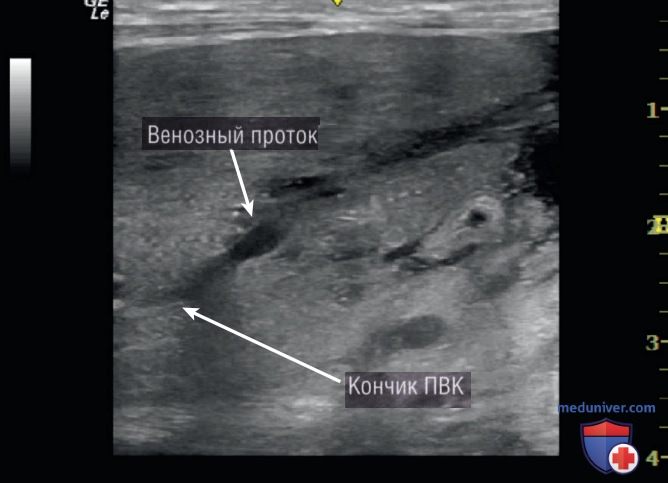
- Итоги и заключение. На основании результатов УЗИ установлено, что ПВК находится в венозном протоке, и было рекомендовано установить альтернативный ЦБК.
УЗИ у постели больного способно контролировать венозную канюляцию во время введения ЦБК и может подтвердить расположение кончиков пупочного венозного и артериального, а также периферически введенных центральных катетеров. Использование УЗИ для подтверждения нахождения кончика катетера в режиме реального времени может сократить количество попыток манипуляций, рентгенограмм после процедуры и общее время процедуры.
з) Случай 2:
- Клиническая картина. 4-месячный новорожденный переведен в кардиологическое отделение ИТ после сложной операции по поводу врожденной патологии сердца. Он находится на механической вентиляции, и на 1-й день после операции у него возникает острая дыхательная недостаточность, характеризующаяся усиленным дыханием и десатурацией кислорода. Проведено УЗИ грудной клетки.
- Результаты УЗИ. УЗИ левой половины грудной клетки демонстрирует рассеянные В-линии, а в правой половине грудной клетки определяется большой плевральный выпот с повышенной эхогенностью и плавающими частицами, указывающими на гемоторакс (рис. 28).
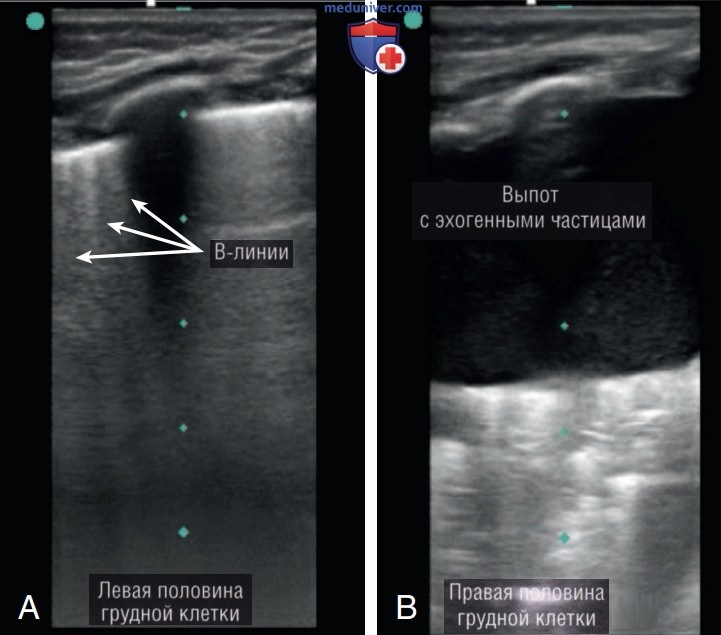
- Итоги и заключение. Для удаления гемоторакса была экстренно дренирована плевральная полость, а дыхание пациента и насыщение кислородом сразу же улучшились. Гемоторакс повторно не скапливался, и дальнейшее хирургическое вмешательство не потребовалось.
Из-за наличия хрящевой ткани в грудине и ребрах новорожденные являются идеальными пациентами для проведения УЗИ грудной клетки у постели больного, поскольку изображения могут быть получены быстро и с высоким разрешением. При ОРДС или гемодинамической нестабильности УЗИ у постели больного является идеальным инструментом для немедленного принятия клинических решений и лечения.
и) Контрольные вопросы:
1. Какая последовательность прохождения структур катетером НЕПРАВИЛЬНАЯ?
A. ПВК: пупочная вена, подвздошная вена, НПВ, а затем кавоатриальное соединение.
Б. PICC нижней конечности: БВ, подвздошная вена, НПВ, а затем кавоатриальное соединение.
B. PICC верхней конечности: плечевая вена, подмышечная вена, ПКВ, ВПВ, а затем кавоатриальное соединение.
Г. ПВК: пупочная артерия, подвздошная артерия, нисходящая аорта, грудная аорта на уровне от Т6 до Т9.
Ответ: А. Последовательностью выбора вены является: пупочная вена, левая воротная вена, венозный проток, печеночная вена, НПВ, а затем кавоатриальное соединение. Все остальные описанные выше траектории катетера верны.
2. 32-недельный новорожденный доставлен в ОИТ с развивающейся дыхательной недостаточностью. УЗИ легких демонстрирует двустороннее скольжение легких и консолидирующий процесс с небольшим плевральным выпотом в левой половине грудной клетки и рассеянными В-линиями в правой половине грудной клетки. На основании данных результатов УЗИ какое из следующих состояний является наименее вероятным?
A. Пневмония.
Б. ПТН.
B. САМ.
Г. РДС.
Ответ: Б. Преходящее тахипноэ новорожденного является наименее вероятным при наличии консолидирующего процесса. Пневмония, САМ и РДС могут проявляться консолидацией. Однако следует подчеркнуть, что УЗИ легких необходимо трактовать с учетом клинической ситуации. Гестационный возраст, лабораторные исследования матери, родовспоможение и тяжесть поражения легких являются некоторыми факторами, которые следует учитывать при принятии диагностических решений относительно основных патофизиологических процессов, влияющих на легкие. Кроме того, важно отметить, что пневмоторакс можно исключить, визуализировав двустороннее скольжение легких.
3. Доношенный новорожденный поступил в ОИТ сразу после рождения с тяжелой гипоксической дыхательной недостаточностью. Его мать не получала дородовой помощи и была доставлена в родильное отделение на активной стадии родов. Биофизический профиль, выполненный при поступлении, выявил выраженный олиго-гидрамнион. Физикальное обследование младенца подтвердило синдром Поттера. Из-за системной гипотензии и обострения гипоксемии провели УЗИ сердца у постели больного при клиническом подозрении на стойкую легочную гипертензию и легочную гипоплазию. Какой из следующих методов является предпочтительным для оценки систолического давления в ЛА с помощью эхокардиографии?
A. Измерение максимальной скорости регургитации при трикуспидальной недостаточности.
Б. Измерение времени ускорения в ЛА.
B. Оценка направления трансдуктального шунта.
Г. Оценка положения стенки межжелудочковой перегородки.
Ответ: А. При наличии трикуспидальной недостаточности с полным допплеровским параметром измерение максимальной скорости регургитации является наиболее точным количественным методом для оценки систолического давления в легочной артерии с использованием следующего уравнения:
СДПЖ или PASP = давление RA + + [4 х (максимальная скорость регургитации при трикуспидальной недостаточности)2].
4. Вас вызывают к постели доношенного новорожденного, который второй день на вено-венозной ЭКМО из-за стойкой легочной гипертензии. У младенца недавно развились системная гипотензия и анасарка, которые значительно усилились за последние 4 ч. Вы выполняете УЗИ сердца в условиях стационара, чтобы исключить перикардиальный выпот. Какая из следующих позиций является рекомендуемой начальной кардиальной позицией, чтобы быстро исключить перикардиальный выпот?
A. Парастернальная позиция подлинной оси.
Б. Апикальная 4-камерная позиция.
B. Субкостальная позиция.
Г. Парастернальная позиция по короткой оси.
Ответ: В. Рекомендуемая позиция для быстрого исключения перикардиального выпота — субкостальная. Данная позиция показывает нижнюю и заднюю части полости перикардиа, где наиболее вероятно скопление зависимой жидкости. Выпот в перикарде выявляется в виде анэхогенной полосы между печенью и свободной стенкой ПЖ в ближнем поле экрана.
5. Вас вызывают к постели 2-дневного 24-недельного новорожденного, которому требуется повышение FiO2 для поддержания сатурации кислорода на уровне 85%. Газовый анализ артериальной крови показывает нарастание метаболического ацидоза. Вы решаете провести УЗИ головы у постели больного (рис. 29). Какой диагноз является наиболее вероятным на данном ультразвуковом изображении?
A. Правостороннее субдуральное кровоизлияние.
Б. Левостороннее субдуральное кровоизлияние.
B. Правостороннее внутрижелудочковое кровоизлияние.
Г. Левостороннее внутрижелудочковое кровоизлияние.
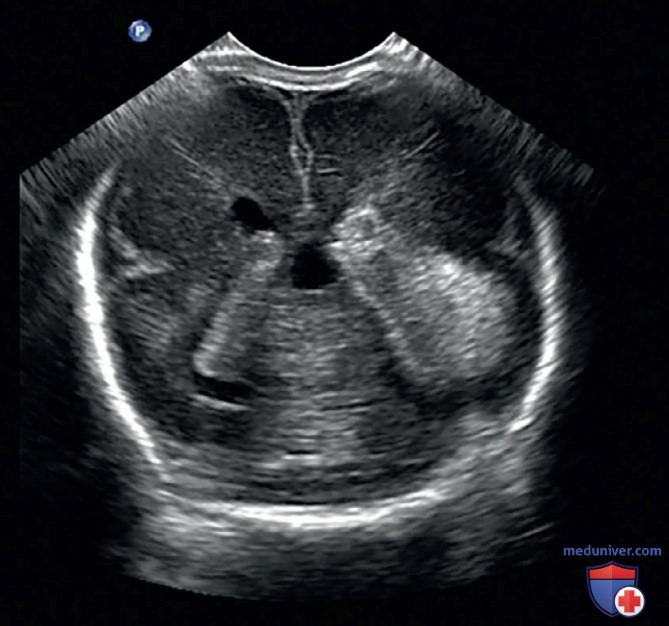
Ответ: Г. На этом изображении головного мозга в корональном сечении (см. рис. 29) показано большое внутрижелудочковое кровоизлияние (степень IV) в левом боковом желудочке, которое распространяется в паренхиму левой теменной доли. Нет никаких ультразвуковых признаков право-или левостороннего субдурального либо правостороннего внутрижелудочкового кровоизлияния.
- Рекомендуем ознакомиться далее "Программы обучения УЗИ point-of-care в США"
Редактор: Искандер Милевски. Дата публикации: 15.2.2024

