Коррекция генетического заболевания. Нейтральные стволовые клетки
Несмотря на то что коррекция генетического заболевания на уровне генома остается наиболее оптимальным и предпочтительным терапевтическим методом, мРНК также является перспективным вектором (возможно даже более доступным) для блокировки доминантного негативного гена. С целью ингибирования трансляции и/или повышения деградации мРНК уже давно используются белковые молекулы с антисенсовыми олигонуклеотидными или полными последовательностями, блокирующими связывание мРНК с биосинтетическим аппаратом клетки.
Кроме того, двуцепочечная РНК индуцирует стремительную деградацию мРНК, механизм которой остается до конца не выясненным (Jen, Gewirtz, 2000). Однако маловероятно, что одно лишь устранение мРНК, транскрибированных с мутантного аллеля с короткими или единичными мутациями, будет способствовать экспрессии мРНК нормального аллеля. Альтернативу представляет использование рибозинов hammerhead и hairpin, обладающих способностью связываться с высокоспецифическими участками мРНК с последующей индукцией их расщепления и инактивации в процессе трансляции.
В настоящее время изучается возможность применения данного метода в терапии патологического остеогенеза (Dawson, Marini, 2000). Независимо от того что именно является мишенью — геномные или цитоплазматические элементы, успех новых технологий генной терапии будет определяться эффективностью включения реагентов в стромальные клетки костного мозга ех vivo, оптимального выбора специфического вектора и стабильной способности мезенхимальных стволовых клеток экспрессировать нужные факторы in vivo (Bianco et al., 2001).
Таким образом, открытие мезенхимальных стволовых клеток с их неожиданными свойствами создает новую концептуальную схему развития клеточных линий. Однако для понимания биологической роли стромальных стволовых клеток, их природы, способности к трансдифференцировке или дедифференцировке, их физиологического значения в процессе эмбрионального развития, постнатального роста, созревания и старения, а также при заболеваниях человека необходимы дальнейшие междисциплинарные исследования.
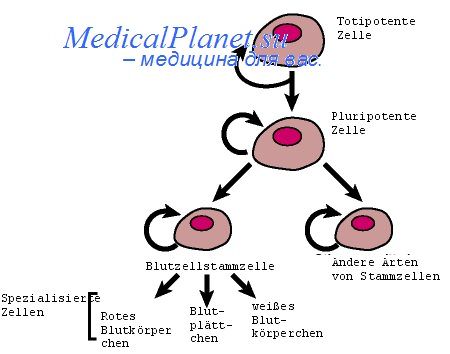
Нейтральные стволовые клетки
Экспериментальные доказательства возможности регенерации клеток ЦНС были получены значительно раньше открытия эмбриональных стволовых клеток в исследованиях, показавших наличие в неокортексе, гиппокампе и обонятельных луковицах головного мозга взрослых крыс клеток, захватывающих Н-тимидин, то есть, способных к синтезу белка и делению (Altman, 1962, 1963).
Еще в 60-е годы прошедшего столетия допускалось, что эти клетки являются предшественниками нейронов и принимают непосредственное участие в процессах обучения и памяти (Altman, Das, 1965). Чуть позже было выявлено наличие синапсов на образованных de novo нейронах (Kaplan, 1981, 1985) и появились первые работы об использовании эмбриональных стволовых клеток с целью индукции нейроногенеза in vitro (Wobus et al., 1984).
В конце XX века эксперименты с направленной дифференцировкой ЭСК в нейральные клетки-предшественники (McBurney et al., 1988; Brustle, 1999), дофаминергические и серотонинергические нейроны (Lee et al., 2000) привели к пересмотру классических представлений о способности нервных клеток млекопитающих к регенерации (Eriksson et al., 1998; Luskin, 1998; Eisch et al., 2000). Результаты многочисленных исследований убедительно доказали как реальность перестроек нейрональных сетей, так и наличие нейроногенеза на протяжении всего периода постнатальной жизни организма млекопитающих (Викторов, 2002).
Установлено, что нейральные стволовые клетки экснрессируют глиальный кислый фибриллярный белок, который среди зрелых клеток нейральной линии сохраняется только на астроцитах. Следовательно, стволовым резервом в зрелой ЦНС могут быть астроцитарные клетки. Действительно, в обонятельных луковицах и зубчатой извилине были выявлены нейроны, происходящие из GFAP-позитивных предшественников, что противоречит традиционным представлениям о прогениторнои роли радиальной глии, не экспрессирующей GFAP в зубчатой извилине в зрелом возрасте. Не исключено, что в ЦНС существуют две популяции стволовых клеток (Doetsch et al., 1999; Seri, 2001).
- Читать далее "Стволовой резерв нервной системы. Нейральные стволовые клетки эмбриона"
Оглавление темы "Нейральные стволовые клетки":1. Дифференцировка прогениторных клеток. Стволовые свойства культурных клеток
2. Определение потенциала дифференцировки стволовых клеток. Системная трансплантация стволовых клеток
3. Доставка стволовых клеток в ткани. Генная инженерия клеток
4. Лечение рецессивных заболеваний. Преобразованные стволовые клетки
5. Коррекция генетического заболевания. Нейтральные стволовые клетки
6. Стволовой резерв нервной системы. Нейральные стволовые клетки эмбриона
7. Маркеры нейральных стволовых клеток. Дифференциация стволовых клеток нервной системы
8. Регенерация центральной нервной системы. Трансплантация нейральных стволовых клеток
9. Культура нейральных стволовых клеток. Приживление нейральных стволовых клеток у разных видов
10. Ксенотрансплантация нейральных стволовых клеток. Получение нейральных стволовых клеток

