Место прикрепления вирусной ДНК к ДНК клетки. Места интеграции вирусного генома SV40
Chow е. а. (1975) разработали методический прием, который был основан на том, что при высокой множественности заражения в условиях литической инфекции ДНК вируса SV 40 интегрировал с ДНК клетки, после чего вырезался и при этой процедуре нередко включал в свой состав фрагмент клеточной ДНК. При этом в месте включения ДНК клетки образовывались гетеродуплексы с петлей, расположение которых устанавливалось с помощью электронного микроскопа.
В случае определенного места интеграции в молекуле вирусной ДНК петли должны были иметь постоянную локализацию. Полученные данные свидетельствовали о полуспецифическом характере при продуктивной инфекции мест прикрепления, которые выявлялись в зоне 0,205—0,312 ед. физической карты (за точку нуль принимался разрыв рестриктазой EcoR 1, которая разрезала кольцевую молекулу ДНК вируса SV 40 в одном строго определенном месте генома вируса SV40).
Авторы предполагают, что существует несколько мест прикрепления, которые соответствуют точкам 0,205; 0,248; 0,312 и, вероятно, 0,59. Предполагается, что только при такой локализации вирусной ДНК синтезируется Т-антиген и проявляется трансформированный фенотип клетки. Вместе с тем Hwang и Kucherlapati (1980) выявили четыре независимых места интеграции последовательностей генома SV40 в трансформированных фибробластах человека, три из которых локализованы в пятой хромосоме человека.
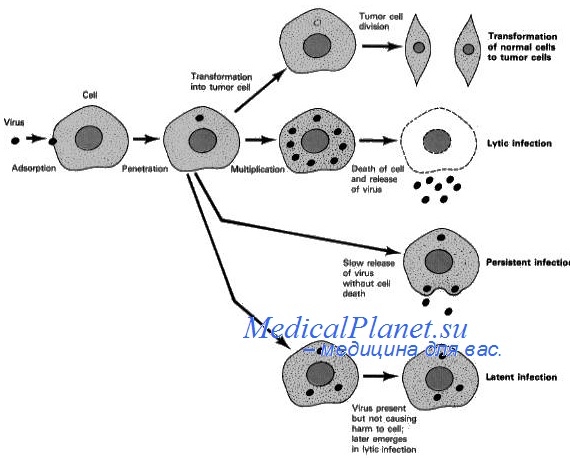
Интегрированные вирусные последовательности перемежаются с клеточными участками. Использование одновременной рестрикции разными ферментами показало, что последовательности, находящиеся внутри вирусного генома, различаются в каждом случае. Какая-либо специфичность интеграции генома SV 40 в клетках человека отсутствует. В клетках крыс и хомяков обнаружено от одного до пяти мест интеграции SV 40 (Chepelinsky с. а., 1980). В приведенных выше работах определялся механизм интеграции вирусной ДНК. Вслед за инфицированием мышиных клеток наблюдался синтез длинных тандемио соединенных «голова-хвост» молекул вирусной ДНК, что происходило в условиях репликации вирусной ДНК.
С использованием физических методов идентификации вирусных геномов установлена активная рекомбинация между полимерами. Это является основанием для предположения об их отношении к пулу предшественников форм интеграции. В ряде лабораторий предпринимаются дальнейшие эксперименты для подтверждения данной гипотезы.
- Читать далее "Копии вируса в геноме клетки. Геном саркомы Рауса"
Оглавление темы "Вирусная теория происхождения опухолей":1. Онкогенные вирусы. Молекулярно-биологические механизмы вирусного онкогенеза
2. ДНК-провирус. Интеграция вирусного генома
3. Теория протовируса. Изначальная интеграция генома вирусов
4. Геном эндогенного вируса как причина рака. Взаимодействие вирусного генома с геномом клетки
5. Варианты интеграции вирусного генома. Экспрессия интегрированных вирусных ДНК-копий
6. Место прикрепления вирусной ДНК к ДНК клетки. Места интеграции вирусного генома SV40
7. Копии вируса в геноме клетки. Геном саркомы Рауса
8. Переход вирусного генома в клеточный геном. Паповавирусы
9. Строение полиомавирусов. Геном паповавирусов
10. Ген А — онкоген полиомавирусов. Функции гена А паповавирусов

