Кишечные причины гнойного воспаления. Этапы гнойного воспаления
Любые неблагоприятные воздействия на желудочно-кишечный тракт (раздражающие или повреждающие агенты, инфекция и др.) могут привести к нарушению экосистемы и колонизации патогенной микрофлорой. Кроме того, хорошо известно влияние антибиотиков на микроэкологический статус. К нарушению колонизационной резистентности могут привести наркологические, местноанестезирующие вещества, обволакивающие, абсорбирующие, слабительные, отхаркивающие, желчегонные и другие средства, изменяющие моторику и образование муцина.
Некоторые психотропные препараты, соли тяжелых металлов, некоторые антигистаминные средства, вещества, содержащие эфирные масла, различные иммуномоду-лирующие агенты способны ингибировать рост нормальной микрофлоры или нарушать взаимоотношения хозяина и его микрофлоры и, следовательно, колонизационную резистентность.
В хирургической практике большое значение имеют циркуляторные нарушения в тонкой кишке, создающие условия для вегетации анаэробных бактерий (патогенных и условно-патогенных), перемещающихся из дистальных отделов толстой кишки.
Таким образом, хирургическая инфекция может быть вызвана не только экзогенной микрофлорой, но и аутомикрофло-рой, распространяющейся из внутренних регионов их естественного обитания гематогенным или лимфогенным путем. Однако в литературе чрезвычайно мало уделяется внимания характеристике течения воспалительного процесса в зависимости от способа контаминации.
По общему признанию, универсальной схемой (этапами) инфекционного процесса являются: 1) взаимодействие инфекционного агента с эпителием соответствующих экологических ниш; 2) преодоление клеточных и гуморальных механизмов защиты макроорганизма, чему способствуют метаболические особенности, обеспечивающие размножение возбудителей в организме хозяина; 3) токсические воздействия.
В основе всех факторов патогенности микроорганизмов лежат одни и те же принципиальные закономерности: активные молекулы-лиган-ды, синтезируемые возбудителем, способны узнавать комплементарные структуры макроорганизма и связываться с ними в рецепторе, что далее ведет к каскаду патофизиологических реакций, нарушающих функцию клеток и тканей организма хозяина.
Для хирургических инфекций, вызванных условно-патогенными микробами, характерно прежде всего наличие первичного гнойного очага, который является продуцентом субстанций, определяющих возникновение, течение и исход инфекции. Механизм формирования первичного гнойного очага представляется следующим образом. В течение фиксации микроб находится в лаг-фазе, продолжительность которой не более 2—4 ч.
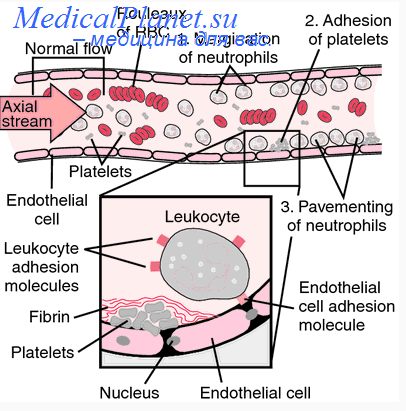
Однако через несколько минут инфект можно обнаружить в печени, селезенке и крови. К месту фиксации микроорганизма начинается миграция нейтрофилов, максимум которой достигается через 3—8 ч. Несмотря на миграцию неитрофилов, количество микроорганизмов в очаге увеличивается в 50 раз через 7 ч, при внутрибрюшном заражении за это время концентрация микроорганизмов увеличивается на 1—2 порядка.
При недостаточности элиминации и киллинга возбудителя в первые 1—8 ч после заражения наблюдается резкое увеличение концентрации микробов в первичном очаге. Любой способ элиминации микроба из места его фиксации в этом решающем периоде является благоприятным, так как оптимизирует соотношение микроб/фагоцит. Известно, что оптимальное соотношение числа фагоцитирующих нейтрофилов с количеством микробных клеток равно 1:10, при котором происходит лизис бактерий в 95 %.
Примерно через 6—7 ч развивается окклюзия кровеносных сосудов, которая является частью защитного механизма против генерализации инфекции, через 6—8 ч формируется абсцесс. К началу формирования абсцесса подавляется миграция нейтрофилов в его центре вследствие нарушения микроциркуляции и снижения хемотаксиса факторами вирулентности микробов. Если, наоборот, происходит усиление миграции нейтрофилов в очаг, то инфекционный процесс может приобрести злокачественный характер за счет гиперстимуляции большой массы фагоцитов.
С другой стороны, причиной прогрессирования гнойной инфекции может стать превышение числа микробов (или их антифагоцитарной активности) над числом фагоцитов (или их антибактериальной активности)].
При повышении уровня антигенов и токсинов над инактивирующей способностью фагоцита наступает гиперстимуляция последнего. Образующиеся при этом токсичные продукты метаболизма фагоцита (микробицидные факторы: реактивные метаболиты кислорода, ферменты) усугубляют микробное повреждение тканей первичного очага, что еще более облегчает размножение возбудителя.
По достижении концентрацией микроба в первичном очаге критического уровня местные факторы защиты уже не в состоянии удержать выход продуктов очага за его пределы, что приводит к внутрисосудистой активации крови и, возможно, к генерализации инфекционного процесса.
- Читать далее "Гнойный очаг. Характеристика воспаления в гнойном очаге"
Оглавление темы "Особенности иммунитета при гнойной инфекции":1. Причины гнойной инфекции. Инфекционное воспаление
2. Кишечные причины гнойного воспаления. Этапы гнойного воспаления
3. Гнойный очаг. Характеристика воспаления в гнойном очаге
4. Иммунитет при гнойном воспалении. Интерфероны при гнойной инфекции
5. Фагоцитоз при гнойном воспалении. Гуморальный иммунитет гнойного воспаления
6. Детский иммунитет. Роль гуморального имунитета в воспалении у детей
7. Значение иммуноглобулинов в развитии гнойных болезней. Нарушения Т-иммунитета
8. Эндотоксины и эндотоксикоз. Факторы детоксикации организма
9. Виды бактериальных антигенов. Токсины грамотрицательных бактерий
10. Токсины острой фазы воспаления. Молекулы средней массы гнойного воспаления

