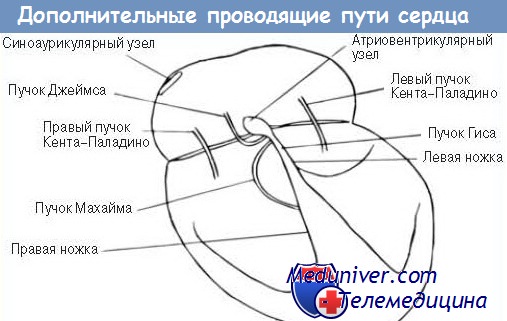
Дополнительные проводящие пути сердца. Топография пучков Кента
Длительное время анатомическая основа синдромов предвозбуждения до конца не была выяснена. Сегодня нет смысла в хронологическом порядке рассматривать результаты этих поисков и существующих споров, так как не только морфологическими и физиологическими исследованиями, но и путем хирургической деструкции при радикальном лечении синдрома ВПУ доказано существование ДПП. Хотя клинические и электрофизиологические работы преобладают над морфологическими, уже известно более 40 исследований, касающихся анатомического субстрата синдрома предвозбуждения (Frank и др., 1976; Becker и др., 1978; Wolferth, Wood и др., 1942; Dhnell, 1944; Anderson и др., 1971, 1972 и др.).
Обширный обзор и анализ патологических находок, по данным многочисленных источников, приводят в своей монографии Sherf и Neuman (1978). Весьма интересными и важными являются при этом клинико-патологические сопоставления (Becker, 1978; Klein и др., 1980; Rossi, 1980; Brechenmacher и др., 1980), т. е. когда прижизненно доказано наличие синдрома ВПУ.
Большинство работ посвящено изучению пучков типа Кента. Хотя до сих пор выясняется, какие мышечные связи описал Кент в правой стенке сердца между предсердием и желудочком — пучок или только узловидные массы специализированной ткани (последние нашли и в некоторых нормальных сердцах Anderson и др.), однако нет сомнения, что его имя связано с обоснованием субстрата дополнительного проведения возбуждения через АВ соединение.
В большинстве случаев дополнительные проводящие пути состоят полностью из мышечных волокон, т. е. рабочего миокарда. Исключение составляют синоатри-альные клетки типа Р или миокардиальные несколько атипичные клетки, не соответствующие структуре специализированной проводящей ткани (James; Lev; Anderson и др.). Недавно стало известно даже о непосредственном гистологическом подтверждении ДПП на материале биопсии, взятом во время операции у больного с синдромом ВПУ (Untereker и др.).
Выяснение анатомического субстрата синдрома ВПУ является одним из доказательств того, что его наличие вызвано пороком развития. По данным экспериментальной эмбриологии, образование ДПП тесно связано с периодом формирования АВ фиброзных колец. Тrueх и др. в сердцах зародышей и новорожденных в возрасте менее 6 мес нашли многочисленные дополнительные связи в отверстиях и щелях фиброзного кольца. В раннем периоде развития зародыша миокард предсердия сохраняет единство в АВ канале с желудочками. В процессе дальнейшего развития в АВ кольцах могут сохраниться мышечные волокна как результат порока облитерации отверстий в кольце, позволяя, таким образом, одному или нескольким мышечным пучкам проходить в области АВ кольца.
Anderson с соавт. и Gerlis с соавт. указывают, что специализированная проводящая ткань также развивается из миогенных тканей и приобретает свойства проводимости позднее. Модальные структуры, начинающиеся в миокарде АВ канала зародыша и в дальнейшем имеющие возможность менять свою функцию, позволяют предполагать, что и остатки мышечной ткани, находящейся в непосредственной близости к фиброзным кольцам, которые также первоначально происходят из мышечного канала, смогут проводить импульсы и стать, таким образом, трактами, обходящими АВ узел. Допускается, что при нормальном развитии сердца все дополнительные мышечные соединения резорбируются.
Концепция эмбриологической этиологии предвозбуждения как дефекта развития подтверждается фактом семейной наследственности синдрома предвозбуждения (сборные данные такого рода приведены в монографии Ferrer).
По данным литературы, дополнительные проводящие пути типа пучка Кента имеют в среднем 1 мм в диаметре. Минимальный размер — 0,1 мм; лишь в наблюдении Lev при аномалии Эбштейна пучок Кента имел ширину 20 мм. Длина ДПП — от 2 до 10 мм (Becker и др., 1978; Boineau и др.). Целый ряд исследователей на аутопсии находили множественные пучки в разной комбинации, причем было отмечено, что они могут находиться в непосредственной близости друг к другу. В частности, Klein и, др. обнаружили три левосторонних пучка на протяжении 2 см. Anderson и др.предложили расширенную классификацию анатомических субстратов предвозбуждения; она не включает спорных эпонимов, а также терминов, предложенных Rossi.
Для выполнения операции разделения ДПП необходимо прецизиозно знать все возможные их топографо-анатомические соотношения с другими структурами сердца. Следует учесть, что такие центральные структуры сердца, как АВ узел, пучок Гиса, центральное фиброзное тело, фиброзные треугольники, верхний отдел межжелудочковой перегородки, нижняя часть межпредсердной перегородки находятся на расстоянии нескольких миллиметров друг от друга, а ДПП — в непосредственной близости к этим образованиям или (как например, пучки Джеймса, Махейма) имеют прямой контакт со специализированной проводящей системой.
- Читать далее "Классификация пучков Кента. Правосторонние и левосторонние дополнительные проводящие пути"
Оглавление темы "Дополнительные проводящие пути сердца - как причина аритмий":- Атрио-вентрикулярное соединение. Проводящие пути АВ узла и его строение
- Дополнительные проводящие пути сердца. Топография пучков Кента
- Классификация пучков Кента. Правосторонние и левосторонние дополнительные проводящие пути
- Септальные дополнительные проводящие пути сердца. Топография межжелудочковой перегородки сердца
- Трехстеночная щель сердца. Фиброзное кольцо и фиброзные треугольники сердца
- Синдром укороченного интервала Р—R (Lown—Ganong—Levine). Предвозбуждение типа Махейма
- Электрофизиологические исследования (ЭФИ) сердца. Чреспищеводное и интракардиальное электрофизиологическое исследование сердца
- Электростимуляция сердца при исследовании. Показатели ЭФИ сердца
- Оценка синоатриального узла и предсердий. Вызов и прекращение тахикардии
- Варианты ри-энтри тахикардий. Предсердная эктопическая тахикардия

