Устойчивость к внутрибрюшинному перитониту. Неадекватность экспериментального перитонита
Серии экспериментов были направлены на то, чтобы выявить механизмы повышенной устойчивости морских свинок к внутрибрюшному заражению. Животных вначале иммунизировали каловой взвесью 100 мг в полном адъюванте Фрейнда, затем через 2 нед внутрибрюшинно вводили 2 мл 15% каловой взвеси. Через 2 нед у выживших свинок брали кровь для получения сыворотки и брали клеточную взвесь селезенок.
Сыворотку получали путем центрифугирования гепаринизированной крови, а клеточную взвесь — путем протирания ткани селезенки через капроновую сетку в жидкость Хенкса, в которую добавляли 5% аутогенной сыворотки и гепарин.
Затем воспроизводили перитонит у мышей. Для этого белым мышам обоего пола массой 30—35 г внутрибрюшинно вводили 0,1 мл 15% взвеси кала морских свинок. Одновременно первой группе животных (15 мышей) внутрибрюшинно вводили 0,1 мл изотонического солевого раствора, второй группе (15 мышей) —по 0,1 мл сыворотки переболевших морских свинок; третьей группе (15 мышей) — по 0,1 мл взвеси клеток селезенки переболевших морских свинок.
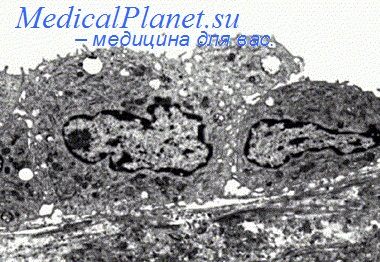
Падеж мышей 1-й группы начался через 2 ч после внутрибрюшного заражения, к концу 1-х суток все животные этой группы погибли. Во 2-й группе к концу 2-х суток были живы 2 мыши, а в 3-й группе к концу 3-х суток выжило 6 мышей. Таким образом, эти опыты подтверждают роль клеточных механизмов защиты, в частности роль СФМ при разлитом перитоните.
В то же время они указывают пути для разработки способов рациональной терапии этого заболевания. Оценивая роль СФМ в защите организма при перитонеальной инфекции, важно подчеркнуть реакцию большого сальника, в котором, согласно W. Т. Daems (1980), имеются скопления макрофагов «млечные» пятна, относящиеся к СФМ. При перитоните, в частности, при экспериментальном воспалении брюшины у морских свинок, крыс и мышей уже к концу 1-х суток сальник формирует мешковидные образования, в просвете которых видны скопления каловой взвеси. Позднее здесь образуются осумкованные гнойники, при этом сальник резко уменьшается в размерах за счет склеивания соприкасающихся поверхностей, образования: сборок и дубликатур, а затем склерозируется. Следует также отметить, что у животных введенная каловая взвесь, как правило, концентрируется в поддиафрагмальной зоне, особенно между печенью и диафрагмой.
Оценивая экспериментальный перитонит, следует упомянуть точку зрения хирургов о неадекватности его моделей перитониту у человека [Попов В. А., 1985]. Эта точка зрения, по-видимому, основана на субъективной трактовке понятия модель патологического процесса. Совершенно очевидно, что биологические модели большинства патологических процессов человека условны и отражают лишь отдельные стороны болезни.
В этом плане модель перитонита с введением в брюшную полость каловой взвеси не составляет исключения. Однако она позволяет воспроизвести стандартную распространенную воспалительную реакцию брюшины и свойственные такой форме инфекционного процесса интоксикацию и нарушения гомеостаза. Перфорация кишечника, создание странгуляционной непроходимости для моделирования перитонита по нашим данным дают большую вариабельность результатов. В то же время модель разлитого калового перитонита позволяет изучать такие стороны этого процесса у людей как нарушения иммунной защиты и неспецифической резистентности, структурные механизмы повреждения детоксицирующей макрофагальной, сердечнососудистой, дыхательной, выделительной и особенно периферической нервной систем, отрабатывать методы коррекции нарушений гомеостаза с использованием сорбентов и иммунозаместительной терапии.
Следует также подчеркнуть, что в отличие от данных К. С. Симоняна (1971) нам удалось получить у крыс разлитой гнойно-фибринозный перитонит путем введения каловой взвеси без предварительного воспроизведения деструктивного процесса. В то же время эти результаты не противоречат положению указанного автора о значении иммунной реактивности в развертывании последовательных стадий воспалительного процесса. Следует также указать, что при распространенном перитоните, особенно при быстром поступлении инфекта в брюшную полость в первый период преобладают процессы альтерации, которые включают в частности массивный выброс биологически активных веществ с соответствующей общей реакцией организма.
Эта стадия такая же закономерная стадия воспаления, как и последующая экссудативная, что не всегда учитывается клиническими специалистами. Эта закономерность прослежена нами и при обширных инфицированных ранах в эксперименте, в которых вначале преобладают процессы альтерации и нарушения кровообращения («сухая рана») и лишь после начала лечения проявляются признаки фазы экссудации.
- Читать далее "Ультразвук в лечении перитонита. Применение ультразвуковых волн для лечения гнойной инфекции"
Оглавление темы "Особенности и лечение перитонита":1. Мезотелий при каловом перитоните. Эксудация при каловом перитоните
2. Отложение фибрина при перитоните. Морфология фибринозных пленок
3. Внутренние органы при перитоните. Брюшина при каловом перитоните
4. Миокард при перитоните. Микроциркуляция при перитоните
5. Токсико-инфекционный шок при перитоните. Клетки крови при перитоните
6. Нарушения моторики кишечника при перитоните. Функции макрофагов при перитоните
7. Регуляция гомеостаза при перитоните. Значение фагоцитоза при перитоните
8. Устойчивость к внутрибрюшинному перитониту. Неадекватность экспериментального перитонита
9. Ультразвук в лечении перитонита. Применение ультразвуковых волн для лечения гнойной инфекции
10. Ультразвуковые инструменты. Эффективность ультразвука в хирургии

