Лечение ИВЛ-ассоциированной пневмонии. Препараты
Ни решение о начале антибиотикотерапии, ни выбор препарата не требует интерпретации результатов посева, так как эта информация не будет доступна ранее, чем через 48-72 часа. Решение скорее принимается на основании клинических подозрений и микроскопии окрашенной по Граму мокроты. Более того, выбор препарата основывается на индивидуальных факторах риска полирезистентной инфекции и профиле антибиограмм данного учреждения. От антимикробной терапии можно безопасно воздержаться, если
1) окраска по Граму не выявляет микроорганизмов и
2) пациент не имеет признаков тяжелого сепсиса.
Клинические признаки инфекции с отрицательным результатом окраски мокроты по Граму указывают либо на внелегочный источник инфекции, либо на стерильное воспаление.
Пациенты, у которых при окраске по Граму выявлены микроорганизмы, или имеющие клиническую нестабильность, должны получать эмпирическое лечение по поводу ИВЛ-ассоциированой пневмонии впредь до получения результатов посева. Особую важность имеет назначение «адекватной терапии», определяемой, как воздействие одним антимикробным агентом, к которому патоген чувствителен, в правильной дозе, правильным способом и своевременно.
Второй ключевой аспект лечения ИВЛ-ассоциированой пневмонии включает последовательные переоценки и интерпретации первоначальной микробиологии, так чтобы: 1) лечение можно было прекратить, если ничего не высеялось и не наступило клинического ухудшения; 2) лечение можно было сократить, воздействуя только на специфический этиологический патоген; и 3) в перспективе можно было определить конечную точку терапии и следовать к ней.
Увеличение смертности, связанное с неадекватной первоначальной антимикробной терапией ИВЛ-ассоциированой пневмонии детализируют достаточное количество данных. Iregui et al. показали, что задержка лечения (определяемая как первоначальное назначение антибиотика более чем через 24 часа после выявления диагностических критериев ИВЛ-ассоциированой пневмонии) сопровождается увеличением смертности (ОШ 7,68; 95% ДИ 4,50-13,09).
Подобным образом, Kollef et al. сообщили, что неадекватная первоначальная антибиотикотерапия грамотрицательных инфекций является фактором риска для смертности (ОШ 4,22; 95% ДИ 3,57-4,98). Alvarez-Lerma et al. продемонстрировали, что приписываемая ИАП смертность была ниже среди пациентов, которые получали соответствующую первоначальную антибиотикотерапию (16,2% против 24,7%; р=0,03).
Выбор первоначальной антибиотикотерапии зависит не только от факторов риска пациента, но и от местных (в идеале, для конкретного отделения) микробиологических данных, что увеличивает вероятность того, что будет предписана соответствующая антимикробная терапия. В общем, лечение пациентов, имеющих риск развития полирезистентной инфекции, должно обеспечивать воздействие против метициллин-резистентного золотистого стафилококка, P. aeruginosa, Acinetobacter spp. и вырабатывающей БЛРС Klebsiella spp.
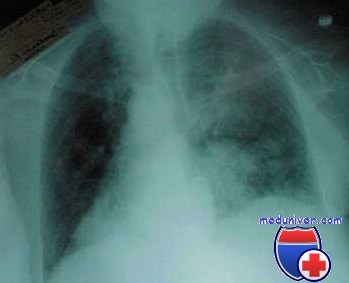
Обычно требуется не менее двух лекарств, одного, эффективного против метициллин-резистентного золотистого стафилококка (например, ванкомицин, линезолид), и одного, эффективного против полирезистентных грамотрицательных палочек, особенно P. aeruginosa (например, пиперациллин-тазобактам, меропенем). Пациентов с рано развившейся ИВЛ-ассоциированной пневмонии при отсутствии вышеупомянутых факторов риска можно лечить препаратами узкого спектра действия.
Первоначальная антибиотикотерапия по поводу ИВЛ-ассоциированной пневмонии должна проводиться парентерально. Энтеральное лечение можно выбрать, если пациенты адекватно отвечают на внутривенную терапию, работа желудочно-кишечного тракта нормальна и пероральные антибиотики имеют равную биодоступность. Использование аэрозольного аминогликозида в качестве дополнения ликвидирует бактерии, но не влияет на смертность.
Неадекватная дозировка антибиотиков приводит к появлению полирезистентных бактерий и связана с худшими исходами ИВЛ-ассоциированной пневмонии. Для достижения нужного лечебного эффекта необходима адекватная первоначальная дозировка ванкомицина (15 мг/кг каждые 12 часов), аминогликозидов (гентамицин, тобрамицин 7 мг/кг в день; амикацин 20 мг/кг в день) и фторхинолонов (левофлоксацин 750 мг в день, ципрофлоксацин 400 мг каждые 8 часов) (при нормальной функции почек).
Связь между использованием фторхинолона и возникновением ИВЛ-ассоциированной пневмонии, вызванной полирезистентными патогенами, в особенности Pseudomonas и метициллин-ре-зистентным золотистым стафилококком была подтверждена на обширном фактическом материале. Применение фторхинолона в лечении ИВЛ-ассоциированной пневмонии должно быть благоразумным, основанным на регулярном обновлении характерных для данного отделения антибиограмм.
Тогда как для пациентов с подозрением на ИВЛ-ассоциированную пневмонию необходима эмпирическая терапия несколькими препаратами, пока не будут доступны результаты посевов, комбинированное воздействие на конкретного патогена (например, «двойное покрытие» Pseudomonas) вряд ли приведет к успеху и может ухудшить исход. Ни in vitro, ни in vivo не было показано синергии при такой комбинированной терапии.
Мета-анализ всех исследований сравнения монотерапии бета-лактамом и комбинированной терапии бета-лактамом-аминогликозидом у иммунокомпетентных пациентов с сепсисом, включавший 64 исследования и 7586 пациентов, не обнаружил различия ни в смертности, ни в развитии устойчивости.157 Клиническая неудача гораздо чаще связана с комбинированным лечением.
Задачей эмпирической терапии является введение сочетания антибиотиков, вероятно покрывающего все патогены, с последующей настройкой терапии, по возможности. Таким образом, идеальная терапия при подозрении на ИВЛ-ассоциированную пневмонию включает начальный период хорошей чувствительности, за которым следует период хорошей чувствительности, основанный на микробиологических результатах.
То есть, ни один пациент с ИВЛ-ассоциированной пневмонии не остается нелеченным, и ни одному пациенту без ИВЛ-ассоциированной пневмонии лечение не продолжается после получения микробиологических данных.
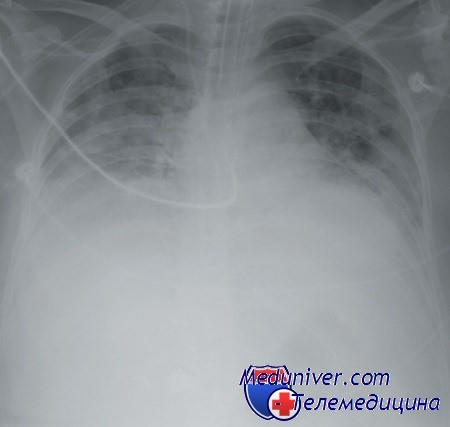
После начала лечения при подозрении на ИВЛ-ассоциированную пневмонию, посевы из нижних дыхательных путей могут выявить:
1) отсутствие роста или несущественный рост (ниже заранее определенного порогового значения);
2) значительный (выше порога) рост патогена, чувствительного к препарату узкого спектра; или
3) значительный рост патогена, чувствительного только к препарату широкого спектра.
При первом сценарии, антимикробную терапию можно безопасно прекратить, если состояние пациента не ухудшается. При втором сценарии, терапию сокращают до препарата узкого спектра, активного против патогена. При последнем сценарии, продолжается лечение первоначальным препаратом широкого спектра, активным против патогена.
После начала патогенспецифической терапии, необходимо определить ее продолжительность, чтобы избежать длительного и ненужного применения. Накопление клинических и рентгенологических признаков занимает больше времени, чем уничтожение инфекции. Vidaur et al. Обнаружили, что улучшение оксигенации и нормализация температуры тела происходит у пациентов с ИВЛ-ассоциированной пневмонией без легочных осложнений в течение трех дней. Dennesen et al. наблюдали клинический ответ на терапию (например, нормализацию температуры, лейкоцитоза, напряжения кислорода в артериальной крови и уменьшение числа бактерий в мокроте) в пределах 6 дней от начала лечения ИВЛ-ассоциированной пневмонии.
Было проведено рандомизированное многоцентровое исследование 401 пациента (ИВЛ-ассоциированной пневмонии доказана бронхоскопией с количественной микробиологией), распределенных так, чтобы антибактериальное лечение проводилось в течение 8 или 14 дней. Все пациенты получали адекватную эмпирическую терапию, и все пациенты в группе восьмидневной терапии на протяжении этого времени были стабильны. У пациентов, которых лечили восемь дней, была равнозначная смертность, продолжительность механической вентиляции и частота рецидивирования инфекции, несмотря на значительно большее число дней без антибиотикотерапии.
Рецидивная инфекция у пациентов, которых лечили восемь дней, вызывалась полирезистентными патогенами реже; однако у пациентов с ИВЛ-ассоциированной пневмонией, вызванной неферментирующими грамотрицательными палочками (например, Pseudomonas, Acinetobacter, Stenotrophomonas) рецидив пневмонии возникал чаще. Таким образом, восьмидневный курс изначально подходящей антибиотикотерапии представляется безопасным и эффективным, при условии, что пациент стабилен и патоген — не неферментирующая грамотрицательная палочка.
У отдельных пациентов для лечения ИВЛ-ассоциированной пневмонии может быть эффективен более короткий курс лечения. Singh et al. рандомизировали пациентов с подозрением на ИВЛ-ассоциированную пневмонию и оценкой по CPIS менее 6 баллов для получения либо стандартной терапии (на усмотрение врача), либо монотерапии ципрофлоксацином, с переоценкой на третий день и прерыванием антибиотикотерапии, если CPIS оставался меньше 6.
Если при оценке на третий день CPIS оставался меньше 6, то антибиотикотерапия продолжалась у 96% (24/25) из группы стандартной терапии, но ни у одного из группы экспериментальной терапии (р=0,0001). Смертность не отличалась, несмотря на меньшую продолжительность (р=0,0001) и стоимость (р=0,003) антимикробной терапии в группе с краткосрочным лечением.
При отсутствии ответа на соответствующее лечение по поводу ИВЛ-ассоциированной пневмонии, возникает дилемма. Нужно предположить неадекватное лечение, неправильный диагноз или связанное с пневмонией осложнение (например, эмпиему или абсцесс легкого). Следует повторить диагностические мероприятия, включая количественную оценку культур из мокроты (используя более низкий диагностический порог при интерпретации количественной микробиологии, учитывая недавнее воздействие антибиотиков), и рассмотреть вопрос о расширении покрытия, пока не появятся новые данные.
- Рекомендуем далее ознакомиться со статьей "Катетерная инфекция. Диагностика и лечение"
Оглавление темы "Инфекции травматологических больных":- Хинолоны, метронидазол в лечении инфекций. Триметоприм-сульфаметоксазол - TMP-SMX
- Токсичность антибиотиков. Аллергия к бета-лактамам
- Нефротоксичность и ототоксичность антибиотиков. Поражение почек, слуха
- Применение антибиотиков при печеночной и почечной недостаточности
- ИВЛ-ассоциированная пневмония. Факторы риска
- Профилактика ИВЛ-ассоциированной пневмонии. Лекарства и санация пищеварительного тракта
- Диагностика ИВЛ-ассоциированной пневмонии. Критерии
- Лечение ИВЛ-ассоциированной пневмонии. Препараты
- Катетерная инфекция. Диагностика и лечение
- Вторичный перитонит при травме. Причины и диагностика

