Принципы лечения атаксии Фридрейха и ее эффективность
В настоящее время выявление с помощью прямой ДНК-диагностики случаев атаксии Фридрейха на ранней и пресимптоматической стадии приобретает особое значение в связи с потенциальными возможностями превентивной терапии, перспективы которой становятся все более реальными в свете новых знаний о патогенезе болезни. Центральное место в этих разработках занимают препараты митохондриального ряда, антиоксиданты и хелатные соединения, способствующие уменьшению аккумуляции железа в митохондриях.
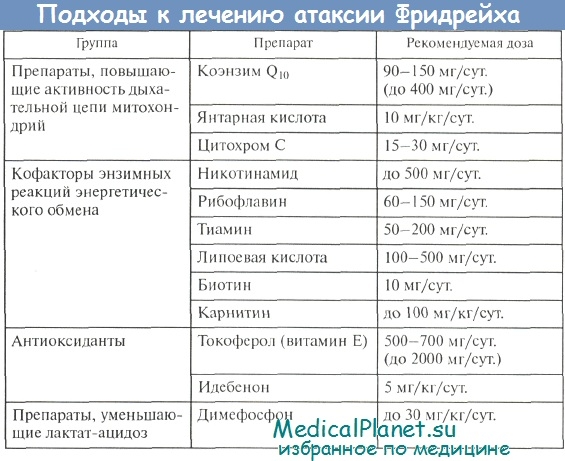
В связи с недостаточностью энергопродукции при атаксии Фридрейха важное значение в лечении данного заболевания придается в настоящее время препаратам, поддерживающим функцию митохондрий и широко применяющимся в терапии других митохондриальных болезней. Наиболее перспективные и доступные группы митохондриальных препаратов, которые могут быть использованы в терапии атаксии Фридрейха, указаны в таблице 10 (Казанцева Л.З. и др., Kieburtz К., Chinnery P.F., Turnbull D.M.).
Необходимо подчеркнуть особо важную роль применения при атаксии Фридрейха препаратов янтарной кислоты, при окислении которой конечный уровень макроергических соединений значительно превышает таковой при окислении НАД-зависимых субстратов. Напротив, применение известного «классического» антиоксиданта — аскорбиновой кислоты — при атаксии Фридрейха не рекомендуется, поскольку в экспериментах in vitro было установлено, что данный водорастворимый антиоксидант может приводить к образованию токсичных форм «патогенетически значимого» при атаксии Фридрейха иона железа (Rustin P. ct al.).
Общий принцип лечения данными препаратами состоит в сочетанием назначении лекарств, синергично влияющих на разные уровни энергетического метаболизма. Рекомендуется одновременное назначение как минимум трех лекарственных средств из первых трех групп, указанных в таблице 10, в соответствующих дозах. Если при биохимических исследованиях у больного выявляется лактат-ацидоз, в схему терапии добавляют димефосфон.
В комплекс применяемых препаратов обязательно должны входить стимуляторы переноса электронов в дыхательной цепи, в первую очередь коэнзим Q10 в высоких дозах, а также сукцинаты. Из коферментов энзимных реакций преимущество должно отдаваться никотинамиду, входящему в состав I комплекса дыхательной цепи. Из числа антиоксидантов возможно использование витамина Е, особенно с учетом выраженного положительного эффекта препарата при фенотипически сходной витамин-Е-дефицитной атаксии. Подобрать наиболее оптимальное сочетание препаратов для терапии конкретного пациента можно с учетом данных цитохимического исследования крови.
Нами в 2000—2003 гг. проведено исследование эффективности вышеуказанной комплексной терапии у 25 больных атаксией Фридрейха с использованием модифицированной балльной клинической шкалы (Pourcher Е., Barbeau А.) и цитохимического метода оценки активности ключевых митохондриальных ферментов — СДГ, ГФДГ, ГДЕ МДГ и ЛДГ. Продолжительность лечебного курса в условиях стационара составляла 3 нед., после чего больным рекомендовалось продолжать прием препаратов в домашних условиях (с соответствующей корректировкой дозы и кратности приема) в течение 4—6 мес. и более. Цитохимическое исследование активности митохондриальных дегидрогеназ проводилось больным до и после курса лечения.
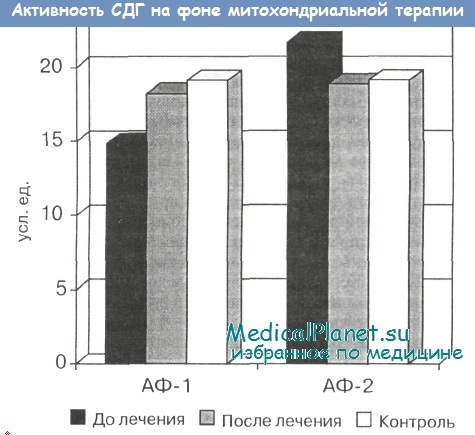
Анализ полученных цитохимических данных на фоне проводимой комплексной терапии позволил установить, что у 92% больных произошло значительное улучшение показателей активности исследуемых ферментов (прежде всего СДГ) — вплоть до их полной нормализации. В подгруппе больных с исходной депрессией активности СДГ (подгруппа АФ-1) этот параметр повышался, а в подгруппе больных с исходно повышенной активностью СДГ и ЛДГ(АФ-2) понижался практически до нормальных значений. Величина активности ЛДГ в обеих группах после лечения оказалась выше контрольной, что, вероятно, отражает возросшую активность гликолиза при энергообеспечении клеток в условиях системного дефекта митохондриального метаболизма.
У основной части больных положительная динамика состояния на фоне проведенного лечения была зафиксирована по таким клиническим критериям, как мышечная сила в конечностях, толерантность к физическим нагрузкам, общая утомляемость, двигательная активность, речевые и координаторные функции. В целом, общее количество баллов по шкале, отражающее тяжесть состояния, снизилось на фоне лечения на 3—15% от исходного. Необходимо отметить, что уменьшение общей тяжести болезни, выраженное в баллах по всем рубрикам использованной шкалы, было более отчетливым, чем улучшение в разделе шкалы «атаксия». Наблюдавшееся улучшение касалась также экстраневральных проявлений болезни — миокардиодистрофии и сахарного диабета (при их наличии в клинической картине), что проявлялось улучшением метаболических процессов в миокарде (по данным ЭКГ) и нормализацией гликемии. Таким образом, положительная динамика клинической картины у наших пациентов с атаксией Фридрейха в основном коррелировала с улучшением метаболических процессов, оцениваемых по комплексу цитохимических показателей.
Полученные предварительные результаты свидетельствуют о том, что вышеуказанный комплекс митохондриальных препаратов может способствовать определенной стабилизации энергетических процессов в клетке и тем самым в какой-то степени замедлять развитие нейродегенерации при атаксии Фридрейха. В то же время, очевидно и другое: эффективность доступных на сегодня митохондриальных препаратов остается сравнительно ограниченной и в долговременной перспективе они, к сожалению, не способны существенно видоизменить естественное течение такого тяжелого заболевания, как атаксия Фридрейха. Повторные курсы лечения данными препаратами могут рассматриваться как патогенетически обоснованная поддерживающая терапия у пациентов с атаксией Фридрейха.
Из всех антиоксидантов наибольшой интерес при атаксии Фридрейха вызывает в настоящее время новый препарат идебенон — синтетический короткоцепочечный структурный аналог коэнзима Q10. Органом-мишенью для идебенона является миокард, в связи с чем его применение оправдано прежде всего у пациентов с классическим фенотипом, включающим гипертрофическую кардиомиопатию.
P.Rustin и соавт. оценивали эффект идебенона как «сборщика» свободных радикалов спектрофотометрическим методом в гомогенатах кардиомиоцитов, полученных при эндомиокардиальной биопсии убольных атаксией Фридрейха (Rustin R et al.). Препарат назначали пациентам перорально в дозе 5 мг/кг веса в сутки; на фоне лечения оценивались уровни активности ферментов цикла Кребса, аконитазы и трех комплексов дыхательной цепи митохондрий. Результаты экспериментов показали, что идебенон защищает липиды мембран и ферменты дыхательной цепи от железоиндуцированного повреждения, не приводя при этом к снижению активности аконитазы. Кроме того, было показано, что короткая молекула идебенона легко проходит через мембраны, включая структуры гематоэнцефалического барьера, и уменьшает уровень протопорфирина IX эритроцитов.
Через 12 мес. непрерывного приема идебенона (5 мг/кг массы в сутки), по данным ультразвуковых методов исследования, значительно уменьшились толщина межжелудочковой перегородки и масса левого желудочка по сравнению с группой плацебо. Исследования показали, что идебенон не останавливает прогрессирования атаксии и неврологическая картина у больных остается без изменений.
Эффективность идебенона в отношении окислительного стресса была подтверждена обнаружением снижения уровня маркера окислительного повреждения ДНК — 8-гидрокси-2'-d-оксигуанозина — на 20% от исходного до лечения (Schulz J. et al.). Теоретически, идебенон и прочие антиоксиданты, действующие на уровне митохондрий, могут замедлять прогрессирование болезни.
Наиболее убедительные результаты использования идебенона получены совсем недавно на трансгенной модели атаксии Фридрейха у мышей: показано, что данный препарат отсрочивает развитие кардиомиопатии и наступление смерти у фратаксин-дефицитных животных, не влияя, однако, на имеющийся дефект ключевых Fe-S-содержащих ферментов (Seznec Н. et al.). Эти данные позволяют заключить, что идебенон оказывает свое действие на более позднем этапе патогенетического каскада по отношению к первичному дефициту Fe-S-белков, будучи эффективным даже при полном отсутствии в клетках-мишенях фратаксина, что дополнительно обосновывает целесообразность его применения у больных атаксией Фридрейха.
Первые подходы к патогенетической терапии атаксии Фридрейха хелатными соединениями с целью выведения избыточного железа из митохондриальных депо оживленно обсуждаются в литературе. Например, неоднократно сообщалось о попытках применения при атаксии Фридрейха хелатного препарата «Десфсрал» (действующее вещество — десферроксамин). Однако E.Becker и соавт., изучая химическую структуру и фармакокинетику данного препарата, продемонстрировали неспособность десферала проникать внутрь митохондрии, связываться с железом и выводить его из данного клеточного компартмента. Результатом применения препарата является истощение внеклеточных депо железа, интактных при атаксии Фридрейха. В экспериментах in vitro показано, что добавление десферроксамина в экспериментальные системы защищает экстрагированные белки комплекса II дыхательной цепи и липиды от Fe-зависимого окисления, но при этом приводит к выраженному снижению общей активности аконитазы (Richardson D. el al., Rustin R et al.).
Другое исследуемое хелатное соединение — деферипрон, на которое возлагались большие надежды, — также оказалось неэффективным в отношении выведения железа из митохондриального компартмента и, кроме того, обладало выраженными побочными эффектами в виде серьезных расстройств функции печени и др. Имеются сообщения и о принципиально новой группе хелатов — PIH (аналоги пиридоксаль-изоникотинол гидразонов) — высокоспецифичных и эффективно элиминирующих железо в экспериментах с использованием эритроцитов кролика. Благодаря хорошей растворимости в жирах препарат легко проникает через двуслойную мембрану митохондрий. Целый ряд аналогичных препаратов, обладающих низкой токсичностью и способностью выводить из митохондрий депонированное железо, проходят в настоящее время стадию испытаний на животных моделях, и их эффективность активно обсуждается (Richardson D.R. et al.). D.B.Shachar и соавт. предложили первое хелатное соединение VK-28 (гидроксиэтил-пиперазин-квинолин), проникающее в ткани мозга и оказывающее нейропротективное действие.
Авторы предполагают, что в перспективе можно будет использовать данное соединение для лечения ряда нейродегенеративных процессов с аномальным распределением железа (болезнь Паркинсона, атаксия Фридрейха, ацерулоплазминсмия, болезнь Галлервордена-Шпатца и др.).
Одним из перспективных направлений научных исследований является поиск эффективных соединений, увеличивающих содержание в клетках белка-фратаксина. Результаты работ M.Turano и соавт., M.Ghazizadeh и соавт. указывают на потенциальную роль циспластина и 3-нитропропионовой кислоты в качестве индукторов экспрессии фратаксина, а также на ген FRDA в качестве потенциальной мишени для этих соединений. По-видимому, в ближайшем будущем можно ожидать появления этих и ряда других принципиально новых методов лечения атаксии Фридрейха.
Комплексное лечение больных атаксией Фридрейха должно включать применение довольно широкого спектра симптоматических средств. Обычно назначают препараты, улучшающие метаболизм миокарда: рибоксин, кокарбоксилазу, предуктал и др. При выраженной тахикардии в схему терапии добавляют небольшие дозы бета-блокаторов. При этом необходимо помнить, что при сахарном диабете эти препараты должны применяться под строгим врачебным контролем. В редких случаях спастичности хороший эффект дают миорелаксанты — баклофен (в дозе 5—15 мг/сут.) или сирдалуд (в дозе 4-6 мг/сут.). Следует помнить, что эти препараты должны назначаться осторожно, с медленным и постепенным повышением суточной дозы. Их передозировка может вызвать общую слабость и ухудшение походки.
Больным атаксией Фридрейха рекомендуется диетическое сбалансированное питание с уменьшенным содержанием углеводов до 10 г/кг (вариант диеты №9), поскольку высокое их потребление является своеобразной «провокацией», усиливающей дефект энергетического обмена.
Большое значение при атаксии Фридрейха имеют физические методы лечения. Их целью является предотвращение контрактур конечностей, тренировка и поддержание мышечной силы, воздействие на тонус мышц. Важен также эффект обучения необходимым двигательным навыкам, что способствует более длительной сохранности функциональной активности и предотвращению различных травм. Особое значение имеет умеренная и тщательно дозированная лечебная физкультура, которая должна проводиться регулярно с обязательным включением координаторно-вестибулярного комплекса упражнений. Для борьбы с контрактурами целесообразно назначать массаж, парафин (озокерит), специальную ортопедическую обувь с жестким высоким задником. Иногда при выраженных контрактурах и ретракции ахилловых сухожилий может быть рекомендовано оперативное лечение (рассечение сухожилий и их пластика, в том числе с использованием трансплантатов). При парезах целесообразно использовать электростимуляцию мышц, при спастичности — электрофорез с миорелаксантами.
Современным и перспективным методом коррекции координаторных нарушений у больных атаксией Фридрейха является компьютерная стабилография с использованием метода зрительной обратной связи, которая уже на протяжении 5 лет с успехом используется нами в Институте неврологии РАМН (Устинова К.И. и др.). Баланс-терапия проводится на компьютерном стабилоанализаторе, который обеспечивает регистрацию и анализ траектории перемещения центра давления, оказываемого человеком на плоскость опоры в процессе поддержания им вертикальной позы. Траектория перемещения центра давления представляется на экране монитора в виде стабилограмм, т.е. во времени, в сагиттальном и фронтальном направлениях и в двухмерном пространстве. Данный метод может с успехом использоваться как для диагностики, так и для коррекции нарушений стояния и ходьбы.
При атаксии Фридрейха описаны примеры успешного оперативного лечения тяжелых форм сколиоза (кривизна свыше 40°), особенно у детей, сохраняющих навыки самостоятельной ходьбы (Harding А.Е.). Хирургическая коррекция деформаций грудного отдела позвоночника может способствовать удлинению ожидаемой продолжительности жизни пациентов за счет улучшения легочных функций, а также в определенной степени помогает поддерживать функцию равновесия.
- Читать "Профилактика и скрининг на атаксию Фридрейха"
Оглавление темы "Атаксия Фридрейха":- Пример атипичной формы атаксии Фридрейха
- Пример атипичной формы атаксии Фридрейха варианта FARR
- Пример атаксии Фридрейха фенотипа спастической атаксии
- Пример мягкой формы атаксии Фридрейха - акадской формы
- Морфология атаксии Фридрейха
- Дополнительные методы обследования при атаксии Фридрейха
- Дифференциальная диагностика атаксии Фридрейха
- ДНК-диагностика атаксии Фридрейха
- Принципы лечения атаксии Фридрейха и ее эффективность
- Профилактика и скрининг на атаксию Фридрейха

