Строение скелетной мышцы. Гистология
Скелетную мышцу образуют мышечные волокна — очень длинные (до 30 см) цилиндрические многоядерные клетки диаметром 10 — 100 мкм, образующие пучки. Многоядерность возникает в эмбриональном периоде в результате слияния одноядерных мио-бластов (предшественников мышечных клеток). Овальные ядра обычно располагаются на периферии волокна под клеточной мембраной.
Знание этой особенности расположения ядер полезно, когда необходимо отличить скелетную мышцу от сердечной и гладкой мышцы, поскольку в двух последних ядра располагаются в центральной части клеток.
Различия диаметра волокон скелетной мышцы зависят от таких факторов, как особенности самой мышцы, возраст, пол, состояние питания и физическая тренированность человека. Хорошо известно, что физические упражнения увеличивают мускулатуру и снижают жировые отложения. Полученное таким путем увеличение массы мышечной ткани вызвано выраженным нарастанием диаметра каждого мышечного волокна и образованием в волокнах новых миофибрилл.
Этот процесс, характеризующийся нарастанием объема клетки, известен как гипертрофия (греч. hyper — сверх + trophe — питание); рост ткани за счет увеличения числа клеток обозначается термином «гиперплазия» (греч. hyper— сверх + plasis— образование). Гиперплазия не развивается ни в скелетной, ни в сердечной мышечной ткани, но происходит в гладкой мышечной ткани, клетки которой не утратили способности делиться митозом. Гиперплазия довольно часто развивается в таких органах, как матка, где во время беременности происходит как гиперплазия, так и гипертрофия.
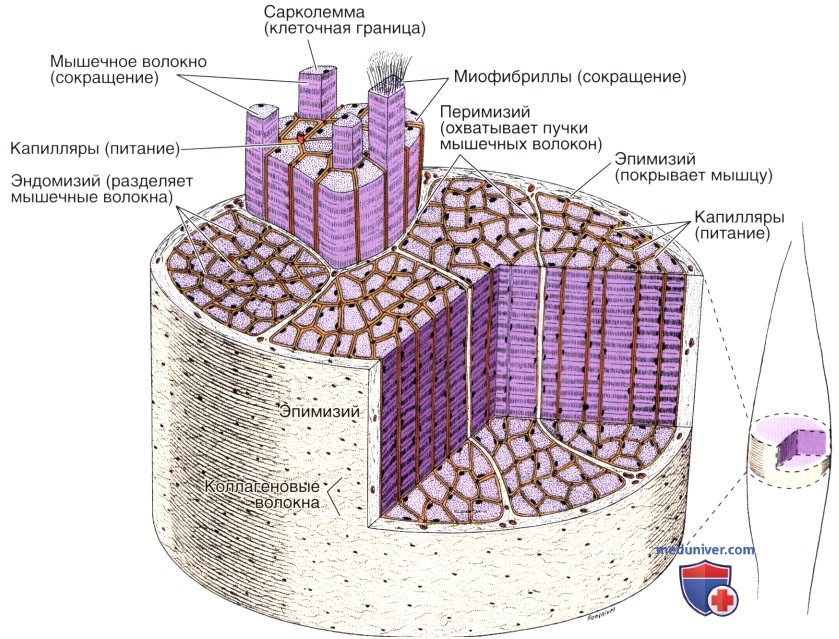
Рисунок справа указывает на участок мышцы, который детально представлен в виде увеличенного сегмента органа.
Цветом выделены эндомизий, перимизий и эпимизий.
Организация - строение скелетной мышцы
Крупные скопления волокон, которые образуют различные типы мышц, сгруппированы не случайным образом, а располагаются в виде правильных пучков. Всю мышцу снаружи окружает оболочка из плотной волокнистой соединительной ткани — эпимизий (греч. epi — верхний + mys — мышца).
От эпимизия внутрь мышцы отходят тонкие прослойки соединительной ткани, которые охватывают пучки волокон внутри мышцы. Соединительная ткань, окружающая каждый пучок мышечных волокон, известна как перимизий (греч. peri— вокруг + mys — мышца). Вокруг каждого мышечного волокна располагается окружающий его тонкий слой соединительной ткани — эндомизий (греч. endon — внутри + mys — мышца), состоящий главным образом из базальной пластинки и ретикулярных волокон.
Одной из наиболее важных функций соединительной ткани в мышцахявляется механическая передача сил, которые образуются в результате сокращения мышечных волокон, поскольку в большинстве случаев отдельные мышечные волокна не протягиваются от одного края мышцы к другому.
Кровеносные сосуды проникают в мышцу в составе соединительнотканных прослоек и образуют богатую капиллярную сеть, которая располагается между мышечными волокнами и параллельно им. Капилляры относятся к непрерывному типу; в соединительной ткани обнаруживаются также и лимфатические сосуды.
Некоторые мышцы конусообразно сужаются у своих краев, где образуется мышечно-сухожильное соединение. Под электронным микроскопом видно, что в этой переходной зоне коллагеновые волокна сухожилия вставлены в сложные складки плазмолеммы мышечных волокон.
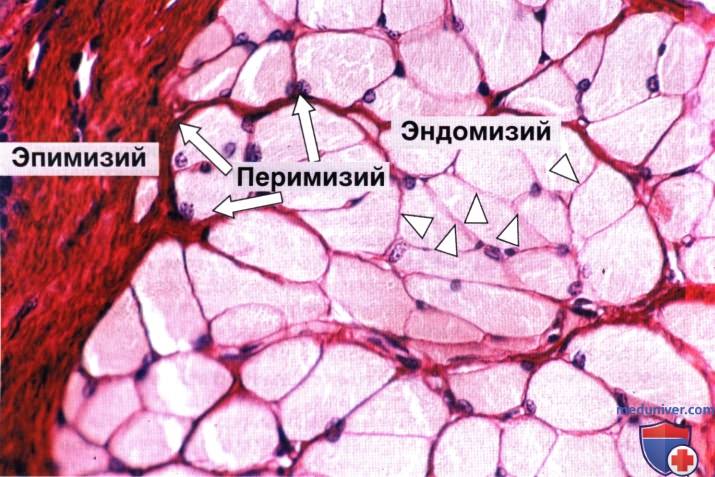
Эндомизий показан треугольниками, а перимизий — стрелками. Слева виден участок эпимизия. Окраска: пикросириус—гематоксилин. Большое увеличение.
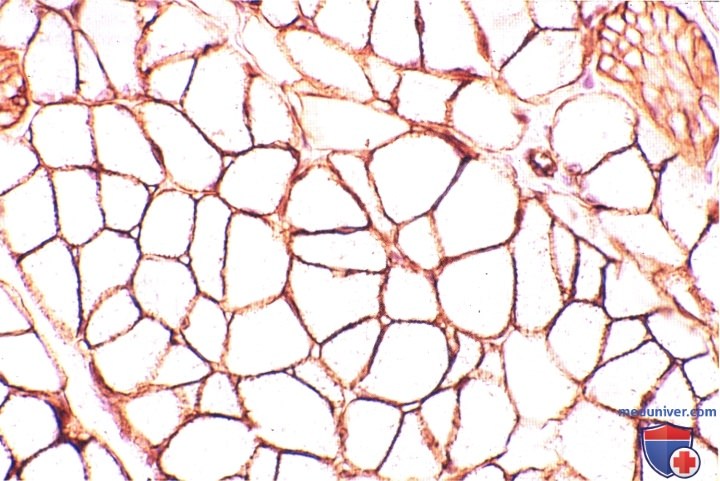
И ммуногистохимическая реакция выявления ламинина — белка, входящего в состав эндомизия, окрашивает его в различные оттенки коричневого цвета.
В верхнем правом углу виден слегка косой срез мелкого нерва. Ламинин присутствует также вокруг нервных волокон.
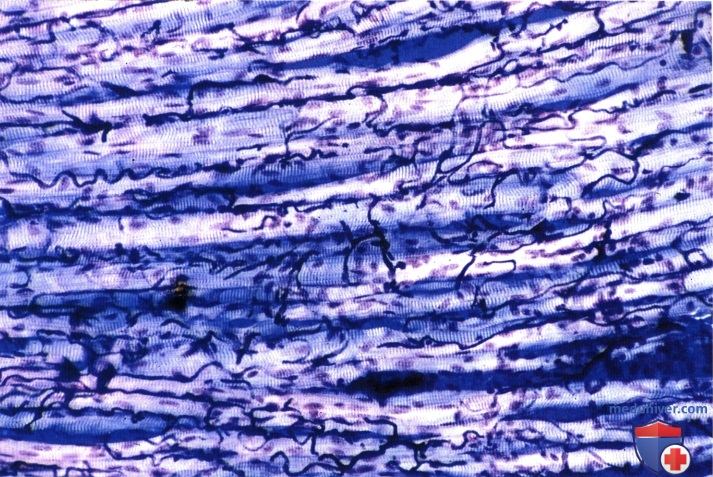
Кровеносные сосуды были налиты пластическим материалом у животного прижизненно. Обратите внимание на исключительно богатую сеть кровеносных капилляров вокруг мышечных волокон.
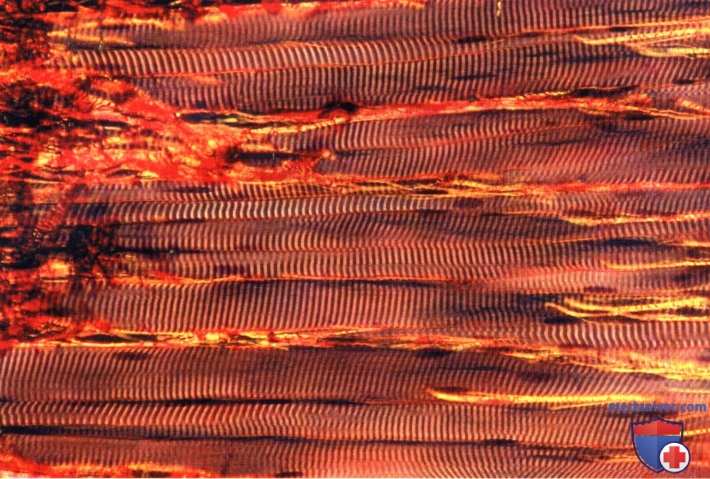
Окраска по Гимзе. Микрофотография выполнена при малом увеличении с использованием поляризованного света.
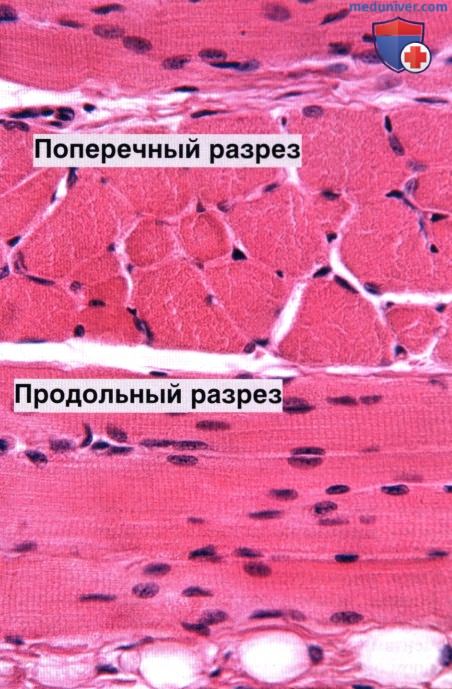
Ядра видны на периферии поперечнополосатых волокон, непосредственно под клеточной мембраной, что особенно заметно на поперечных срезах волокон. Окраска: гематоксилин-эозин. Среднее увеличение.
В левой части микрофотографии отчетливо видно проникновение коллагеновых волокон в мышцу.
Окраска: пикросириус—поляризованный свет. Среднее увеличение.

Окраска по Гимзе. Большое увеличение.

Окраска: пикросириус—поляризованный свет. Большое увеличение.
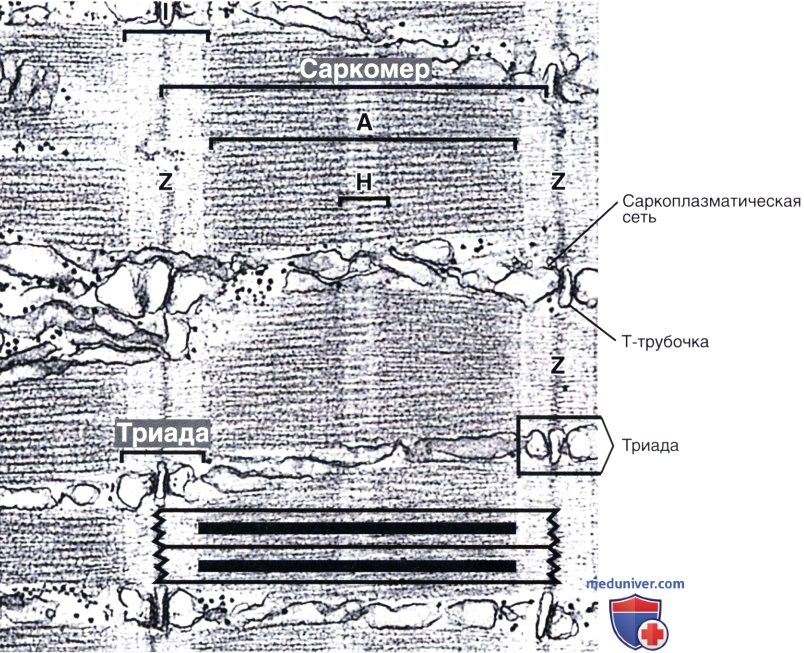
Расположение толстых и тонких филаментов в саркомере схематически представлено в нижней части иллюстрации.
Как здесь показано, расположение триад в мышце земноводных совпадает с Z-линией в каждом саркомере. В мышце млекопитающих, однако, каждый саркомер содержит две триады — по одной на каждой границе А- и I-дисков.
Электронная микрофотография, х35 000.
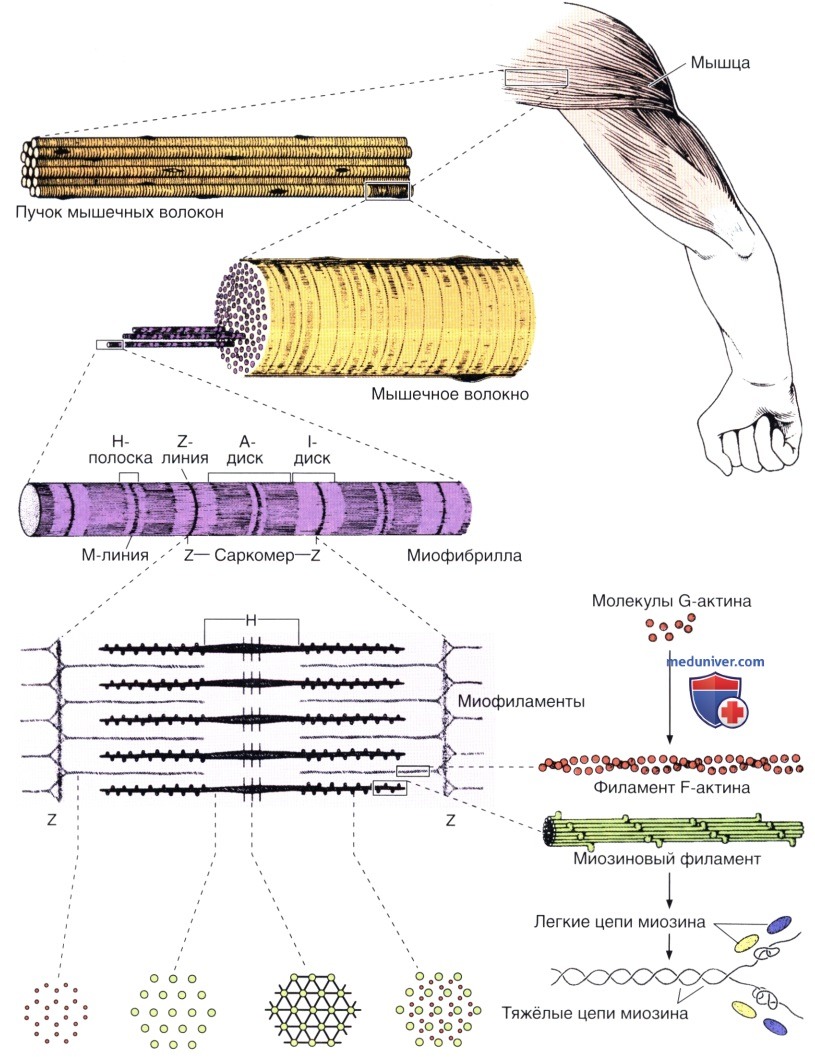
Показаны структура и расположение толстых и тонких филаментов в саркомере. Молекулярная структура этих компонентов представлена справа.
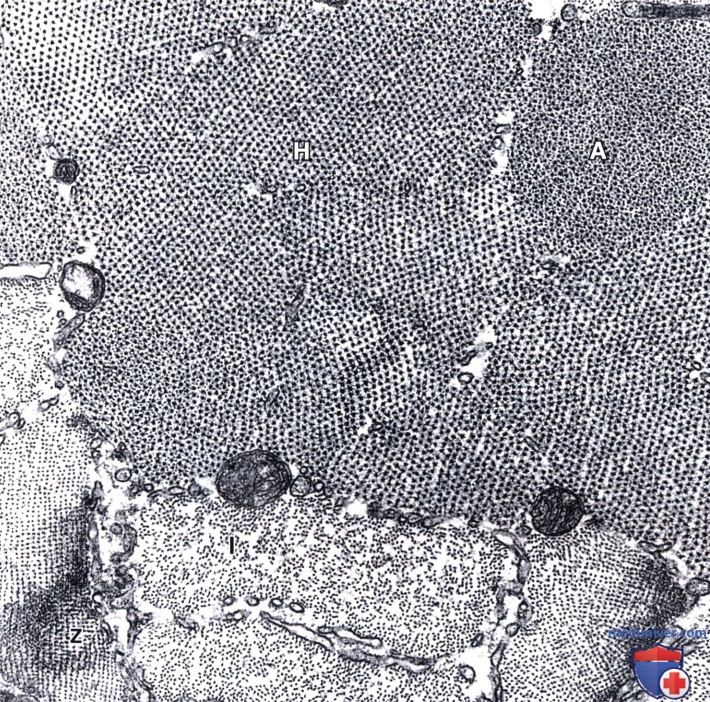
На этой электронной микрофотографии можно выявить некоторые детали, схематично представленные на рисунке выше.
I — I-диск; А — А-диск; Н — Н-полоска; Z — Z-линия. х36 000.
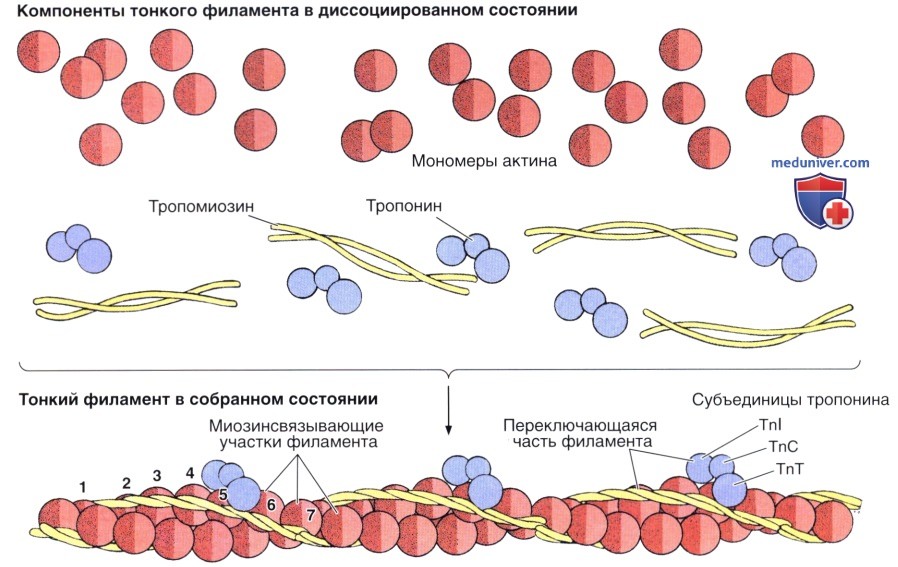
В верхней части рисунка показаны отдельные компоненты, в нижней — они представлены в полимеризованной форме. Глобулярные актиновые молекулы поляризованы и полимеризуются в одном направлении.
Обратите внимание на то, что каждая молекула тропомиозина протягивается над семью молекулами актина. TnI, TnC и TnC — субъединицы тропонина.
Организация - строение волокон скелетной мышцы
При световой микроскопии на продольных срезах мышечных волокон видна поперечная исчерчен-ность, обусловленная чередованием светлых и темных полос — дисков. Темные диски — А-диски (анизотропные) названы так, поскольку они обладают двойным лучепреломлением в поляризованном свете; светлые диски — I-диски (изотропные) не меняют направления поляризованного света. Под электронным микроскопом видно, что каждый I-диск рассекается пополам темной поперечной линией, которая известна как Z-линия (телофрагма).
Самой малой повторяющейся единицей сократительного аппарата является саркомер (греч. sarkos— мясо + теге— часть), который располагается между двумя соседними Z-линиями. В покоящейся мышце его длина равна 2,5 мкм.
Саркоплазма мышечного волокна содержит длинные цилиндрические нити диаметром 1—2 мкм— миофибриллы, которые располагаются в ней в виде пучков. Миофибриллы идут параллельно длинной оси мышечного волокна и состоят из цепочек связанными своими краями саркомеров. Саркомеры соседних миофибрилл располагаются так, что их латеральные границы совпадают — это обусловливает поперечную исчерченность, характерную и для всего мышечного волокна.
Электронно-микроскопические исследования показали, что строение саркомеров определяется главным образом присутствием двух типов филаментов (толстых и тонких), которые симметричным образом располагаются параллельно длинной оси миофибриллы. Длина толстых филаментов составляет 1,6 мкм, ширина (толщина) — 15 нм; они находятся в А-диске, занимая центральную часть саркомера. Тонкие филаменты проходят между толстыми филаментами, располагаясь параллельно им; одним концом они прикреплены к Z-линии. Длина тонких филаментов составляет 1,0 мкм, ширина (толщина) — 8 нм.
В результате такого расположения I-диск состоит из частей тонких филаментов, которые не перекрываются с толстыми филаментами. А-диски образованы преимущественно толстыми филаментами, помимо которых в них находятся заходящие за толстые филаменты части тонких филаментов. При детальном исследовании А-диска в его центре обнаруживается более светлая зона — Н-полоска, которая соответствует области, состоящей только из палочковидных участков молекул миозина.
Н-полоску рассекает надвое М-линия (мезофрагма), которая является участком, где между соседними толстыми филаментами образуются латеральные соединения. Главным белком М-линии является креатинкиназа. Этот фермент катализирует перенос фосфатной группы с фосфокреатина (формы хранения высокоэнергетических фосфатных групп) на АДФ, тем самым образуя АТФ, необходимый для мышечного сокращения.
Тонкие и толстые филаменты перекрываются на некотором расстоянии в пределах А-диска. Вследствие этого на поперечном срезе участка перекрывающихся филаментов видно, что каждый толстый филамент окружен шестью тонкими филаментами, расположенными в форме шестиугольника.
Филаменты в поперечнополосатой мышце содержат несколько белков; четырьмя главными белками являются актин, тропомиозин, тропонин и миозин. Тонкие филаменты состоят из первых трех белков, тогда как в состав толстых филаментов входит главным образом миозин. Совместно на миозин и актин приходится 55% общего содержания белка в поперечнополосатой мышце.
Актин встречается в виде длинных нитевидных (филаментозных) полимеров (F-актин), которые состоят из двух нитей, образованных глобулярными мономерами (G-актин) диаметром 5,6 нм, скрученных одна вокруг другой с образованием двойной спирали. Молекулы G-актина обладают структурной асимметрией. При полимеризации молекул G-актина с образованием F-актина они связы ваются друг с другом по ти пу «конец в начало», образуя филаменты с отчетливо выраженной полярностью.
Каждый мономер G-актина содержит участок связывания миозина. Актиновые филаменты, которые заякорены в области Z-линии и располагаются перпендикулярно ей, обладают противоположной полярностью по обеим сторонам этой линии. Предполагается, что актиновые филаменты закреплены в этой области с помощью белка а-актинина, который является главным компонентом Z-линии. Считается, что а-актинин и десмин (белок промежуточных филаментов) связывают воедино соседние саркомеры, тем самым удерживая миофибриллы в правильном положении.
Тропомиозин — длинная, тонкая молекула длиной около 40 нм, содержит две полипептидные цепи. Эти молекулы связаны между собой головкой к хвосту, формируя филаменты, которые лежат поверх акти-новых субъединиц вдоль наружных краев бороздки между двумя скрученными актиновыми нитями.
Тропонин представляет собой комплекс из трех субъединиц: TnT, которая прочно прикреплена к тропомиозину, TnC, которая связывает ионы кальция, и TnI, которая угнетает взаимодействие между актином и миозином. Тропониновый комплекс прикреплен к определенному участку на каждой молекуле тропомиозина.
В тонких филаментах каждая молекула тропомиозина охватывает семь молекул G-актина и имеет один тропониновый комплекс, связанный с ее поверхностью.
Миозин — значительно более крупный комплекс (молекулярная масса -500 кДальтон), который можно разъединить на две идентичные тяжелые цепи и две пары легких цепей. Тяжелые цепи миозина — тонкие, стержневидные молекулы (длиной 150 нм и толщиной 2—3 нм), которые скручены попарно. Небольшие шаровидные (глобулярные) выпячивания у одного края каждой тяжелой цепи образуют головки, которые содержат участки связывания АТФ, а также обладают способностью к ферментному гидролизу АТФ (АТФазной активностью) и к связыванию с актином.
С головкой соединены четыре легкие цепи. Каждый толстый филамент образован несколькими сотнями молекул миозина, причем их стержневидные участки взаимно перекрываются, а глобулярные головки обращены к одному из краев.
Анализ тонких срезов поперечнополосатой мышцы указывает на присутствие поперечных мостиков между тонкими и толстыми филаментами. Эти мостики, которые, как выяснилось, формируются за счет головки молекулы миозина и короткого участка ее стержневого отдела, участвуют в превращении химической энергии в механическую.
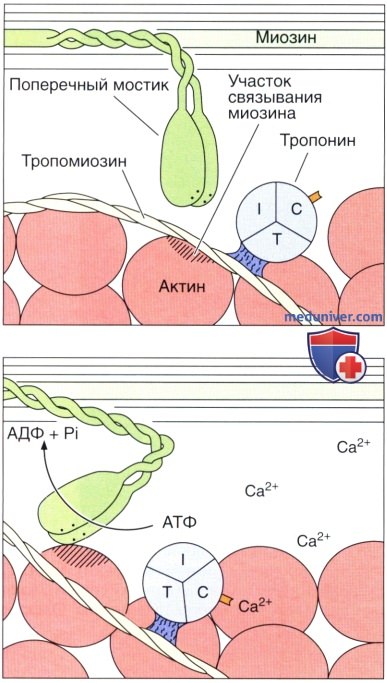
На втором этапе миозиновая головка связывается с актином, и АТФ расщепляется до АДФ, давая энергию, обеспечивающую движение миозиновой головки.
Вследствие этого изменения миозина, связанные с ним тонкие филаменгы скользят по толстым филаментам.
Этот процесс, который повторяется многократно в течение одного сокращения, приводит к полному перекрыванию актина и миозина и обусловливает укорочение всего мышечного волокна. I, Т и С — субъединицы тропонина.
Видео лекция гистология мышечной ткани (гладкой, поперечнополосатой, сердечной)
- Читать далее "Саркоплазматическая сеть и система поперечных трубочек скелетной мышечной ткани"
Оглавление темы "Гистология мышечной ткани":- Виды мышечной ткани. Строение
- Строение скелетной мышцы. Гистология
- Саркоплазматическая сеть и система поперечных трубочек скелетной мышечной ткани
- Механизмы сокращения скелетной мышцы. Схема
- Иннервация скелетных мышц. Механизмы
- Мышечные веретена и сухожильные органы Гольджи. Гистология
- Сердечная мышца: строение, гистология
- Гладкая мышечная ткань: строение, гистология
- Регенерация мышечной ткани. Механизмы заживления мышц

