Примеры гомоцистинурии у детей
В качестве иллюстрации особенностей клинической картины гомоцистинурии приводим два наблюдения за детьми с пиридоксинрезистентной и пиридоксинзависимой формой заболевания.
Наташа Е., 9 лет, поступила в клинику Института педиатрии и детской хирургии с диагнозом: подвывих хрусталиков, вторичная глаукома. Матери 36 лет, страдает язвенной болезнью желудка. У отца ость родственники с психическими заболеваниями, тугоухостью и алкоголизмом.
Девочка родилась от второй беременности, которая протекала с токсикозом па всем протяжении. Роды в срок. Масса тела при рождении — 3350 г, рост — 51 см. До 6 мес находилась па грудном вскармливании. Рапное психомоторное развитие протекало без особенностей: вовремя стала держать голову, сидеть ходить и говорить. Только в возрасте 4,5 лет родители обратили внимание на снижение зрения и задержку умственного развития.
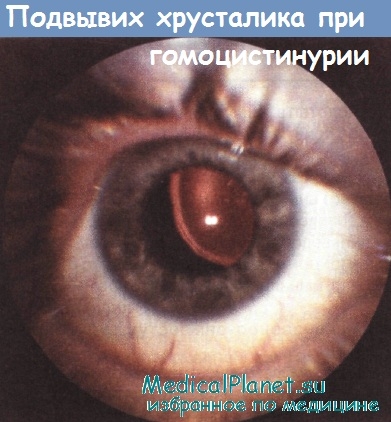
В возрасте 5 лет после внезапно развившейся глаукомы на фоне подвывиха хрусталиков в переднюю камеру глаза и высокой степени миопии — (—13 D) ребенку была произведена операция удаления хрусталиков.
К моменту обследования девочки в отделе клинической генетики (9 лет) имелся четко выраженный симптомокомплокс, свойственный гомо-цистинурии: конституциональные и скелетные аномалии в виде укороченного туловища, длинных конечностей, парушения осанки, короткой шеи, вальгусной деформации нижних конечностей, неправильного прикуса, умеренно выраженного остеопороза; нарушения зрения в виде афокии, вторичной глаукомы, дегенеративно-атрофических изменений угла передней камеры глаза; сердечпо-сосудистые расстройства, проявляющиеся ногрубыми изменениями ЭКГ и ФКГ, наличием систолического шума, нарушением процесса реполяризации желудочков; изменения нервной системы в виде значительного интеллектуального дефекта (IQ = 55 ед.) и парушений ЭЭГ.
При лабораторном обследовании (хроматография па ионообменных смолах) найдены характерные для гомоцистипурии изменения аминокислотного спектра крови и мочи: гиперметионипемия (15 мг/л при норме 4—8 мг/л), гиперметионинурия (44,1 мг/сут при норме 2,0—7,0 мг/сут), гомоциетипурия (78,0 мг/сут при отсутствии в норме), наличие в моче дисульфидов гомоцистеина и цистеина (141,2 мг/сут при отсутствии в норме).
Назначение малобелковой диеты с низким содержанием метиопина и добавлением цистина оказало благоприятный эффект и способствовало нормализации биохимических изменений, что создало более благоприятные условия для последующего развития ребенка.
Ира Д., 7 лет, поступила в клинику с диагнозом: синдром Марфана. Матери при рождении ребенка было 38 лет. У нее имелась гиперметропия, костные деформации (килевидная грудная клетка), конституциональные аномалии (клинодактилия, сутулость, короткая шея), волосы светло-русые, глаза голубые. У родственников матери отмечались заболевания сердечнососудистой системы и почек. Отцу ребенка — 44 года, здоров.
Девочка родилась от четвертой беременности (роды третьи). Первая беременность у матери протекала удовлетворительно, родился сын, которому сейчас 17 лет, здоров. Девочка, родившаяся от второй беремсппости, умерла от пневмонии в возрасте 1 года 10 мес. Третья беременность прорвана (медицинский аборт) по желанию жопщины. Масса тола Иры при рождении — 3700 г, рост — 52 см. Закричала сразу, к груди приложена на вторые сутки, сосала вяло. Со второй недели жизни находилась на искусственном вскармливании.
Развитие ребенка протекало с задержкой, ходить стала с 1 года 6 мес, говорить — только после 3 лет. Из перенесенных заболеваний следует отметить ветряную оспу, корь, краснуху и частые ОРЗ. Родители обратили внимание па задержку психомоторного развития у ребенка только в возрасте 2 лет. С этого времени девочка наблюдалась психоневрологом. Диагноз заболевания оставался нелепым, предполагался гипотиреоз, в связи с чем в течение 2 лет проводилось лечение тиреоидином (без эффекта). В возрасте 5 лет обнаружен двусторонний подвывих хрусталиков и диагностирован синдром Марфана.
При поступлении в клинику у девочки отмечались следующие конституциональные аномалии: укороченное туловище, длинные конечности, сутулость, короткая шея, неправильный рост зубов. Походка спастически изменена. Волосы светло-русые, мягкие, вьющиеся крупными завитками, глаза карие. На коже лица в области скул характерный легкий румянец. Над сердцем прослушивался нежный систолический шум, па ЭКГ и ФКГ негрубые изменения. Выявлен двусторонний подвывих хрусталиков без изменений глазного дна.
При рентгенографии трубчатых костей отмечался умеренно выраженный остсопороз, ядра окостенения соответствовали возрастной норме. При наблюдении за ребенком выявлены эмоциональная вялость, замедленность реакций, недостаточная ориентация в окружающей обстановке, инертность нервнопсихической деятельности (слабая переключаемость внимания и низкая работоспособность). При выполнении заданий лицо ребенка оставалось амимичным, временами появлялась немотивированная улыбка. Речь обедненная, состоящая из коротких фраз. Интересы но соответствовали возрасту, предпочитала играть с детьми младшего возраста. Коэффициент развития DQ—32 ед. при норме свыше 80 ед. На ЭЭГ регистрировались признаки общемозговых парушений в сочетании с возбуждением подкорковых образований.
Особенности клинической картины (задержка психомоторного развития, конституциональные аномалии, подвывих хрусталиков, изменения со стороны сердца и др.) позволили, заподозрить гомоцистинурию. При лабораторном обслодопапии (высоковольтный электрофорез, аминокислотный анализатор и др.) были найдены характерные для гомоцистипурии изменения аминокислотного спектра крови и мочи.

В крови концентрация метионина достигала 14,9 мг/л (норма 8 мг/л) и обнаруживался нехарактерный для здоровых людей гомоцистин (8 мг/л). Суточная экскреция метионина с мочой составляла 44 мг, гомоцистина — 216 мг. Кроме того, отмечалось повышение экскреции веществ, свидетельствующих о вовлечении соединительной ткани в патологический процесс. Так, суточная экскреция кислых глюкозаминогликапов (22,2 мг) превышала норму в 3 раза, а содержание оксипролина в суточной моче приближалось к верхней границе нормы (59,7 мг при норме 66,0 + 4,6 мг).
Сочетание специфических клинических и лабораторных изменений позволило диагпостировать гомоцистинурию. В качестве патогенетически обоснованного лечения был использован витамин В6 per os в дозе 100 мг/сут. Биохимический контроль за проводимым лечением показал, что в данном случае речь идет о пиридоксинчувствительной форме гомоцистинурии.
Как видно из таблицы, уже на 4-й день лечения витамином B6 в дозе 100 мг/сут наступила нормализация биохимических показателей: снизилась до нормы суточная экскреция с мочой метионина, исчезли из мочи гомо-цистин и дисульфиды гомоцистина и цистеина. Одновременно изменилась экскреция с мочой серина и цистина. Отмеченные сдвиги в экскреции этих аминокислот могли свидетельствовать об интенсификации потребления серина в реакции конденсации и об увеличении синтеза цистина (конденсация существовавшей недостаточности блокированного фермента). При кратковременной отмене витамина В6 вновь увеличилась экскреция метионина, в моче появился гомоцистин и его дисульфиды.
Возобновление лечения витамином В6, даже в меньшей дозе (30 мг/сут), привело к нормализации аминокислотного спектра крови и мочи. При выписке из клиники ребенку рекомендовано длительное лечение витамином В6 в дозе 30 мг/сут. Кроме того, предложено ограничить использование в диете продуктов, богатых метионином.
При повторном поступлении (через 1 и 2 года) в клинику отмечено определенное влияние проведенного лечения: повысился уровень умственного развития (IQ = 45 ед.), аминокислотный спектр крови и мочи соответствовал норме. Под влиянием длительного лечения значительно потемнел цвет волос и ресниц.
Таким образом, гомоцистинурии свойствен прогредиентный характер течения патологического процесса. При рождении дети с гомоцистинурией, как правило, не имеют каких-либо внешних дефектов. Однако в результате наследственных нарушений метаболизма метионина постепенно начинают выявляться изменения в отдельных органах и системах. Прежде всего обращается внимание па задержку психомоторного развития, в последующем — па появление костных аномалий, изменения зрения и выраженную умственную отсталость.
Отсутствие на ранних этапах жизни ребенка полного симптомокомплекса, свойственного гомоцистинурии, нередко приводит к неправильной трактовке генеза заболевания (последствия перенесенной внутричерепной родовой травмы, менингоэнцефалита и т. п.).
Наши наблюдения показали, что имеется определенная зависимость клинической картины от возраста больного. Чем старше ребенок, тем больше органов и систем вовлекается в патологический процесс, и, как и при синдроме Марфана, речь идет, по-существу, о заболевании всего организма.
В статьях на сайте представлены оригинальные сведения, касающиеся только части наследственных заболеваний обмена аминокислот: нарушения метаболизма триптофана, фенилаланина, гистидина и метионина. В своей практической деятельности врач может встретиться и с другими нозологическими формами. Ведь в настоящее время известно более 60 ферментопатий, сопровождающихся изменениями обмена аминокислот: болезнь «кленового сиропа», гиперлизинемия, гиперпролипемия, гипервалинемия и пр.
При большинстве этих заболеваний, несмотря на разный уровень метаболических блоков и качественно иные метаболические расстройства, ведущим симптомом в клинической картине является задержка психомоторного развития и последующая умственная отсталость. Существует мнение, что все эти заболевания фенотипически сходны и без специальных лабораторных исследований врач не может их разграничить. Действительно, если исходить из характера поражений ЦНС, то эта точка зрения верна. Однако собственный опыт говорит о том, что для каждого заболевания аминокислотного обмена свойственно сочетание нарушений нервной системы и других органов и систем.
Сочетание отдельных признаков и создает нередко достаточно специфичную для каждой нозологической формы картину болезни. Так, например, болезнь «кленового сиропа» характеризуется не прогредиентным, а острым течением патологического процесса—«метаболическая катастрофа». Уже с первых часов жизни у ребенка обнаруживаются нарастающие неврологические расстройства (беспокойство, судороги и др.), напоминающие последствия внутричерепной родовой травмы.
На аутопсии нередко находят множественные очаги кровоизлияния в мозг, что как бы подтверждает прижизненный диагноз. Однако в отличие от травматических повреждений мозга у ребенка с этим метаболическим дефектом отмечаются чрезвычайно частые судорожные состояния (до 100 и более приступов в сутки), а моча имеет специфический запах «кленового сиропа». Назначение общепринятых противосудорожпых средств обычно бывает малоэффективным.
При гомоцистинурии речь идет не только об умственной отсталости, но также о вовлечении в болезненный процесс соединительной ткани, приводящей к костным деформациям, подвывиху хрусталиков и пр. В связи с этим как бы смещается значимость отдельных клинических симптомов. Резкое падение остроты зрения приводит к тяжелой инвалидизации больного и симптом поражения глаз как бы доминирует над нарушениями ЦНС. Это приводит к тому, что больные гомоцистинурией часто наблюдаются с диагнозом подвывиха хрусталиков у офтальмологов.
Дети, страдающие альбинизмом, как правило, психически развиваются удовлетворительно, но имеют характерный фенотип (светлорусые волосы, голубые глаза и неврологические расстройства— спонтанный нистагм, сниженное зрение и пр.). Следовательно, еще в долабораторном периоде врач но наблюдаемому у ребенка симптомокомплексу может предположить наличие наследственных нарушений обмена аминокислот и предпринять необходимые меры для целенаправленного лабораторного обследования пациента. Ото может быть убедительно проиллюстрировано на примере ФКУ, когда предварительный диагноз основывается только на симптомокомплексе внешних признаков у ребенка с задержкой психомоторного развития: светлые волосы, голубые глаза, белая депигментированпая кожа, своеобразный запах мочи.
Принципы диагностики и терапии при других наследственных нарушениях обмена аминокислот остаются такими же, как для ФКУ, гистидинемии и гомоцистинурии.
- Рекомендуем далее ознакомиться со статьей "Обмен углеводов у детей и его регуляция"
Оглавление темы "Болезни обмена у детей":- Поражение печени при гомоцистинурии
- Примеры гомоцистинурии у детей
- Обмен углеводов у детей и его регуляция
- Методы обследования обмена углеводов у детей
- История открытия галактоземии
- Варианты галактоземии и их причины
- Клиника галактоземии и степени ее тяжести
- Пример галактоземии у ребенка
- Обследование при галактоземии - диагностика
- Диспансерное наблюдение за детьми с галактоземией

