Витамин D-резистентный рахит (фосфат-диабет) у детей - причины, клиника
Витамин D-резистентный рахит, или фосфат-диабет, известен около 50 лет (Parson Fanconi, Albright и соавт., Dent). Однако только в 1958 году стало очевидно (Winters и соавт.), что заболевание следует относить к генетически детерминированным, и оно передается потомству, как сцепленное с Х-хромосомой. В отечественной литературе этому заболеванию посвящены работы Е. М. Фатеевой и соавт., М. А. Жуковского, М. П. Матвеева и соавт., М. С. Игнатовой и Ю. Е. Вельтищева и др.
Клинические проявления фосфат-диабета довольно полиморфны и фенотипи-чески напоминают прежде всего хорошо известный витамин D-дефицитный рахит. Первые симптомы обнаруживаются обычно в начале второго года жизни и характеризуются выраженной деформацией нижних конечностей и отставанием в физическом развитии, наличием рахитических «браслеток» на кистях рук и «четок» на ребрах, мышечной гипотонией, грубыми бокаловидными деформациями метафизов, остеопорозом и др..
При лабораторных исследованиях особенно часто обнаруживается гипофосфатемия (17—38 мг/л), повышение клиренса фосфатов и активности щелочной фосфатазы. Концентрация кальция крови не изменяется. Прогрессирующие костные деформации нередко приводят к тяжелой инвалидизации детей.
Согласно существующим представлениям, ведущим в патогенезе витамин D-резистентного рахита, является снижение реабсорбции фосфатов в почечных канальцах. По мнению Fanconi, первичный дефект реабсорбции фосфатов генетически обусловлен и проявляется в нарушении функции проксимальных извитых канальцев почек. Дефицит неорганических фосфатов приводит к нарушениям процессов минерализации костной матрицы, и как следствие этого наступает ограничение всасывания кальция в кишечнике.
Существует и другая точка зрения, согласно которой фосфатурия обусловлена не первичным дефектом канальцевой реабсорбции фосфатов, а нарушением всасывания кальция в кишечнике, вторичным гиперпаратиреоидизмом с последующим нарушением реабсорбции (Williams, Winters). Однако ряд фактов свидетельствует против патогенетической роли паращитовидных желез в генезе этого заболевания. Это прежде всего нормальный уровень кальция в сыворотке крови у большинства больных даже при длительном течении заболевания.
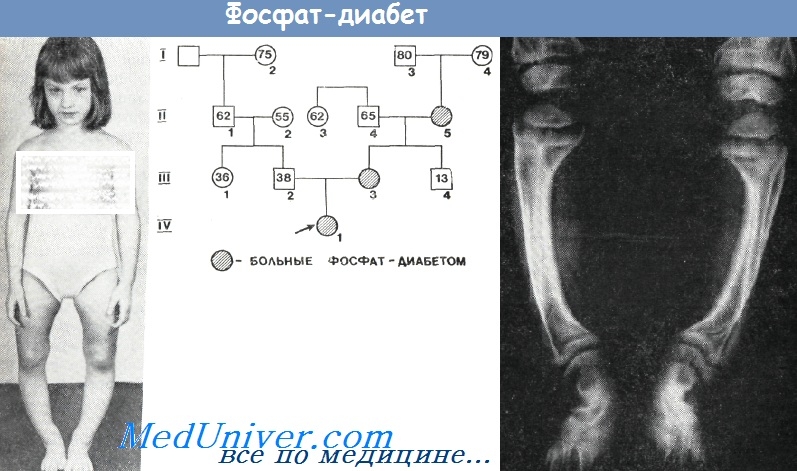
Гистологические и гистохимические исследования костной ткани при фосфат-диабете указывают на то, что причиной остеомаляции в первую очередь следует считать недостаток фосфора (Schreier), а не кальция. Первым этапом в процессе оссификации белковой матрицы является образование электростатических связей анионов фосфатов с аминогруппами коллагеновых волокон.
Длительный период времени оставалась неясной причина резистентности больных к витамину D, содержание которого в крови обычно не было изменено. В 1968 году Avioli и Birge высказали предположение, что основной причиной фосфатдиабета является врожденное нарушение метаболизма витамина D. Это послужило поводом усиления научных изысканий в этом направлении. Как известно, активным метаболитом витамина D2 является 25-оксихолекальциферол (исходная форма, образующаяся в печени). В 1970 году Fraser и Kodicek, применив радиоактивную метку 14С витамина D, показали, что циркуляционная форма 25-оксихолекальциферола в почках превращается в метаболит—1,25-диоксихолекальциферол, обладающий повышенной биологической активностью.
В 1973 году Fraser и соавт. склонились к гипотезе, согласно которой резистентность к витамину D вызвана генетическим дефектом 25-окси-холекальциферол-1-гидроксилазы — энзима, ответственного за продукцию 1,25-дигидроксивитамина D. Однако и эти солидно документированные гипотезы в настоящее время подверглись достаточно аргументированной критике (Haddad и соавт.). Наиболее приемлемой гипотезой считается, что избирательный дефект реабсорбции фосфата в почечных канальцах при фосфат-диабете связан не с нарушением образования стимулирующих эту систему активных метаболитов витамина D, а с изменением структуры белков, участвующих в механизме активного транспорта фосфора в почечных канальцах.
При фосфат-диабете, как и при других формах рахитоподобных заболеваний, в патологический процесс вторично вовлекается костная ткань, что способствует возникновению грубых скелетных деформаций.
Отдельные показатели обмена электролитов основного вещества и волокнистых структур соединительной ткани у больных фосфат-диабетом были изучены Л. В. Шиловым. При исследовании электролитов сыворотки крови у всех больных выявлено снижение концентрации неорганического фосфора от 26 до 36 мг/л и повышение активности щелочной фосфатазы (10—56 ед.). Отмечены значительные потери неорганического фосфора с мочой (более 30 мг/кг массы тела ребенка). Клиренс фосфатов достигал 34 мл/мин. Аналогичные изменения обнаружены у одного из родителей больных детей.
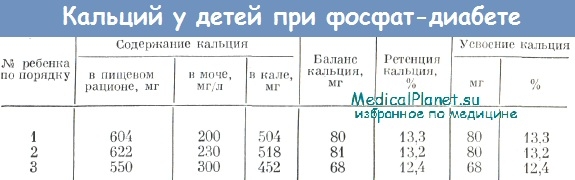
В то же время необходимо указать на то, что в отличие от детей с ПТЛ у больных фосфат-диабетом не изменялась концентрация в сыворотке крови ни общего кальция, ни его фракций. При проведении обменных балансовых исследований по определению ретенции кальция в кишечнике установлено, что усвоение кальция в кишечнике значительно снижено (12,4—13,3% при норме 30%) и повышен выброс кальция с калом (86,7% при норме 70%). Это свидетельствует о значительном снижении ретенции кальция и нарушении процессов его усвоения в кишечнике.
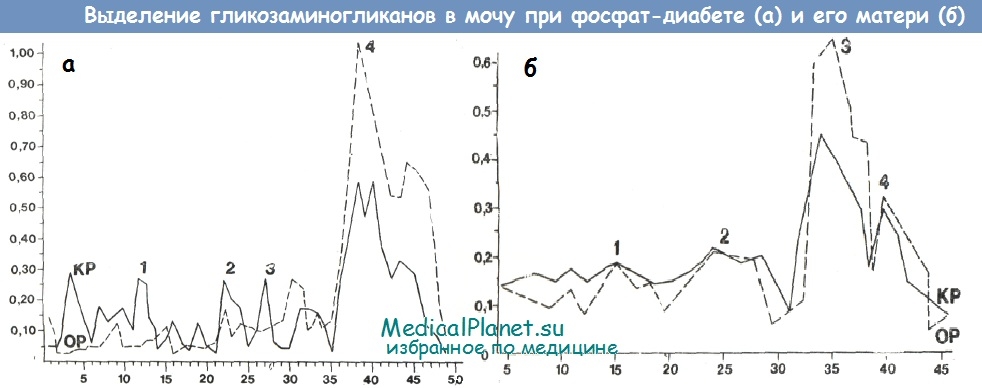
При изучении обмена веществ соединительной ткани Л. В. Шилов установил, что почечная экскреция кислых ГАГ и оксипролина при фосфат-диабете снижена. Так, суточная экскреция с мочой кислых ГАГ находилась в пределах 3,8—5,6 мг, а экскреция оксипролина — 26—42 мг. Следует, однако, заметить, что хроматограммы ГАГ мочи больных фосфат-диабетом отличались от хроматограмм больных с ПТА более высоким содержанием фракций хондроитинсульфатов А и С (40 и 70% соответственно) и сниженным карбазол-орциноловым коэффициентом в местах выхода этих фракций (от 0,2 до 0,4 соответственно).
Заслуживает внимания тот факт, что у родителей больных детей могут обнаруживаться сходные изменения хроматограмм кислых ГАГ мочи: «дерматаноподобный» характер хроматограмм, высокие пики экстинции уроновых кислот в местах выхода хондроитинсульфатов А, С и В.
Таким образом, проведенные исследования убедительно показали явную заинтересованность соединительной ткани в развитии вторичных нарушений опорно-двигательного аппарата при фосфат-диабете.
- Рекомендуем далее ознакомиться со статьей "Соединительная ткань при болезни де Тони-Дебре—Фанкони у детей"
Оглавление темы "Болезни обмена веществ у детей":- Вторичные поражения соединительной ткани - причины рахитоподобных поражений
- Соединительная ткань при почечно-тубулярном ацидозе (ПТА) у детей - клиника
- Витамин D-резистентный рахит (фосфат-диабет) у детей - причины, клиника
- Соединительная ткань при болезни де Тони-Дебре—Фанкони у детей
- Анализы для диагностики болезней соединительной ткани у детей
- Проблемы диагностики нарушений обмена веществ у детей
- Пренатальная диагностика нарушений обмена веществ у детей
- Скрининг нарушений обмена веществ у детей
- Скрининг-программы нарушений обмена веществ у детей
- Методы определения активности ферментов

