Отрицательный результат в иммуноцитохимии. Нейроэндокринная система в иммуноцитохимии
Если оказывается, что антитела (в частности, моноклональные), выбранные для работы с препаратами фиксированной и заключенной в парафин ткани, на самом деле не дают желаемого результата, а все другие компоненты системы вполне эффективны, можно предположить следующую схему. Сначала нужно проверить, сохраняется ли данный антиген в условиях фиксации и обработки ткани. Следует обратить внимание на обработку протеолитиче-скими ферментами. Если окраска по-прежнему неудовлетворительная, проверяют препарат антитела на срезах, фиксированных ацетоном, или на замороженных срезах. При отрицательном результате пробуют применить другую систему иммуномечения, проверяют условия хранения и срок годности антител, в конце концов обращаются на фирму, поставляющую препараты. Если результаты проверки антител на замороженных срезах положительные, то проверяют их на парафиновых срезах. В случае положительной реакции можно думать, что в исходном блоке ткани нет искомого антигена. Отрицательный результат при исследовании нового блока этой ткани указывает на неправильную фиксацию или обработку препаратов. В таком случае для выявления антигена необходимо изменить протокол. Когда метод отлажен, а положительный и отрицательный контроли дают ожидаемые результаты, но исход опыта отрицателен, можно предположить, что
• в ткани вообще нет антигена;
• содержание антигена настолько мало, что его нельзя обнаружить с помощью данного метода, а следовательно, нужно использовать более чувствительный метод;
• ткань перефиксирована или неправильно обработана и порезана. Это легко проверить, убедившись, что положительный контроль идентичен по своим характеристикам исследуемой ткани. В нашей лаборатории хранится серия блоков тканей (например, миндалин, кишечника), которые были фиксированы в течение разного времени в различных фиксаторах и могут использоваться как контроли в тех случаях, когда режим фиксации заведомо отличается от обычного.
Подтверждает общее правило, что прежде чем использовать новый метод, нужно освоить все его этапы в полном соответствии с протоколом, а прежде чем применять новую партию антител или систему Детекции, нужно ознакомиться с их характеристиками. Необходимо прочитать описание реактивов в прилагаемой инструкции, а также имеющие отношение к делу публикации. Если, судя по литературным данным, какие-то антитела используют только при работе с замороженными срезами, не стоит удивляться, что они не дают удовлетворительных результатов в случае фиксированных парафиновых срезов.
В этой статье мы рассмотрим методы изготовления иммуноцитохимических препаратов для электронной микроскопии на примере нейроэндокринной системы (НЭС).
Нейроэндокринная система — это рассеянный по всему организму комплекс, состоящий из клеток разного типа: эндокринных, паракринных, нервных, нейроэндокринных, которые продуцируют регуляторные факторы — пептиды и амины. Сюда относятся эндокринные клетки кишечника и поджелудочной железы, автономной нервной системы и эндокринных желез, например гипофиза. Электронная микроскопия уже давно играет главную роль в идентификации компонентов НЭС. Первые попытки классификации эндокринных клеток основывались в значительной мере на анализе ультраструктуры различных типов содержащихся в них секреторных гранул. Позже появились дополнительные данные, полученные с помощью гистохимических методов, в частности с помощью методов импрегнации серебром, позволяющих различать аргирофильные и аргентаффинные (серотонинсодержашие) гранулы. Применение световой микроскопии в иммуноцитохимии привело к созданию новых методов исследования НЭС. Сравнивая фотографии иммуноокрашенных полутонких срезов, полученные с помощью светового микроскопа, с электронно-микроскопическими фотофафиями соответствующих серийных ультратонких контрастированных срезов (метод полутонких/тонких срезов), удалось исследовать ультраструктуру клеток эндокринных тканей. Этот трудоемкий сравнительный метод позже уступил место электронно-микроскопической иммуноцитохимии.
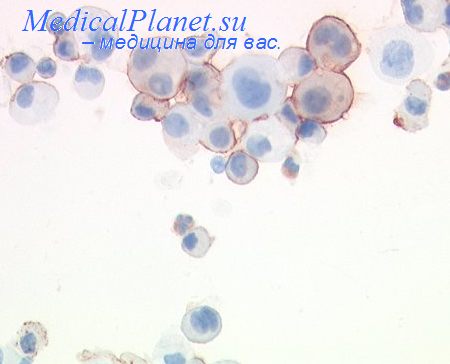
Одной из первых иммунологических меток, используемых в электронной микроскопии вслед за световой, была пероксидаза. При этом для получения электроноплотного продукта, пероксидазы—диаминобензидина, использовали тетроксид осмия. Сейчас этот и другие сходные методы уступают место методам с использованием соединений, меченных коллоидным золотом, которые имеют ряд преимуществ. В частности, можно получать частицы золота разного размера, что позволяет проводить на одном срезе несколько иммунологических реакций и идентифицировать их продукты даже в одной секреторной грануле. Поскольку клетки НЭС часто продуцируют несколько пептидов, такое множественное иммуномечение оказалось очень полезным, например при исследовании посттрансляционного процессинга пептидов.
Электронно-микроскопическая иммуноцитохимия не только позволяет получать ценную информацию о НЭС в норме, но и диагностировать многие патологии. Диагноз этих патологий, в частности новообразований, затруднен, поскольку картина злокачественного роста клеток не имеет четких характеристик, так что обычные гистологические методы часто оказываются неприменимыми. Нейроэндокринные новообразования могут секретировать огромные количества пептидов и аминов или, напротив, не секретировать их вообще; в обоих случаях содержание антигенов в них слишком мало, чтобы их можно было выявить с помощью светового микроскопирования иммуноокрашенных препаратов. Кроме того, может быть недостаточным количество ткани для анализа, например, если биоптат получен с помощью шприца или представляет собой отпечаток. В таких случаях более результативной является электронная микроскопия.
Аномальные клетки могут содержать секреторные гранулы с нарушенной ультраструктурой, и их выявление указывает на изменение иммунореактивности клеток. Таким образом, электронно-микроскопическая иммуноцитохимия может не только служить полезным дополнением к световой, но иногда является единственным способом идентификации аномальных клеток.
Используя методы электронно-микроскопической иммуноцитохимии в клинической диагностике, нужно иметь в виду, что в аномальных клетках вследствие нарушения путей биосинтеза часто синтезируются модифицированные пептиды. Поэтому для однозначной идентификации клеток того или иного типа и вырабатываемых ими продуктов необходим набор специфических антител, узнающих различные производные пептидных предшественников.
Эта статья может служить практическим руководством для тех исследователей, кто намерен использовать электронно-микроскопическую иммуноцитохимию для изучения биологии НЭС и выявления различных ее патологий.
- Читать далее "Иммуноцитохимия нервной системы. Приготовление препаратов в иммуноцитохимии"
Оглавление темы "Электронная иммуноцитохимия. Методы окращивания":1. Отрицательный результат в иммуноцитохимии. Нейроэндокринная система в иммуноцитохимии
2. Иммуноцитохимия нервной системы. Приготовление препаратов в иммуноцитохимии
3. Фиксация препаратов в иммуноцитохимии. Методы фиксации в иммуноцитохимии
4. Смолы в иммуноцитохимии. Фиксация препаратов смолами
5. Разведение антител в иммуноцитохимии. Хранение и использование антител
6. Иммуномечение. Непрямое иммуномечение коллоидным золотом
7. Мечение комплексом белок А — золото. Усиление с помощью серебра
8. Двойное окрашивание антителами меченными золотом. Техника двойного окрашивания антителами
9. Контроль в электронно-микроскопической иммуноцитохимии. Виды контроля в электронной иммуноцитохимии
10. Гибридизация in situ. Особенности гибридизации in situ

