Достижения геномики. Цели геномики.
Наибольший успех достигнут в секвенировании геномов патогенных для человека организмов и переносчиков заболеваний, что имеет непосредственное приложение к профилактике, диагностике и лечению инфекционных и трансмиссивных заболеваний. Уже секвенировано или частично секвенировано более 30 геномов важных бактерий и паразитов, среди которых Haemophilus influenzae, Saccharomyces cere-visae, Mycobacterium tuberculosis, Campylobacter jejuni, Escherichia coll, Vibrio cholerae, Mycobacterium leprae, Neisseria meningitidis, Streptococcus pneumoniae, Yersinia pestis, Salmonella tiphimurium.
В ближайшие 2—4 года ожидается завершение проектов по секвенированию более 100 других видов, среди которых Plasmodium falciparum. Leishmania, Tripanosoma brucei, Tripanosoma cruzi, Aspergillus fumigatus, Bacillus anthrax. Секвенированы практически все геномы вирусов и почти все белок-кодирующие районы геномов прокариот. Расшифровка вирусных геномов, знание механизмов инфицирования, репликации и формирования новых вирусных частиц, позволяют проектировать новые антивирусные лекарственные препараты, которые разрушают вирусный геном, мешая синтезу белков или блокируя передачу вируса из клетки в клетку. Широкое использование ПЦР для идентификации организмов, трудно выращиваемых в культуре, неоценимо для диагностики и контроля инфекционных заболеваний.
Например, ПЦР-метод позволяет отслеживать и оценивать активность инфекционного процесса до и по ходу лечения при вирусном гепатите С. С помощью микрочипов можно изучать экспрессию различных наборов генов у микробов и паразитов на разных фазах инфекции, анализировать механизмы вирулентности и устойчивости патогенов к защитным механизмам хозяина и лекарственным средствам.
Информация о характере генной экспрессии на разных стадиях клеточного цикла у патогенных микроорганизмов, обнаружение генов их вирулентности позволяет выявить новые точки возможного приложения лекарственной терапии. С помощью этого подхода, а также данных по секвенированию генома Plasmodium falciparum, удалось выявить блокатор ключевого для Plasmodium falciparum, метаболического пути, называемого DOXP. Данный путь характерен для всех растений и бактерий, но отсутствует у человека. Блокатор DOXP-пути - препарат фосмидомицин — эффективен против пслирезистентных к таниновым препаратам штаммов плазмодия и является родоначальником нового класса антималярийных лекарственных средств.
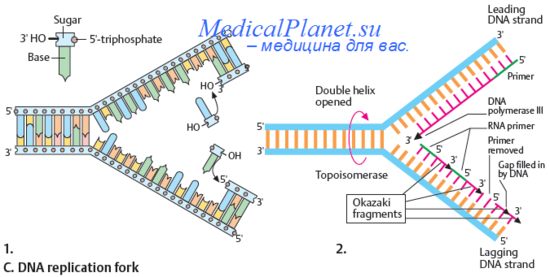
Секвенирование геномов патогенных организмов предоставляет информацию и о новых генах с неизвестной функцией, которые могут быть использованы для разработки не только новых классов диагностикумов и лекарственных средств, но и вакцин. Так, при секвенировании генома вирулентного штамма Neisseria meningitidis группы В, приводящего к гнойному менингиту, было определено свыше 500 поверхностно-экспрессирутошихся или секретирующихся белков (поверхностных антигенов). Соответствующие им последовательности ДНК. были клонированы и экспрессированы в бактериях, а продукты экспрессии, предположительно являющиеся значимыми поверхностными антигенами, использованы для иммунизации мышей. В результате появились две высоко устойчивые вакцины-кандидаты.
В настоящее время вакцины против Neisseria meningitidis групп А и С, широко используются в практике и присутствуют в календаре прививок. Продолжаются испытания на модельных объектах, в частности на мышах, кандидатных противотуберкулезных вакцин, одна из которых представляет собой фрагмент ДНК, кодирующий белок теплового шока М. tuberculosis (генная иммунизация). Эта вакцина не только защищает здоровых мышей от болезни, но и лечит уже инфицированных. Предварительное клиническое тестирование проходят и другие вакцины, основанные на ДНК: среди них вакцины для профилактики малярии. В настоящее время у животных проводится генная иммунизация для выработки иммунитета к некоторым вирусным патогенам (ВИЧ, вирусы гепатита, герпеса, бешенства) и малярийному плазмодию.
Определение полной нуклеотидной последовательности ДНК комара Anopheles gambiae, (переносчика малярии) позволит выявить различия в геномах комаров, связанные со способностью к передаче заболевания. Полученную информацию можно использовать для «конструирования» с помощью транспозонов таких особей, у которых эта способность снижена. Внедрение трансгенных комаров в природную экосистему приведет к снижению заболеваемости малярией,
Различия индивидуальных ответов организма хозяина на инфекционный агент, детерминированы генетически. Необходимо идентифицировать семейства генов, участвующих в модификации восприимчивости к заболеваниям. Например, в случае малярии это гены серповидноклеточности и наследственного овалоцитоза, что следует учитывать при оценке эффективности противомалярийной вакцины. Обнаружение мутаций, изменяющих структуру хемокинового рецептора (он участвует в проникновении ВИЧ в клетку) и проявляющихся выраженной резистентностью к СПИДу, послужило толчком к разработке нового подхода к терапии этого заболевания — создания аналога хемокинового рецептора, препятствующего проникновению вируса в клетки. Можно надеяться, что полученные знания о тонких механизмах организма против инфекционных агентов помогут нам в поиске наиболее логичных путей лечения большинства инфекционных болезней.
Анализируя вместе данные о структуре геномов патогенных организмов, геномов переносчиков заболеваний, а также генома человека, можно выявлять причины индивидуальных различий в восприимчивости к ряду заболеваний в человеческих популяциях. Такие исследования позволят более эффективно использовать информацию о распространении инфекционных заболеваний внутри тех или иных популяций и прогнозировать эпидемиологическую обстановку в отношении «новых» опасных инфекций, например, одного из вариантов болезни Крейтцфельда—Якоба, фатальной инсомнии, новых штаммов вируса гриппа, хантавирусов. Это обеспечит своевременную разработку новейших подходов к профилактике этих заболеваний.
Ценная информация может быть получена при расшифровке геномов таких хорошо изученных биохимически и генетически модельных организмов, как нематода Caenorhabdilis etegans, плодовая мушка Drosophila melanogaster и дрожжи Saccharomyces cerevisae.
Известно, например, что процессы старения могут быть связаны с ослаблением механизмов защиты от вредных воздействий эндогенных и экзогенных оксидантов на ДНК и белки. Такая физиологическая система может быть чрезвычайно консервативной и присутствовать у эволюционно далеких видов. И действительно, у дрозофилы обнаружена копия аллельного варианта гена нематоды (daf2), участвующего в процессе старения.
Простота генома рыбки Danio также открывает хорошие перспективы для идентификации и изучения функций генов, которые сохранились на протяжении эволюции. Для идентификации кодирующих последовательностей и регуляторных районов в геноме человека и патогенных организмов наибольшее значение играет изучение генома мыши. Это связано с наличием у мыши и человека больших сегментов хромосом, имеющих одинаковый порядок расположения генов (синтения). К тому же ряд болезней мыши сходны с таковыми у человека. Используя методику эмбриональных стволовых клеток, можно «нокаутировать» гены по одному и исследовать их функции, а также воспроизводить не существующие в природе у мыши аналоги заболеваний человека. Изучение вариаций клинического фенотипа моногенных болезней на мышах, подвергнутых аутбридингу, позволяет выявлять гены, меняющие течение таких заболеваний, и находить аналогичные гены-модификаторы у человека. Таким образом, мыши служат хорошей моделью при расшифровке молекулярных механизмов патогенеза как моногенных, так и сложных мультифакториальных заболеваний. Чрезвычайно полезны они и при испытании новых лекарственных средств.
- Читать далее "Перспективы геномики. Фармакогеномика."
Оглавление темы "Геномика. Медицинская генетика.":1. Стратегия картирования генов человека. Методы полногеномного скрининга.
2. Геномика. Виды геномики. Задачи геномики.
3. Достижения геномики. Цели геномики.
4. Перспективы геномики. Фармакогеномика.
5. Биоэтические проблемы геномики. Деонтология и геномика.
6. Медицинская генетика. Задачи медицинской генетики.
7. Наследственные болезни. Классификация наследственных болезней.
8. Гинеалогический метод. Клинико-генеалогический метод.
9. Близнецовый метод. Задачи и методика близнецового метода.
10. Популяционные методы медицинской генетики. Статистические методы медицинской генетики.

