Третичная и четвертичная структура белков. Ион-индуцированный диполь и диполь-индуцированный диполь
Под третичной структурой белка понимают пространственное расположение полипептидной цепи, т. е. его конформацию. В формировании третичной структуры важную роль играют нековалентные взаимодействия между спиральными и Р-структурными участками, образованными неполярными остатками аминокислот.
Если белок содержит не одну, а несколько субъединиц (полипептидных цепей), то их взаимное расположение в пространстве называется четвертичной структурой белка.
Третичная структура белка, характеризующаяся определенным расположением аминокислотных остатков в пространстве, определяет функциональную активность белка. Четвертичная структура белка важна в первую очередь как регуляторный фактор. Отдельные субъединицы белка, образующие его четвертичную структуру, называются протомерами, а сами белки, состоящие из нескольких протомеров, — олигомерами. Все белки, содержащие более чем одну субъединицу, являются аллостери-ческими белками, т. е. такими, функциональная активность которых регулируется при изменении конформации субъединиц в результате связывания с каким-либо реагентом (лигандом). Субъединицы в молекуле белка не всегда бывают идентичными: известно много случаев, когда одна субъединица обладает каталитической активностью, а друга выполняет регуляторную функцию, активируя или ингибируя каталитическую субъединицу.
Взаимодействие ион-индуцированный диполь возникает как результат влияния иона на неполярную молекулу. При этом заряд иона индуцирует превращение неполярной молекулы в диполь, в результате чего возникает взаимодействие, несколько более слабое, чем ион-диполь.
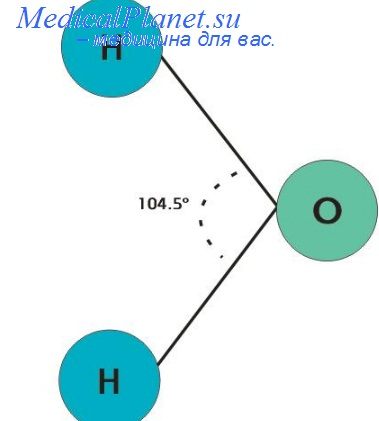
Притяжение может существовать и между двумя диполями. Такое взаимодействие (диполь-диполь) обусловливает ориентацию молекул друг относительно друга и, возможно, играет важную роль в процессах сборки.
Диполь также может индуцировать превращение неполярных молекул в диполи. Взаимодействия диполь-индуцированный диполь относятся к числу слабейших.
Наконец, две неполярные молекулы могут притягиваться друг к другу вследствие того, что происходит взаимная индукция диполей. Хотя электроны в нейтральной молекуле распределены вокруг ядра равномерно, если рассматривать такую молекулу в течение длительного времени, однако, в каждый данный момент существует значительная вероятность того, что центр отрицательного заряда не будет совпадать с центром положительного заряда. Отсюда и возможность существования мгновенных диполей, которые, пусть временно, но могут индуцировать превращение ближайших молекул в такие же диполи. Между диполями в такой системе возникает слабое притяжение. Это так называемые дисперсионные силы; именно за счет этих сил такие газы как Н2, N2 или Не, имеющие неполярные молекулы, могут при надлежащих значениях температуры и давления переходить в жидкое состояние.
Итак, важная особенность вандерваальсовых взаимодействий между органическими молекулами состоит в том, что все они обусловлены слабыми силами, действующими только на малых расстояниях; именно этим силам принадлежит, однако, выдающаяся роль в определении биологической структуры, биологической специфичности и характера биохимических реакций. Общий эффект складывается, естественно, из взаимодействий различных типов.
Изучая кристаллы различных органических молекул с помощь методов дифракции рентгеновских лучей и дифракции нейтронов, удалось показать, что расстояние между атомом водорода и электроотрицательным атомом меньше вандерва-альсова радиуса электроотрицательного атома. Когда впервые с помощью рентгеноструктурного анализа, (который не дает возможности установить локализацию атома водорода), определили расстояние между двумя атомами кислорода, оказалось что оно лежит в пределах 2,75—2,45 А. Это меньше вандерваальсова расстояния между двумя атомами кислорода (2,8 А) и гораздо больше расстояния между двумя ковалентно связанными атомами кислорода (1,4 А). Отклонения можно было объяснить допустив, что между двумя атомами кислорода помещается атом водорода. Так возник термин водородная связь.
- Читать далее "Стереоспецифичность связывания лигандов. Пространственная конфигурация заместителей"
Оглавление темы "Структура белков в организме":1. Термодинамика фармакологии. Классическая термодинамика
2. Термохимия. Второй закон термодинамики в фармации
3. Термодинамическое равновесие. Критерии равновесия в фармации
4. Строение воды. Водородные связи воды
5. Комплементарность связывания лекарств. Связывание лекарств в организме
6. Гидрофобность лекарств. Мембранные белки и лекарства
7. Вторичная структура белков. Организация полипептидной цепи
8. Третичная и четвертичная структура белков. Ион-индуцированный диполь и диполь-индуцированный диполь
9. Стереоспецифичность связывания лигандов. Пространственная конфигурация заместителей
10. Конформация белков в организме. Конформация лиганд в фармакологии

