Механизмы защиты вирусов, бактерий от иммунитета
Гуморальный и клеточный иммунные ответы организма для защиты от инфекции были обсуждены в отдельных статьях на сайте (рекомендуем пользоваться формой поиска выше). Как известно, микроорганизмы разработали способы сопротивления и уклонения от действий иммунной системы, что во многом определяет вирулентность и патогенность. Эти механизмы включают:
(1) рост в нишах, недоступных для иммунной системы;
(2) антигенную вариабельность;
(3) устойчивость к врожденной иммунной защите;
(4) подавление эффективности Т-клеточного иммунного ответа с помощью специфической или неспецифической иммуносупрессии.
Некоторые микроорганизмы реплицируются в местах, недоступных для иммунного ответа организма-хозяина. Микроорганизмы, размножающиеся в просвете кишечника (например, токсинпродуцирующая С. difficile) или желчного пузыря (например, S. typhi), недоступны для клеточно-опосредованного иммунного ответа.
Некоторые микроорганизмы быстро проникают в клетки организма-хозяина, до того как гуморальный иммунитет станет эффективным (например, спорозоиты малярии, входящие в клетки печени, Trichinella spp. и Т. cruzi, проникающие в клетки скелетных или сердечных мышц). Некоторые крупные паразиты (например, личинки ленточных червей) формируют в тканях человека цисты, покрытые прочной капсулой, и таким образом становятся недоступными для иммунных клеток и антител.
Латентный период заболевания — радикальная стратегия вируса для уклонения от иммунной защиты в этот период многие вирусные антигены не экспрессируются.
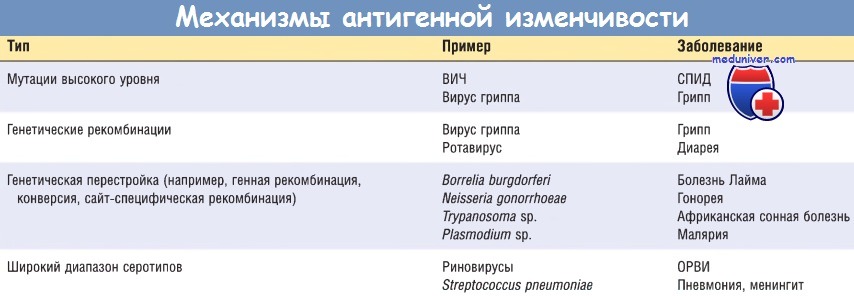
Некоторые микробы уклоняются от иммунного ответа, изменяя свои антигены. Нейтрализующие антитела блокируют способность микробов инфицировать клетки и активируют механизмы уничтожения патогенов. Для того чтобы избежать узнавания, микробы вовлекают генетические механизмы в создание антигенной вариабельности. Низкая специфичность вирусной РНК-полимеразы (при ВИЧ-инфекции и многих респираторных вирусах, включая грипп) и рекомбинация вирусного генома (например, вируса гриппа) обусловливают вирусную антигенную вариабельность.
Спирохеты В. recurrentis неоднократно меняют свои поверхностные антигены, а В. burgdorferi, вызывающие болезнь Лайма, используют подобные механизмы для изменения белков наружной мембраны. Штаммы Trypanosoma sp. имеют множество генов, кодирующих основной поверхностный антиген, названный вариабельным поверхностным гликопротеином, и, соответственно, могут изменять экспрессию этого белка. Известны около 80 серотипов S. pneumoniae, и каждый имеет свой, отличный от других капсульный полисахарид.
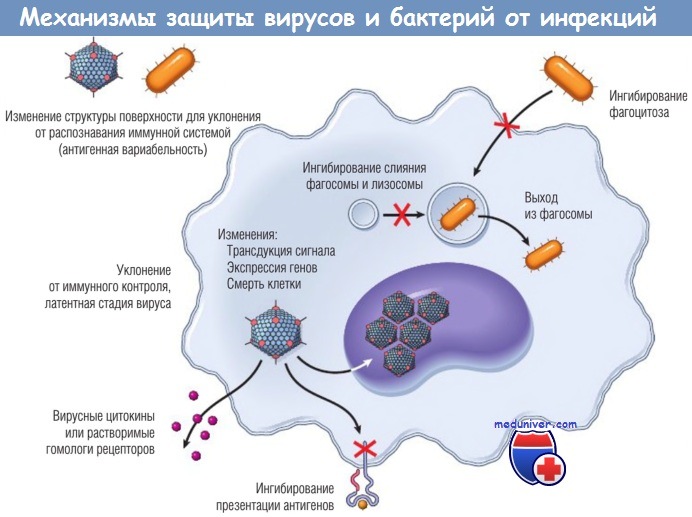
Некоторые микроорганизмы научились уклоняться от врожденного иммунитета, например избегать киллинга фагоцитами с участием компонентов системы комплемента. Катионные антимикробные пептиды (дефензин, кателицидин и тромбоцидин) обеспечивают важную начальную защиту от внедрения микроорганизмов. Резистентность к этим антимикробным пептидам является ключевым фактором вирулентности многих патогенов, позволяя им избежать киллинга нейтрофилами и макрофагами.
Наличие углеводной капсулы на поверхности многих бактерий, вызывающих пневмонию или менингит (пневмококков, менингококков, Н. influenzae), делает их более вирулентными, ограждая антигены бактерий и препятствуя их фагоцитозу нейтрофилами. Например, Е. coli с капсулой К1, содержащей сиаловую кислоту, вызывает менингит у новорожденных. Сиаловая кислота не связывается с белком С3b, который необходим для активации системы комплемента по альтернативному пути. Так бактерия уклоняется от комплемент-опосредованного лизиса и опсонизации, приводящей к фагоцитозу.
Многие бактерии продуцируют токсичные белки, которые поражают фагоциты, предотвращают их миграцию или уменьшают окислительный стресс. Бактерии также могут «обмануть» иммунную систему, покрываясь собственными белками организма-хозяина. Некоторые бактерии, включая Salmonella spp., могут изменять липидную структуру липополисахаридов, что уменьшает активацию TLR. S. aureus покрыт молекулами А-белка, который связывает фрагмент Fc антител и таким образом ингибирует фагоцитоз.
Бактерии Neisseria spp., Haemophilus spp. и Streptococcus spp. секретируют протеазы, разрушающие антитела. Как уже упоминалось, другой успешный способ уклонения от иммунного ответа заключается в репликации возбудителей внутри фагоцитарных клеток. Множество вирусов, некоторые внутриклеточные бактерии (включая микобактерии, листерии и легионеллы), грибы (например, С. neoformans) и простейшие (например, лейшмании, трипаносомы, токсоплазмы) способны к размножению внутри фагоцитов.
Вирусы могут продуцировать молекулы, ингибирующие врожденный иммунитет. Некоторые вирусы (например, герпес-вирусы и поксвирусы) вырабатывают белки, блокирующие активацию системы комплемента. Вирусы разработали большое количество стратегий для борьбы с IFN, ранней иммунной защитой организма от вирусов. Некоторые вирусы продуцируют растворимые гомологи рецепторов IFN-a и IFN-Р или IFN-y, которые связываются и ингибируют антивирусные эффекты IFN, либо производят белки, ингибирующие внутриклеточный сигнальный путь JAK/STAT рецепторов IFN.
Вирусы могут также инактивировать или ингибировать ключевой медиатор антивирусного действия IFN — протеинкиназу, зависимую от двухцепочечной РНК. Некоторые вирусы кодируют в своем геноме гомологи других цитокинов и хемокинов или их рецепторов, способные различными путями ингибировать иммунный ответ.
Некоторые микроорганизмы продуцируют факторы, которые делают невозможным распознавание инфицированных клеток хелперными Т-клетками CD4+ и цитотоксическими Т-клетками CD8+. Так, некоторые ДНК-содержащие вирусы (например, герпес-вирусы, включая HSV, CMV и EBV) могут связываться или изменять локализацию молекул МНС класса I, нарушая презентацию антигенов Т-клеткам CD8+.
Снижение экспрессии молекул МНС класса I могло бы сделать инфицированные клетки мишенями для NK-клеток, однако герпес-вирусы также экспрессируют вещества, гомологичные молекул МНС класса I, которые действуют как эффективные ингибиторы NK-клеток. Аналогично герпес-вирусы могут сделать мишенью молекулы МНС класса II с целью ранней их деградации и нарушения презентации антигена хелперным Т-клеткам CD4+. Вирусы также могут инфицировать лейкоциты и непосредственно нарушать их функции: ВИЧ поражает Т-лимфоциты CD4+, макрофаги и дендритные клетки, а EBV инфицирует В-лимфоциты.
- Вернуться в оглавление раздела "Патофизиология"
Оглавление темы "Патофизиология инфекционных болезней":- Средства биотерроризма и биологического оружия
- Виды входных ворот инфекций
- Пути распространения инфекции в организме
- Пути выхода инфекции из организма хозяина
- Виды инфекций передающихся половым путем (ИППП)
- Механизмы защиты организма от инфекций
- Как вирусы вызывают инфекцию?
- Как бактерии вызывают инфекцию?
- Механизмы повреждения тканей иммунитетом
- Механизмы защиты вирусов, бактерий от иммунитета

