Механизм развития (патогенез) вирусного гепатита В
Вирус гепатита В (HBV) может вызывать:
(1) острый гепатит с последующим выздоровлением и элиминацией вируса;
(2) непрогрессирующий хронический гепатит;
(3) прогрессирующий хронический гепатит с исходом в цирроз печени;
(4) молниеносный гепатит с массивными некрозами печени;
(5) бессимптомное носительство.
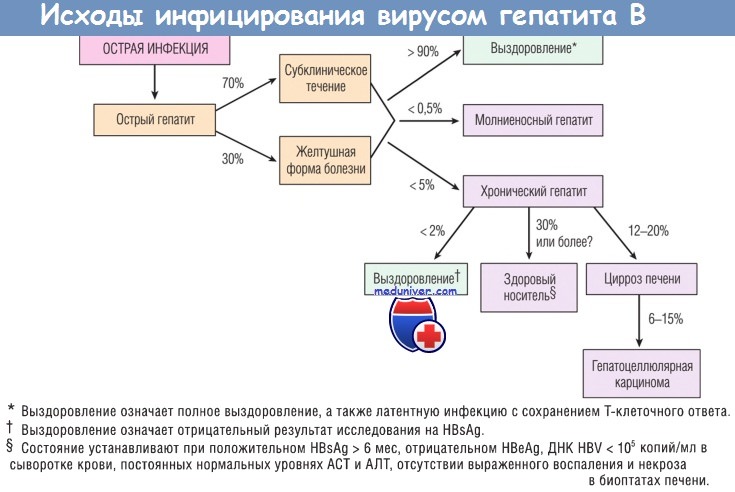
HBV-индуцированная хроническая болезнь печени предшествует ГЦК. Частота различных клинических исходов при инфицировании HBV представлена на схеме ниже.
Заболевания печени, возникающие в результате инфицирования HBV, представляют собой серьезную общемировую проблему. Около 30% населения земного шара (2 млрд человек) инфицированы HBV, при этом 400 млн человек имеют хроническое заболевание. 75% из них проживают в Азии и странах западного побережья Тихоокеанского бассейна.
Частота хронического гепатита В в мире варьирует от высокой (> 8%) в Африке, Азии и странах западного побережья Тихоокеанского бассейна до средней (2-7%) в странах Южной и Восточной Европы и низкой (< 2%) в Западной Европе, Северной Америке и Австралии.
Далее будет показано, что частота вирусоносительства обусловлена возрастом инфицирования: наибольшая — при перинатальном инфицировании и наименьшая — в случае инфицирования взрослых. В США частота HBV-инфекции стремительно увеличивается. В настоящее время ежегодно выявляют 46 тыс. новых случаев заболевания вирусным гепатитом В, при этом 5000 наблюдений — острая симптомная форма.
Путь передачи HBV зависит от географического региона. Так, в областях с высокой распространенностью HBV в 90% случаев отмечают вертикальный путь передачи вируса (во время родов). В регионах с умеренной распространенностью основным путем передачи является горизонтальный (при контакте с больным), особенно в раннем детском возрасте. В областях с низкой распространенностью, таких как США, вирус в основном передается при незащищенных гетеросексуальных или гомосексуальных половых контактах и внутривенном введении наркотических препаратов (при совместном использовании игл и шприцев).
Доля распространения инфекции при переливании крови в последние годы значительно сократилась благодаря скринингу донорской крови и доноров на HBsAg, а также отказу от оплачиваемого донорства крови.
Инфекция, вызванная HBV, характеризуется длительным инкубационным периодом (4-26 нед). В отличие от HAV, HBV определяется в крови как до активной фазы острого и хронического гепатитов, так и во время нее. В США острая HBV-инфекция наблюдается преимущественно у взрослых. У 70% лиц заболевание течет бессимптомно или с незначительными симптомами, а желтухи нет. У 30% присутствуют неспецифические общие симптомы: отсутствие аппетита, лихорадка, желтуха и боль в правом верхнем квадранте живота. Почти во всех случаях инфекция самокупируется и вирус элиминируется без лечения. Хроническое заболевание редко развивается у взрослых в неэндемичных регионах. Молниеносный гепатит также не распространен (0,1-0,5%).
Впервые связь между HBV и развитием гепатита была установлена в 1960-х гг., когда был открыт австралийский антиген (более известный как HBsAg). Вирус является членом семейства ДНК-вирусов Hepadnaviridae, вызывающих гепатит у многих видов животных. HBV имеет 8 генотипов, распределенных географически особым образом. Зрелый вирион HBV представляет собой сферическую, диаметром 42 нм, двухслойную частицу Дейна, внешняя оболочка которой состоит из белков, липидов и углеводов и окружает электронно-плотное, слегка гексагональное ядро диаметром 28 нм. Геном HBV представлен частично циркулярной двухцепочечной молекулой ДНК, состоящей из 3200 нуклеотидов.
Геном вируса гепатита В (HBV) имеет 4 открытые рамки считывания, кодирующие:
- нуклеокапсидный коровый белок (HBcAg, или сердцевинный белок, кор-антиген HBV) и длинный полипептидный транскрипт с прекоровым и коровым участками, обозначаемый как HBeAg (антиген «е» HBV). Прекоровый участок обеспечивает секрецию полипептида HBeAg в кровь, тогда как HBeAg остается в гепатоцитах для сборки полного вириона;
- гликопротеины оболочки (HBsAg, или поверхностный антиген HBV), которые представлены тремя родственными белками: крупным HBsAg (содержит участки пре-Sl, npe-S2 и S), средним HBsAg (содержит участки npe-S2 и S) и малым HBsAg (содержит только участок S). Инфицированные гепатоциты способны синтезировать и секретировать большое количество не обладающих инфекционностью поверхностных белков (главным образом малых HBsAg);
- полимеразу, которая действует и как ДНК-поли-мераза, и как обратная транскриптаза. Репликация генома вируса происходит через матрицу промежуточной РНК в процессе уникального репликационного цикла: ДНК - РНК - ДНК;
- белок НВх, который необходим для репликации вируса и может действовать как активатор транскрипции вирусных генов и большого числа генов организма-хозяина. Этот белок играет определенную роль в патогенезе рака печени при инфицировании HBV.
При естественном течении заболевания могут определяться следующие сывороточные маркеры:
- HBsAg. Появляется до развития симптомов, достигает пика во время развернутой картины заболевания, затем в течение 3-6 мес его уровень постепенно снижается, после чего этот антиген не определяется;
- анти-HBs антитела. Не выявляются вплоть до конца острого периода заболевания и обычно не определяются в течение нескольких недель или даже месяцев после исчезновения HBsAg. Анти-HBs антитела могут персистировать всю жизнь, обеспечивая защиту организма. Это является основой стратегии вакцинации с использованием неинфекционного HBsAg;
- HBeAg, ДНК HBV и ДНК-полимераза. Появляются в сыворотке вскоре после появления HBsAg и указывают на активную репликацию вируса. Персистирование HBeAg является важным показателем продолжающейся репликации вируса, инфекционности и риска развития хронического гепатита. Появление анти-НВе антител означает, что острая инфекция достигла своего пика и идет на убыль;
- анти-НВс IgM. Начинают определяться в сыворотке крови незадолго до развития симптомов, одновременно с повышением уровня трансаминаз (что указывает на разрушение гепатоцитов). По истечении нескольких месяцев анти-НВс IgM замещаются анти-НВс IgG. Как и в случае с анти-HAV антителами, отсутствует прямой метод, выявляющий анти-НВс IgG, но их наличие подразумевается, когда снижается уровень анти-НВс IgM при подъеме общего уровня анти-НВс антител.
Иногда возникают мутантные цепи HBV, которые не продуцируют HBeAg, но обеспечивают полноценную репликацию вируса, что подтверждается экспрессией HBeAg. У таких пациентов уровень HBeAg может быть низким или антиген может вообще не определяться, несмотря на наличие в организме вирусов. Еще одна опасная особенность эволюции инфекции — появление мутантных форм вируса, которые не связываются с нейтрализующими их моноклональными антителами к классическим антигенным детерминантам вириона, реплицирующимися при наличии поствакцинального иммунитета. Например, в одном таком вирусном мутанте замещается аминокислота аргинин в 145-м положении HBsAg на глицин, что значительно затрудняет распознавание HBsAg антителами к HBsAg.
Недавние исследования показали, что, несмотря на самокупирование острой HBV-инфекции, в крови некоторых лиц, имеющих анти-НВе антитела, можно определить методом ПЦР очень низкий уровень ДНК HBV (известно, что ДНК HBV может персистировать в течение многих лет). При этом неясно, какова природа этого вирусного материала: является ли он фрагментом вируса или заразным либо незаразным вирусом.
Иммунный ответ организма на внедрение вируса является главным и решающим фактором исхода заболевания. Механизмы врожденного иммунитета защищают организм во время начальной фазы инфекции, а выраженный ответ вирус-специфических Т-клеток CD4+ и CD8+, продуцирующих IFN-y, сочетается с разрешением острой инфекции. Есть основания полагать, что HBV не повреждает печень непосредственно, поскольку у многих хронических больных в гепатоцитах есть вирионы, однако признаки повреждения клеток печени отсутствуют. Считается, что повреждение гепатоцитов происходит вторично в результате воздействия цитотоксических Т-лимфоцитов CD8+ на инфицированные клетки.
Развитие гепатита В можно предотвратить путем вакцинации и скрининга донорской крови, органов и тканей. Вакцину изготавливают из очищенного HbsAg, вырабатываемого дрожжевыми грибами. Вакцинация способствует развитию защитного иммунного ответа в виде выработки анти-HBs антител у 95% новорожденных, детей и подростков. Всеобщая вакцинация имела большой успех в Тайване и Гамбии, но, к сожалению, ее не проводят во всех странах.
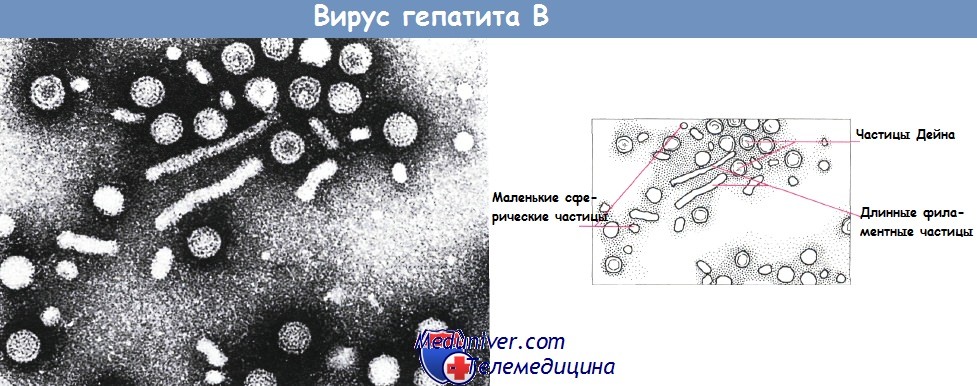
На срезе видны мелкие сферические частицы с диаметром 28 нм (HBsAg); более крупные сферические двумембранные частицы Дейна (42 нм), продолговатые филаментозные частицы.
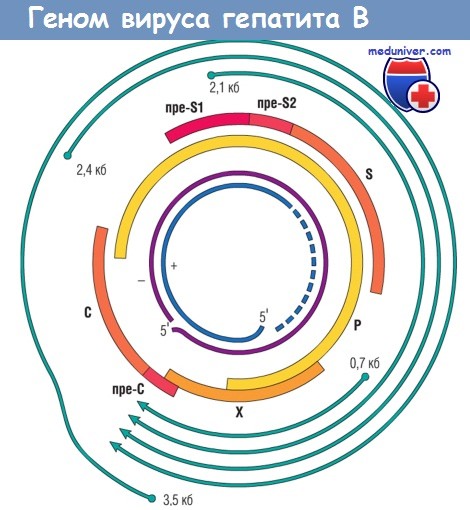
Две внутренние линии — две цепочки ДНК вириона: положительная (+) и отрицательная (-).
Широкие линии обозначают пептиды, образованные вирионом: Р, X, пре-С, С, пре-S1, пре-S2 и S.
Наружные линии — копии мРНК вириона.
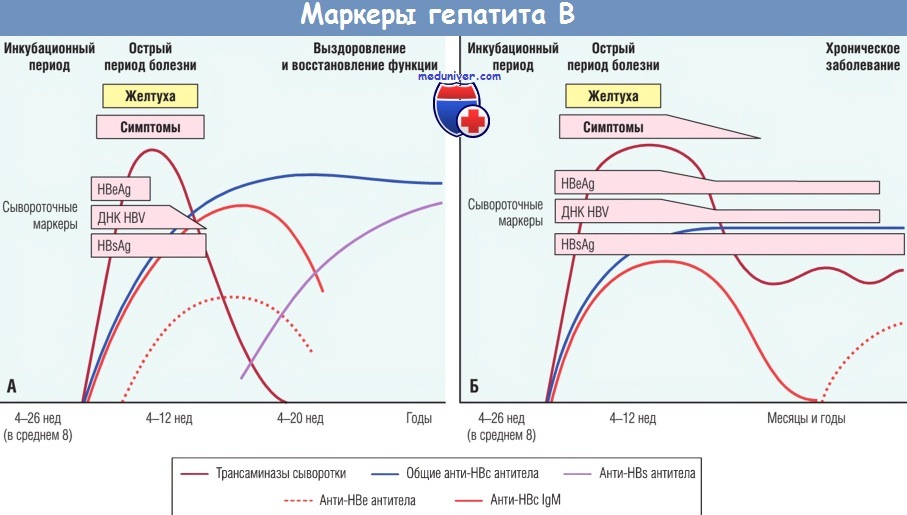
указывающих на острую инфекцию с выздоровлением (А) и прогрессирование в хроническую инфекцию (Б).
HBV — вирус гепатита В; Ig — иммуноглобулин; ДНК — дезоксирибонуклеиновая кислота.
Видео этиология, патогенез, диагностика вирусного гепатита А, В, С, Д, Е
- Рекомендуем ознакомиться со следующей статьей "Механизм развития (патогенез) вирусного гепатита С"
Оглавление темы "Патогенез болезней печени":- Механизм развития (патогенез) желтухи
- Механизм развития (патогенез) холестаза
- Механизм развития (патогенез) вирусного гепатита А
- Механизм развития (патогенез) вирусного гепатита В
- Механизм развития (патогенез) вирусного гепатита С
- Механизм развития (патогенез) вирусного гепатита D
- Механизм развития (патогенез) вирусного гепатита Е
- Механизм развития (патогенез) вирусного гепатита G
- Клинико-патологические синдромы вирусных гепатитов
- Морфология острого вирусного гепатита

