Механизмы удаления микробов и мертвых клеток из очага воспаления
Распознавание микробов и мертвых клеток рецепторами индуцирует активацию лейкоцитов. Активация является следствием запуска сигнальных путей лейкоцитов, приводящего к повышению содержания Са2+ в цитозоле и активации таких ферментов, как протеинкиназа С и фосфолипаза А2.
Функциональные ответные реакции, которые наиболее важны при разрушении микробов или других повреждающих агентов, — это фагоцитоз и внутриклеточный киллинг. В защитной функции воспаления участвуют и другие ответные реакции, которые могут вносить свой вклад в повреждения.
а) Фагоцитоз. Фагоцитоз в своем развитии проходит три последовательных этапа:
(1) распознавание и связывание частицы, которую должен поглотить лейкоцит;
(2) поглощение частицы с последующим формированием фагоцитарной вакуоли (фагосомы) и фаголизосомы;
(3) киллинг или деградация поглощенной частицы.
Функция маннозных рецепторов, скавенджер-рецепторов и рецепторов к различным типам опсонинов состоит в связывании и поглощении микробов. Макрофагальный маннозный рецептор лектин связывает концевые маннозные и фукозные остатки гликопротеинов и гликолипидов.
Эти сахара являются типичными частями молекул стенки микробных клеток, а гликопротеины и гликолипиды млекопитающих содержат концевую сиаловую кислоту или N-ацетилгалактозамин, поэтому маннозный рецептор распознает микробную клетку, а не клетку организма. Скавенджер-рецепторы впервые были выделены как молекулы, связывающие и опосредующие эндоцитоз окисленных или ацетилированных частиц липопротеинов низкой плотности (ЛПНП), которые больше не могли взаимодействовать с обычным рецептором ЛПНП.
Помимо модифицированных частиц ЛПНП макрофагальные скавенджер-рецепторы связывают разнообразные микробы. Интегрины макрофагов, особенно Мас-1 (CD11b/CD18), также могут связывать микробы для фагоцитоза.
Эффективность фагоцитоза значительно увеличивается после опсонизации микробов специфическими белками (опсонинами), для которых фагоциты экспрессируют высокоаффинные рецепторы. Основными опсонинами являются антитела IgG, продукты распада компонента С3b системы комплемента и определенные лектины плазмы крови, особенно маннансвя-зывающий лектин. Все они распознаются специфическими рецепторами на лейкоцитах.
б) Поглощение. После присоединения частицы к рецепторам фагоцита ее окружают псевдоподии (цитоплазматические выросты), а цитоплазматическая мембрана обжимает ее и формирует фагосому, поглощающую эту частицу. Затем фагосома сливается с лизосомой и содержимое лизосомы (ее ферменты) переходит в фаголизосому. Во время этого процесса фагоцит может высвобождать содержимое лизосом и во внеклеточное пространство.
Процесс фагоцитоза сложен, для него необходима интеграция многих рецептор-инициированных сигналов, ведущих к ремоделированию мембран и изменению цитоскелета. Фагоцитоз зависит от полимеризации актиновых филаментов, поэтому неудивительно, что многие сигналы, запускающие фагоцитоз, участвуют и в хемотаксисе. (В отличие от этого пи-ноцитоз и рецептор-опосредованный эндоцитоз мелких частиц зависят от интернализации посредством клатрин-покрытых везикул и не зависят от актиновых филаментов цитоскелета.)
в) Киллинг или деградация. Финальный этап элиминации инфекционных агентов или некротических клеток — их киллинг либо деградация внутри нейтро-филов или макрофагов, что происходит с наибольшей эффективностью после активации фагоцитов. Киллинг микробов осуществляют АФК и активные формы азота, в основном NO.
Образование АФК в основном происходит благодаря быстрой сборке и активации многокомпонентной NADPH-оксидазы (оксидазы фагоцита), которая окисляет NADPH и при этом восстанавливает кислород до О2. Эту быструю окислительную реакцию в нейтрофилах называют респираторным стрессом. Она запускается активирующими сигналами и сопровождает фагоцитоз. Оксидаза фагоцита — ферментный комплекс, содержащий как минимум 7 белков. В неактивных нейтрофилах разные компоненты фермента располагаются в цитоплазматической мембране и цитоплазме.
В ответ на активирующий стимул цитозольные белковые компоненты транслоцируются к фагосомной мембране, где соединяются и формируют функционирующий ферментный комплекс. Таким образом АФК продуцируются внутри лизосомы, где сегрегируются поглощенные субстанции, а собственные органеллы клетки защищены от повреждающего действия АФК. Затем О2 превращается в Н2O2, преимущественно спонтанным диспропорционированием. Н2O2 не может сам эффективно убивать микробы, но азурофильные гранулы нейтрофилов содержат фермент миелопероксидазу, который в присутствии таких галоидов, как Cl-, превращает Н2O2 в гипохлорит (активный компонент отбеливателей).
Последний является потенциальным антимикробным агентом, разрушающим микробы галогенированием (при котором галоид ковалентно связывается с клеточным содержимым) или окислением белков и липидов (перекисным окислением липидов).
Система Н2O2-миелопероксидаза-галоген является самой эффективной бактерицидной системой нейтрофилов. Н2O2 также может превращаться в ОН — другой мощный повреждающий агент.
NO, образованный из аргинина под действием синтазы оксида азота (NOS), также участвует в киллинге микробов. NO взаимодействует с О2 и образует высокоактивный свободный радикал пероксинитрит (ONOO-). Эти свободные радикалы атакуют и повреждают липиды, белки и нуклеиновые кислоты микробов, а также макромолекулы организма-хозяина.
Активные формы кислорода и азота обладают синергическим действием, что подтверждается изучением экспериментальных животных, когда нокаутная мышь (мышь с «выключенным» геном) с отсутствием либо оксидазы фагоцита, либо индуцибельной синтазы оксида азота (iNOS) имела среднюю предрасположенность к инфекциям, а мышь с отсутствием обоих быстро подвергалась диссеминированным инфекционным поражениям в норме безопасными условно-патогенными бактериями. Роль АФК и NO в качестве медиаторов воспаления описана далее в отдельной статье на сайте.
Киллинг микробов может осуществляться с помощью других веществ лейкоцитарных лизосом. Лизосомы нейтрофилов содержат много ферментов, которые участвуют в киллинге микробов, например эластазу. Другие бактерицидные компоненты лизосом: дефенсины (катионовые, богатые аргинином, токсичные для микробов гранулы белка); кателицидины (антимикробные белки нейтрофилов и других клеток); лизоцим (гидролизующий связь мурамовой кислоты и N-ацетилгликозамина, имеющихся в гликопептидной оболочке всех бактерий); лактоферрин (железосвязывающий белок специфических лизосомных гранул); главный основной белок (эозинофильный катионный белок, имеющий ограниченную бактерицидную активность, но цитотоксические для многих паразитов); бактерицидный и повышающий проницаемость белок (связывает бактериальный эндотоксин и важен для защиты организма от некоторых грамотрицательных бактерий).
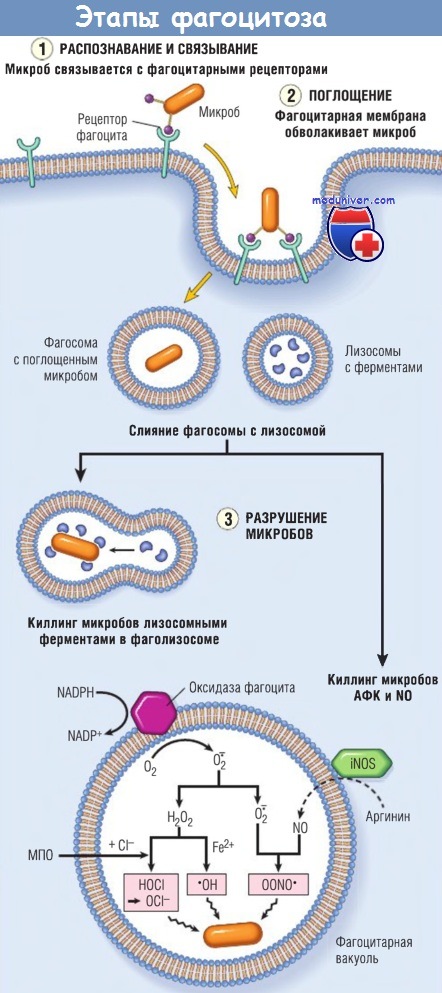
Фагоцитоз частицы (например, бактерии) заключается в связывании ее с рецепторами на фагоцитарной мембране, поглощении и слиянии с лизосомами фагоцитарных вакуолей.
Затем происходит разрушение поглощенных частиц внутри фаголизосомы лизосомными ферментами и активными формами кислорода (АФК) и активными формами азота.
Микробицидные продукты, образованные из O2 — гипохлорит (OCl) и гидроксильный ион (ОН), из оксида азота (NО) — пероксинитрит (OONO).
Во время фагоцитоза содержание гранул может высвобождаться во внеклеточную ткань (не показано).
Н2O2 — пероксид водорода; iNOS — индуцибельная синтаза оксида азота; NADP — никотинамидадениндинуклеотидфосфат;
NADPH — восстановленный никотинамидадениндинуклеотидфосфат; МПО — миелопероксидаза.
- Рекомендуем ознакомиться со следующей статьей "Механизмы повреждения лейкоцитами здоровых клеток"
Оглавление темы "Патофизиология воспаления":- Механизмы удаления микробов и мертвых клеток из очага воспаления
- Механизмы повреждения лейкоцитами здоровых клеток
- Виды нарушений функции лейкоцитов и их причины
- Механизмы завершения воспаления (терминальная фаза воспаления)
- Медиаторы воспаления и их источники, эффекты
- Гистамин и серотонин как клеточные медиаторы воспаления
- Образование метаболитов арахидоновой кислоты (простагландинов, лейкотриенов и липоксинов)
- Образование и функции фактора активации тромбоцитов (PAF)
- Образование и функции активных форм кислорода (АФК)
- Образование и функции оксида азота (NO)

