Сидеробластные анемии у детей. Синдром Пирсона
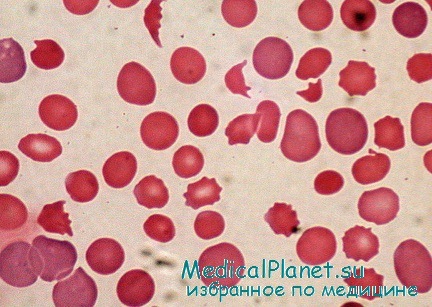
Сидеробластные анемии являются результатом приобретенных и наследственных нарушений синтеза гема. Анемии характеризуются наличием гипохромных микроцитарных эритроцитов, смешанных с нормальными эритроцитами, что дает общую картину диморфной популяции эритроцитов; при подсчете эритроцитов обнаруживается очень высокий разброс диаметров. Концентрация сывороточного железа несколько повышена, насыщение железом трансферрина увеличено.
Во всех случаях сидеробластной анемии независимо от ее причины ухудшенный синтез гема приводит к задержке железа в митохондриях. Морфологически это проявляется появлением в костном мозге ядерных эритроцитов с гранулами железа (агрегаты железа в митохондриях), расположенных около ядра. Эти необычные клетки, называемые кольцевыми сидеробластами, обнаруживаются только в патологических состояниях и отличаются от сидеробластов в костном мозге здоровых людей (предшественники эритроцитов, содержащие гранулы ферритина, рассеянные в цитоплазме). Сидеробластные анемии чаще наблюдаются у взрослых, и эти приобретенные нарушения могут быть идиопатическими или вторичными, вызванными приемом лекарств, злоупотреблением спиртными напитками, либо могут развиться в результате миелодиспластических нарушений. Некоторые сидеробластные анемии наблюдаются у детей.
Врожденная сидеробластная анемия. Этот редкий вид сидеробластной анемии обычно наследуется сцепленно с Х-хромосомой и обычно поражает мужчин, хотя выраженная инактивация асимметрии приводит и к заболеванию женщин. Возможны также случаи передачи заболевания аутосомно-доминантным путем и спорадические случаи заболевания. Наследственная сидеробластная анемия является результатом аномалий эритроцитарного изофермента для синтетазы 5-аминолевулиновой кислоты (ферментная реакция, ограничивающая скорость синтеза гема).
Важным кофактором для синтетазы 5-аминолевулиновой кислоты является пиридоксальфосфат. Ген, контролирующий эритроцитарную синтетазу 5-аминолевулиновой кислоты ALAS2, находится на Х-хромосоме. Выявлено более 20 различных миссенс-мутаций этого гена, некоторые из них происходят около точки связывания с пиридоксальфосфатом.
Тяжелые анемии распознаются в младенчестве или раннем детстве, в то время как более легкие случаи могут протекать незаметно до зрелого возраста. Клиническими проявлениями являются бледность, желтушность, умеренная спленомегалия и/или гепатомегалия. Тяжесть анемии варьирует в широких пределах, поэтому одни пациенты не нуждаются в лечении, а другим требуются регулярные переливания эритроцитов. У некоторых пациентов с наследственной сидеробластной анемией развивается гематологическая реакция на фармакологические дозы пиридоксина. Основным осложнением данного нарушения является перегрузка железом, которая проявляется повышенным уровнем сывороточного ферритина, сывороточного железа и повышенным насыщением трансферрина.
В некоторых случаях при незначительной анемии или при ее отсутствии все же могут иметь место клинические проявления перегрузки железом (например, сахарный диабет, нарушение функции печени). Для лечения детей, зависимых от переливания эритроцитов, используется пересадка стволовых клеток.
Уникальным вариантом врожденной сидеробластной анемии является синдром Пирсона, характеризующийся ранним появлением зависимой от трансфузий анемии, а также нейтропенией и тром-боцитопенией. Кроме обычных аномалий костного мозга, свойственных сидеробластной анемии, у таких детей обнаруживается вакуолизация эритроцитов и предшественников миелоидных клеток. В отличие от других сидеробластных анемий, которые являются микроцитарными, данная анемия макроцитарная, из-за чего ее иногда принимают за анемию Даймонда—Блекфена.
Известны отдельные случаи гипохромной микроцитарной анемии в сочетании с другими аномалиями обмена железа; некоторые пациенты имеют дефекты мобилизации и утилизации железа. Врожденное отсутствие железосвязывающего белка (атрансферринемия) является очень редким нарушением, связанным с тяжелой гипохромной анемией, несмотря на перегрузку железом, и требует трансфузии апо-трансферрина и лечения хелатами, хотя последнего можно избежать, если рано начать трансфузии трансферрина. Железо поглощается нормально и осаждается не в костном мозге, а преимущественно во внутренних органах.
У некоторых пациентов существует рефрактерная гипохромная анемия, ассоциированная с лимфатическими опухолями или лимфоидной гиперплазией. Коррекция анемии у таких пациентов достигается после удаления аномальной лимфатической ткани.
- Вернуться в раздел "патофизиология"
Оглавление темы "Анемии у детей":- Физиологическая анемия у новорожденных детей. Диагностика
- Недостаток фолиевой кислоты у детей. Причины и лечение
- Недостаток витамина В12 - кобаламина у детей. Причины
- Диагностика и лечение дефицита витамина В12 у детей
- Оротацидурия у детей. Тиамин-чувствительная мегалобластная анемия
- Железодефицитная анемия у детей. Причины
- Клиника и диагностика железодефицитной анемии у детей. Анализы
- Дифференциация железодефицитной анемии у детей
- Лечение железодефицитной анемии у детей. Препараты железа
- Сидеробластные анемии у детей. Синдром Пирсона

