Причины и механизмы развития системной красной волчанки (СКВ)
Причина системной красной волчанки (СКВ) остается неизвестной, однако присутствие у этих пациентов, по-видимому, бесчисленного количества аутоантител к собственным компонентам тканей показывает, что при системной красной волчанке (СКВ) фундаментальным дефектом является недостаточность механизмов, поддерживающих аутотолерантность.
Как при большинстве аутоиммунных болезней, в патогенезе системной красной волчанки (СКВ) играют роль и генетические, и иммунологические факторы, и факторы внешней среды.
а) Генетические факторы. СКВ является генетически детерминированным заболеванием, в развитие которого вносят вклад не только МНС-гены, но и многочисленные не-МНС-гены. Ряд данных подтверждает генетическую предрасположенность СКВ:
- у членов семьи больного СКВ существует повышенный риск развития СКВ. До 20% ближайших родственников пациентов имеют аутоантитела и другие иммунорегуляторные отклонения;
- существует более высокая степень конкордантности (> 20%) у монозиготных близнецов по сравнению с дизиготными (1-3%);
- исследование ассоциаций HLA подтверждает концепцию, что МНС-гены регулируют продукцию определенных аутоантител. Специфические аллели HLA -DQ-локуса связаны с продукцией антител к двухцепочечной ДНК, анти-Sm и антифосфолипидных антител, хотя относительный риск невелик;
- некоторые больные СКВ (6%) наследуют недостаточность ранних компонентов системы комплемента — С2, С4 или C1q. Отсутствие системы комплемента может нарушать выведение циркулирующих иммунных комплексов системой мононуклеарных фагоцитов, тем самым благоприятствуя их отложению в тканях. Нокаутные мыши с дефицитом С4 или некоторых рецепторов системы комплемента также склонны к развитию волчаночноподобного аутоиммунитета.
Это обусловлено различными механизмами, включая недостаточность клиренса иммунных комплексов и утрату В-клеточной аутотолерантности. Предполагается также, что дефицит C1q приводит к нарушению фагоцитарного клиренса апоптозных клеток. В нормальных условиях многие клетки подвергаются апоптозу, но, если они не выводятся, их ядерные компоненты могут вызвать иммунный ответ;
- в экспериментальных моделях СКВ идентифицировано несколько не-МНС-локусов чувствительности. Наиболее изученную модель представляют мыши линии (NZB х NZW)F1. Предполагается, что у различных вариантов этой линии с заболеванием ассоциированы до 20 локусов.
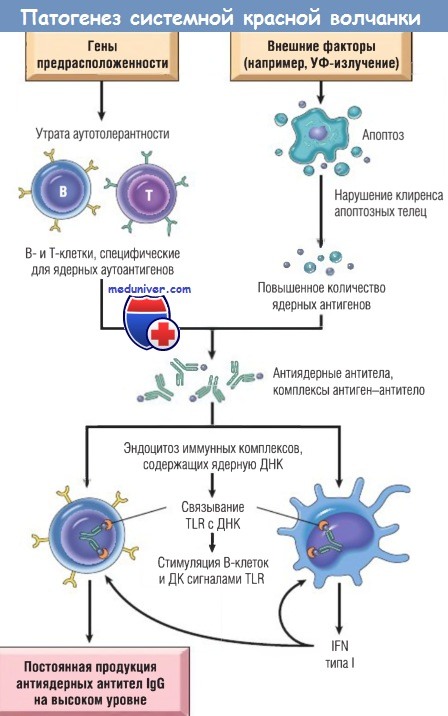
Соответственно этой гипотетической модели гены предрасположенности способны вызвать утрату аутотолерантности, а действие внешних факторов приводит к персистенции ядерных антигенов.
Развивается иммунный ответ на ядерные аутоантигены, который усиливается под воздействием нуклеиновых кислот на дендритные клетки (ДК) и В-лимфоциты, а также продуцируемого IFN типа I.
IFN — интерферон; Ig — иммуноглобулин; TLR — Toll-подобные рецепторы; ДНК — дезоксирибонуклеиновая кислота; УФ — ультрафиолетовый.
б) Иммунологические факторы. В проведенных недавно исследованиях на животных и с участием пациентов обнаружены различные иммунологические отклонения, которые могут привести к персистенции и неконтролируемой активации аутореактивных лимфоцитов:
- нарушения элиминации аутореактивных В-клеток в костном мозге или дефекты механизмов периферической толерантности могут обусловливать утрату аутотолерантности В-клеток;
- в экспериментальных моделях СКВ и у некоторых пациентов получены данные о том, что хелперные Т-клетки CD4+, специфические для нуклеосомных антигенов, также избегают толерантности и способствуют продукции высокоаффинных патогенных аутоантител;
- ядерные ДНК и РНК, содержащиеся в иммунных комплексах, способны активировать В-лимфоциты, взаимодействуя с TLR, в норме распознающими микробные продукты, включая нуклеиновые кислоты. Таким образом, В-клетки, специфические для ядерных антигенов, могут получить сигналы 2 от TLR и активироваться, что приводит к повышенной продукции антиядерных аутоантител;
- проведенный недавно анализ лимфоцитов периферической крови пациентов выявил выраженные молекулярные особенности, свидетельствующие об эффектах IFN типа I. Эти антивирусные цитокины в нормальных условиях образуются во время врожденного иммунного ответа на вирусы. Возможно, нуклеиновые кислоты взаимодействуют с TLR на дендритных клетках и стимулируют продукцию IFN. Другими словами, собственные нуклеиновые кислоты организма имитируют их микробные аналоги.
Роль IFN при СКВ неясна; он способен активировать дендритные клетки и В-клетки и усиливать ответ Тh1-клеток, все это может способствовать продукции патогенных аутоантител;
- в число других цитокинов, которые могут играть роль в нерегулируемой активации В-клеток, входят члены семейства TNF BAFF, повышающие выживаемость В-клеток. Есть сообщения, что у некоторых пациентов и в животных моделях продукция BAFF повышена, таким образом, появляется возможность блокировать цитокины или их рецепторы с целью лечения аутоиммунных болезней.
в) Факторы внешней среды. Существует множество указаний на то, что внешняя среда также вносит свой вклад в патогенез СКВ. Воздействие ультрафиолетового (УФ) облучения может утяжелить заболевание у многих пациентов. УФ-облучение способно индуцировать апоптоз клеток и изменить ДНК, что она станет иммуногенной (возможно, вследствие повышенного распознавания посредством TLR).
Кроме того, УФ-лучи могут модулировать иммунный ответ, например стимулируя продукцию кератиноцитами IL-1 — цитокина, способствующего воспалению. Половые гормоны, по-видимому, также оказывают существенное влияние на развитие и проявления СКВ. В течение репродуктивного возраста (от 17 до 55 лет) частота СКВ среди женщин в 10 раз выше, чем среди мужчин. Отмечено обострение заболевания во время нормальных месячных и беременности. Такие лекарственные средства, как гидралазин, прокаинамид и D-пеницилламин, способны индуцировать у человека СКВ-подобный ответ.
г) Модель патогенеза СКВ. Иммунологические отклонения при СКВ — как задокументированные, так и постулированные — столь же вариабельны и сложны, как и клинические проявления. Тем не менее можно попытаться объединить новые результаты и построить гипотетическую модель патогенеза СКВ. УФ-облучение и другие воздействия среды вызывают апоптоз клеток. Нарушение клиренса ядер этих клеток приводит к накоплению большого количества ядерных антигенов.
Аномалии В- и Т-лимфоцитов ответственны за нарушения толерантности, вследствие чего аутореактивные лимфоциты выживают и остаются функционирующими. Ядерные аутоантигены организма стимулируют эти лимфоциты, и образуются антитела к данным антигенам. Комплексы антиген-антитело связываются с Fc-peцепторами В-лимфоцитов и дендритных клеток и интернализируются. Компоненты нуклеиновых кислот взаимодействуют с TLR и стимулируют продукцию аутоантител В-клетками, а также образование IFN и других цитокинов дендритными клетками, что еще больше усиливает иммунный ответ и апоптоз.
Конечный результат — высвобождение антигена и иммунная активация, завершающаяся продукцией высокоаффинных аутоантител.
д) Механизмы повреждения тканей. Независимо от механизма образования аутоантител ясно, что именно они служат медиаторами повреждения тканей. Большинство повреждений внутренних органов вызывают иммунные комплексы (гиперчувствительность типа III). Комплексы ДНК-анти-ДНК можно обнаружить в почечных клубочках и мелких кровеносных сосудах.
Низкий уровень компонентов системы комплемента в сыворотке (вторичное снижение, обусловленное потреблением белков системы комплемента) и зернистые отложения компонентов системы комплемента и Ig в клубочках подтверждают иммунокомплексную природу заболевания. Аутоантитела, специфические для эритроцитов, лейкоцитов и тромбоцитов, опсонизируют эти клетки и способствуют их фагоцитозу и лизису. Отсутствуют данные о том, что ANA, участвующие в образовании иммунных комплексов, способны проникать в интактные клетки. Однако если ядра клеток повреждены, то ANA могут с ними связываться.
В тканях ядра поврежденных клеток реагируют с ANA, утрачивают структуру хроматина и становятся гомогенными, образуя так называемые КВ-тельца, или гематоксилиновые тельца. С этим феноменом связано появление KB-клеток, которые легко обнаружить, встряхивая кровь in vitro. KB-клетка представляет собой любой фагоцитирующий лейкоцит (нейтрофил или макрофаг), поглотивший денатурированное ядро поврежденной клетки. В прошлом обнаружение КВ-клеток in vitro служило диагностическим тестом СКВ. Однако с появлением новых методов определения ANA этот тест сохранил в основном лишь исторический интерес. KB-клетки обнаруживают у пациентов в перикардиальном или плевральном выпоте.
Таким образом, СКВ представляет собой комплексное расстройство многофакторной природы, возникающее в результате взаимодействия генетических, иммунологических факторов и факторов внешней среды, что активирует хелперные Т-клетки и В-клетки и приводит к образованию патогенных аутоантител различных типов.
Видео этиология, патогенез системной красной волчанки (СКВ)
- Рекомендуем ознакомиться со следующей статьей "Морфология системной красной волчанки (СКВ)"
Оглавление темы "Аутоиммунные болезни":- Механизмы клеточно-опосредованной гиперчувствительности (IV типа)
- Виды аутоиммунных болезней
- Иммунологическая толерантность и ее механизмы
- Патогенез (механизм) аутоиммунитета
- Эпидемиология и критерии системной красной волчанки (СКВ)
- Причины и механизмы развития системной красной волчанки (СКВ)
- Морфология системной красной волчанки (СКВ)
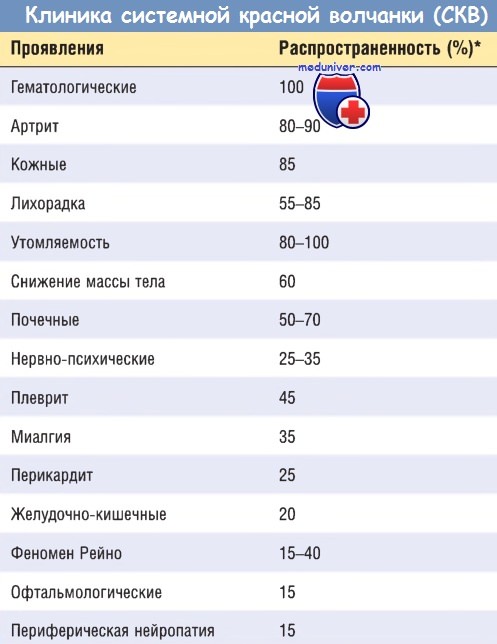
- Клиника системной красной волчанки (СКВ)
- Причины и механизмы лекарственной красной волчанки
- Причины и механизмы развития синдрома Шегрена

