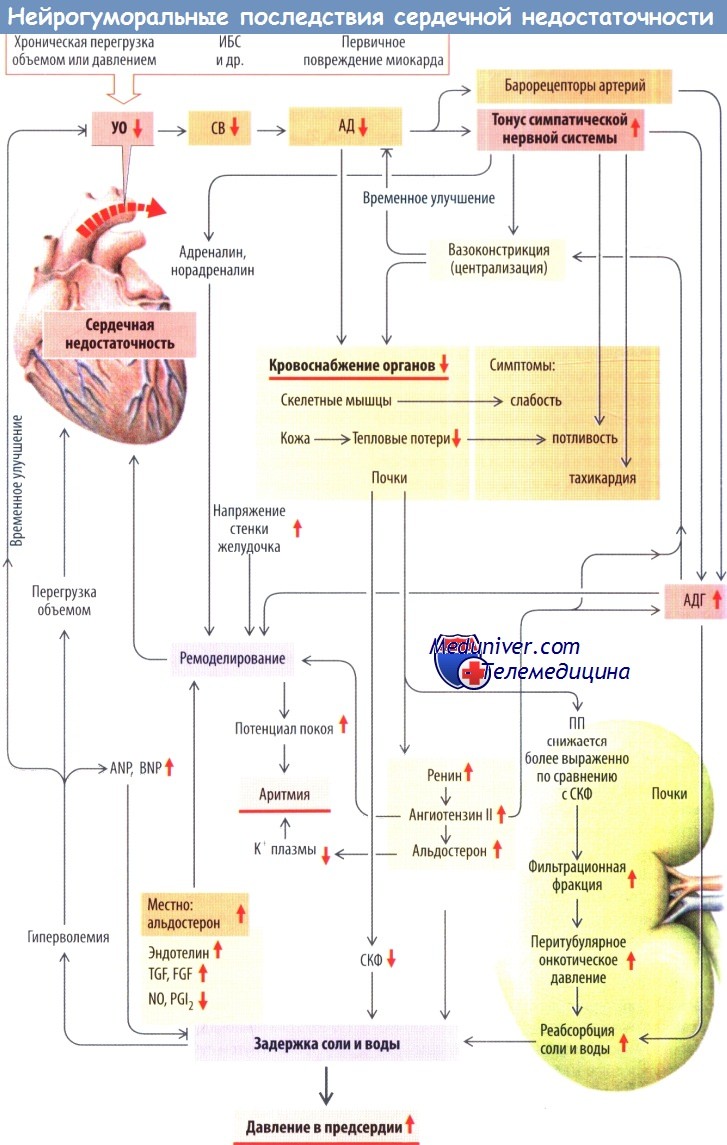
Схема развития сердечной недостаточности
Сердечная недостаточность — это состояние, сопровождающееся снижением сократительной функции миокарда и затрагивающее главным образом левый желудочек. Основными ее причинами служат ИБС и АГ, составляющие 75 % всех случаев сердечной недостаточности. Однако почти все формы заболеваний сердца (клапанные пороки, кардиомиопатии) и некоторые несердечные патологические состояния также могут осложняться сердечной недостаточностью.
В частности, правожелудочковая недостаточность сердца бывает результатом легочной гипертензии, пороков и шунтов, локализующихся в правых отделах сердца.
Правый желудочек также может поражаться вторично в результате снижения функции левого желудочка (митральный стеноз, левожелудочковая недостаточность). Обычно на начальных стадиях сердечная недостаточность проявляется при выраженной физической нагрузке (при этом выявляют снижение максимального потребления O2 и СВ, другие симптомы отсутствуют; I стадия по классификации NYHA [Нью-йоркская кардиологическая ассоциация]).
Однако затем отмечается прогрессивное нарастание симптомов, которые сначала появляются при обычной физической нагрузке, а позднее даже в покое (стадии II—IV по NYHA).
Выделяют сердечную недостаточность с систолической и диастолической дисфункциями. При систолической дисфункции снижается сократительная способность желудочков, желудочки не полностью опорожняются во время сокращения, КДО возрастает, а УО уменьшается. В результате снижается фракция выброса (ФВ = УО/КДО; с. 192). Наиболее частой причиной систолической дисфункции служит инфаркт миокарда. В зависимости от его локализации поражается либо левый, либо правый желудочек, в то же время левожелудочковая недостаточность часто приводит ко вторичной правожелудочковой недостаточности.
Систолическая дисфункция сопровождается нарушениями обеспечения и утилизации энергии, возбуждения сердца, работы сократительного аппарата и регуляции концентрации ионов Са2+ в цитоплазме.
Заполнение желудочка определяется степенью и скоростью расслабления желудочков. Расслабление желудочков сопровождается потреблением АТФ. Динамика расслабления зависит также от снижения концентрации ионов Са2+ в цитоплазме, т. е. от скорости перемещения ионов Са2+ в саркоплазматический ретикулум (SERCA2A) и интерстиций (сарколеммальные Са2+-АТФазы). Кроме того, пассивная жесткость миокарда изменяется в результате фосфорилирования титина («натягивающей пружины»), происходящего при участии протеинкиназы С.
Расслабление ускоряется благодаря фосфорилированию фосфоламбана, происходящего в процессе стимуляции бета-адренорецепторов миокарда (положительный лузитропный эффект).
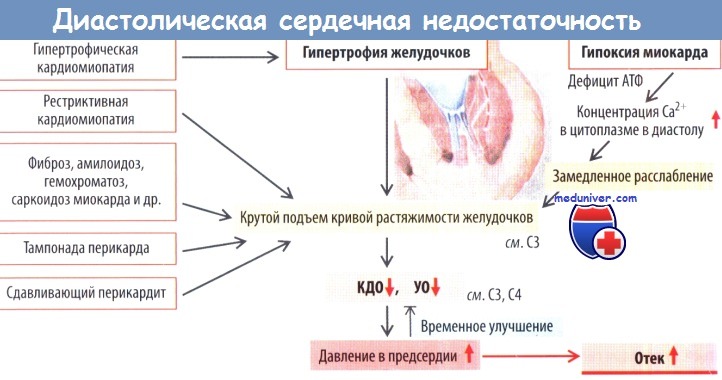
При диастолической дисфункции снижается заполнение желудочков, что обычно возникает вследствие недостаточного расслабления, например, в результате замедления работы Са2+-насоса, что, в свою очередь, обусловлено дефицитом АТФ во время ишемии. К другим причинам диастолической дисфункции относятся избыточная жесткость стенки желудочка и нарушение растяжимости желудочка вследствие:
- гипертрофии миокарда при гипертрофической кардиомиопатии или а) легочной либо системной гипертензии и б) высоком внутрижелудочковом давлении при стенозе клапана легочной артерии или аортального клапана (затрудненный выброс);
- отложения в интерстиции миокарда коллагена из-за возрастных изменений, амилоида при амилоидозе или железа при гемохроматозе;
- рестриктивной кардиомиопатии;
- сдавливающего перикардита или тампонады перикарда.
Диастолическая дисфункция приводит к снижению как УО, так и КДО, в то время как фракция выброса остается неизменной и даже может возрастать с целью сохранить СВ, несмотря на недостаточное заполнение желудочка. Тем не менее значимое уменьшение заполнения левого желудочка может привести к снижению СВ с соответствующими клиническими последствиями (см. ниже).Увеличение давления в соответствующем предсердии сопровождается улучшением заполнения желудочка, но в то же время может привести к отеку в лежащем выше капиллярном русле.
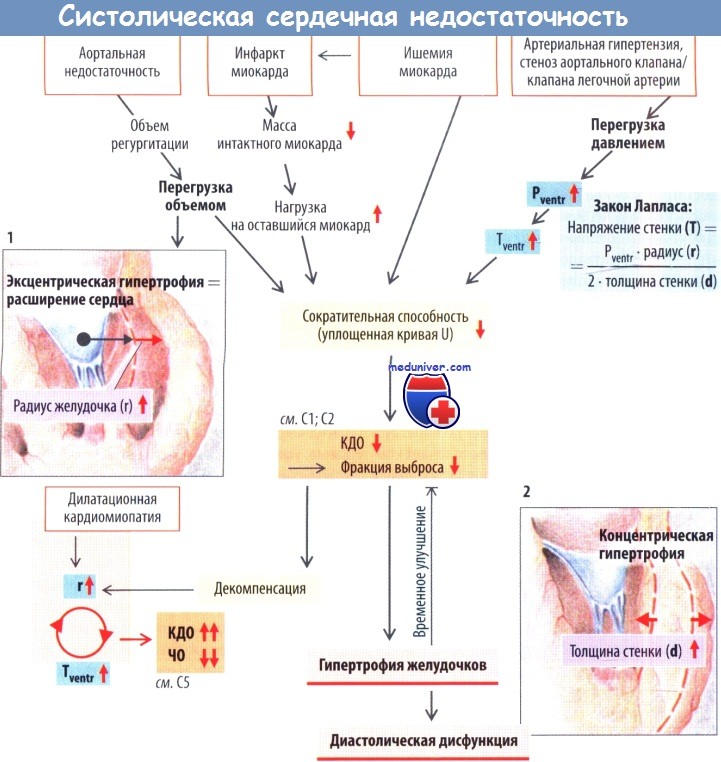
Сердечная недостаточность, обусловленная прямым повреждением миокарда (миокардиальная форма сердечной недостаточности). При ИБС (ишемия) и после инфаркта миокарда возрастает нагрузка на мышцу сердца, незатронутую инфарктом, что приводит к систолической дисфункции (см. выше) со снижением сократительной способности и УО. Гипертрофия оставшегося миокарда, формирование неэластичного рубца, а также снижение интенсивности работы Са2+-насоса в ишемизированном миокарде приводят к дальнейшему прогрессированию диастолической дисфункции.
Наконец, в систолу податливый рубец в зоне инфаркта может выпячиваться наружу (дискинезия), вызывая дополнительную перегрузку объемом (объем регургитации). К сердечной недостаточности могут также приводить кардиомиопатии, при этом будут превалировать гипертрофическая и рестриктивная формы диастолической дисфункции.
Сердечная недостаточность, обусловленная перегрузкой миокарда объемом (перегрузочная объемом форма сердечной недостаточности). Недостаточность клапана аорты, а также недостаточность клапана легочной артерии характеризуются добавлением дополнительного объема регургитации к эффективному УО. В результате увеличивается КДО, а следовательно, и радиус (r) левого желудочка, что, согласно закону Лапласа, повышает напряжение стенки (Т), т. е. увеличивается усилие, которое должен сгенерировать миокард с данной площадью поперечного сечения для достижения эффективного УО.
Поскольку такой способ оказывается неадекватным, уменьшается УО и СВ (= ЧСС - УО), что ведет к падению АД. На хроническую перегрузку объемом расширенный желудочек отвечает компенсаторной гипертрофией, сопровождающейся утолщением его стенок (d). Однако r остается увеличенным (эксцентрическая гипертрофия); данная форма сердечной недостаточности обычно характеризуется менее благоприятным течением по сравнению с концентрической гипертрофией (см. ниже). При несвоевременном устранении причины сердечной недостаточности (например, клапанного порока) последняя относительно быстро прогрессирует ввиду возни кающего ремоделирования миокарда. Возникает порочный круг, когда стенка расширенного желудочка растягивается еще больше (дилатация с перестройкой структуры миокарда) и г быстро увеличивается.
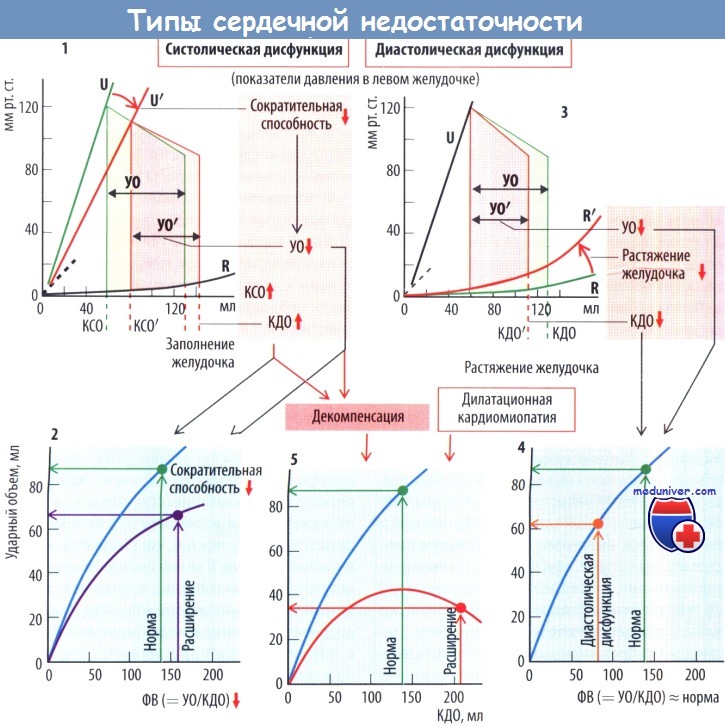
Декомпенсация характеризуется угрожающим жизни падением УО, несмотря на выраженное увеличение КДО. Сходные соображения применимы и к дилатационной кардиомиопатии.
Сердечная недостаточность, обусловленная перегрузкой давлением (перегрузочная давлением форма сердечной недостаточности). Напряжение стенки (Т) левого желудочка возрастает при системной или легочной гипертензии, а также при аортальном стенозе или стенозе клапана легочной артерии, поскольку в этих ситуациях давление в соответствующем желудочке (Pventr) должно быть высоким (закон Лапласа). Возникает систолическая дисфункция желудочка с компенсаторной его гипертрофией. Гипертрофия является концентрической, поскольку в этом случае объем желудочка не увеличивается, а в некоторых случаях может даже сокращаться. Благодаря гипертрофии уменьшается выраженность систолической дисфункции, но одновременно возникает диастолическая дисфункция. КДО и УО снижаются.
На фоне высокой нагрузки давлением ремоделирование миокарда и неадекватное капиллярное кровообращение (относительная коронарная ишемия) обусловливают критическую массу миокарда, равную 500 г, при которой происходят структурные изменения миокарда, приводящие к декомпенсации.
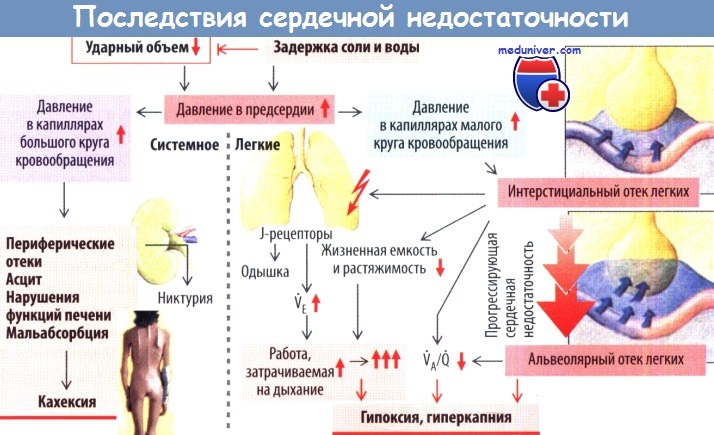
Основные симптомы левожелудочковой недостаточности — утомляемость, обусловленная снижением СВ, и одышка, связанная с увеличением давлении в легочных венах. Если давление в легочных капиллярах превысит онкотическое давление плазмы, то жидкость начнет пропотевать через стенки капилляров и скапливаться в интерстициальном пространстве и в просвете альвеол, что приведет к интерстициальному и альвеолярному отеку легких. Отек способствует усилению одышки и снижению растяжимости ткани легкого(она становится более ригидной), увеличению работы, затрачиваемой на дыхание, уменьшению вентиляционно-перфузионного отношения, а также снижению РaO2.
При сохраняющейся тяжелой левожелудочковой недостаточности появляется выпот в плевральных полостях, что ведет к учащению дыхания, в конечном итоге может возникнуть респираторный алкалоз.
При правожелудочковой недостаточности возрастает системное венозное давление, что приводит к появлению периферических отеков (особенно голеней и стоп, появляющихся в течение дня; ночью жидкость выводится из организма в результате никтурии) и к полнокровию органов брюшной полости (особенно печени и ЖКТ) со скоплением жидкости в брюшной полости (асцит). Нарушается функция печени (в крови увеличивается концентрация билирубина, активности печеночных ферментов и протромбинового времени). В дальнейшем венозный застой может вызвать мальабсорбцию, экссудативную энтеропатию с потерей белка и кахексию.
Нейрогуморальные последствия сердечной недостаточности. Помимо механического влияния на сердце сердечная недостаточность включает ряд компенсаторных механизмов, прежде всего направленных на восстановление СВ и АД. В реализации этих компенсатор ных механизмов участвуют барорецепторы левого желудочка, каротидного синуса и дуги аорты, актива ция которых способствует увеличению высвобожде ния АДГ, астимуляция тонуса симпатической нерв нот системы — усиленному высвобождению норадрена лина. Эти механизмы приводят к:
- задержке воды под влиянием АДГ (увеличение наполнения сердца) и спазму периферических сосудов;
- норадренергическому увеличению ЧСС (тахикардия) и восстановлению сократительной способности миокарда (положительное инотропное действие), а также СВ;
- более быстрому расслаблению миокарда (положительное лузитропное действие);
- альфа-1-адренергической вазоконстрикции, а следовательно, к снижению кровоснабжения скелетных мышц (слабость), кожи (бледность) и почек, цель которой заключается в перераспределении СВ в сторону преимущественного кровоснабжения сердца и головного мозга (феномен централизации кровообращения);
- активации ренин-ангиотензин-альдостероновой системы (за счет усиления активности симпатических нервов и ослабления почечного кровотока), приводящей к задержке ионов Na+ с последующим увеличением объема внеклеточной жидкости и наполнения сердца в диастолу(преднагрузки) как попытке увеличения СВ.
Указанные компенсаторные механизмы препятствуют появлению клинических симптомов хронической сердечной недостаточности в течение ряда лет (I функциональный класс по NYHA), но в долгосрочной перспективе играют отрицательную роль. За счет спазма сосудов, обусловленного симпатическими влияниями, а также действием ангиотензина II и АДГ, увеличивается пре- и постнагрузка на желудочки, что ведет к апоптозу кардиомиоцитов с последующим фиброзом (см. ниже). Более того, задержка воды и ионов Na+ почками обусловливаетхрониче-скую перегрузку желудочков объемом.
Высокое давление в предсердиях приводит к высвобождению предсердного натрийуретического пептида (ANP), а высокое напряжение стенки желудочков запускает высвобождение мозгового натрийуретического пептида (BNP). Однако натрийуретические пептиды не в состоянии полностью предотвратить избыточное накопление ионов Na+. Плазменные концентрации BNP или NT-BNP, пептида, образующегося параллельно BNP в результате расщепления pro-BNP, —это ценные диагностические маркеры, позволяющие отслеживать характер течения сердечной недостаточности.
Ремоделирование сердца начинается на самых ранних этапах развития сердечной недостаточности (I стадия по NYHA) под влиянием механических и нейрогормональных стимулов. Это неизбежно способствует прогрессии сердечной недостаточности. Причины ремоделирования:
1) высокое напряжение стенки желудочков, что среди прочих эффектов приводит к увеличению концентрации ионов Са2+ в цитоплазме кардиомиоцитов;
2) системные сигналы роста (норадреналин, АДГ, ангиотензин II; инсулин при сахарном диабете 2-го типа);
3) местные ростовые сигналы (эндотел и н, фактор роста соединительной ткани, TGF, PDGF, FGF,уменьшение активности ингибиторов роста NO и PGI2).
4) воспалительные сигналы (TNF-a, IL-6, генерация радикалов кислорода альдостероном сердца). Кардиомиоциты увеличиваются в размере (гипертрофия), но при этом становятся рефрактерными к влиянию катехоламинов (подавление активности бета-1-адренорецепторов, увеличение антагонистической активности Gi-белков, расщепления рецепторов), и снижается активность Са2+-АТФазы.
В результате удлиняется ПД кардиомиоцитов (вследствие уменьшения интенсивности деполяри-зационных токов), а потенциал покоя становится менее отрицательным. Указанные изменения могут приводить к аритмиям (по механизмам формирования реэнтри, постпотенциалов, эктопических водителей ритма), а в некоторых случаях даже к фибрилляции желудочков (возникаету 50 % пациентов с сердечной недостаточностью, что становится причиной внезапной смерти). В целом снижается сократительная способность миокарда (в т. ч. частично вследствие исчезновения функциональной связи между диги-дропиридиновыми и рианодиновыми Са2+-каналами), уменьшается его растяжимость, меняется объем и геометрия полостей сердца. Активация фибробластов (FGF и др.) приводит к отложению коллагена в стенке желудочков и фиброзу миокарда.
Лечебные мероприятия при сердечной недостаточности направлены на устранение кардиальных влияний норадреналина (бета-адреноблокаторы), угнетение синтеза и устранение эффектов ангиотензина II (ингибиторы АПФ и антагонисты ангиотензиновых рецепторов I типа), а также эффектов альдостерона, который кроме задержки ионов Na+ (гиперволемия) и выведения К+ (риск аритмий!) приводит к образованию в сердце и сосудах свободных радикалов, чем вносит свой вклад в развитие воспалительного ответа с фиброзом и ремоделированием миокарда. Ингибиторы АПФ не блокируют высвобождение альдостерона полностью, поскольку его образование при сердечной недостаточности (частично в сердце) лишь отчасти зависит от ангиотензина II.
Таким образом, селективные антагонисты альдостерона (например, эплеренон) положительно влияют на выживаемость пациентов с сердечной недостаточностью.
Видео этиология, патогенез сердечной недостаточности систолической, диастолической, лево- и правожелудочковой
- Рекомендуем ознакомиться со следующей статьей "Схема развития перикардита и других болезней перикарда"
Оглавление темы "Патофизиология в схемах":- Схема развития инфаркта миокарда
- Схема развития сердечной недостаточности
- Схема развития перикардита и других болезней перикарда
- Схема развития шока (гемодинамического)
- Схема развития отеков
- Схема развития атеросклероза
- Схема развития метаболического синдрома
- Схема развития васкулитов и тромбоэмболии
- Схема развития варикоза вен (варикозного расширения вен)
- Схема нарушения метаболизма при дефектах ферментов

