Механизмы развития (патогенез) наследственного сфероцитоза
Наследственный сфероцитоз - наследственное заболевание обусловлено внутренними нарушениями скелета мембраны эритроцитов. Эти дефекты придают эритроцитам сфероидную форму, снижают их способность к деформации и делают восприимчивыми к секвестрации и деструкции в селезенке.
Наиболее распространен наследственный сфероцитоз в Северной Европе (1 случай на 5000 человек). В 75% случаев обнаруживается аутосомно-доминантный тип наследования. Остальные пациенты имеют более тяжелую форму заболевания, обычно обусловленную наследованием двух различных дефектов (состояние, известное как комбинированная гетерозиготность).
а) Патогенез наследственного сфероцитоза. Эластичность и стойкость нормальных эритроцитов обусловлены физико-химическими свойствами специализированного скелета мембраны, тесно прилегающего к внутренней поверхности плазматической мембраны. Его главный белковый компонент, спектрин, состоит из двух полипептидных цепей, а и b, образующих переплетенный (спиральный) гибкий гетеродимер. «Головные» области димеров спектрина связываются между собой и образуют тетрамеры, тогда как «хвосты» связываются с олигомерами актина.
Каждый олигомер актина может связывать множество тетрамеров спектрина, тем самым образуя двухмерный спектрин-актиновый скелет, соединяющийся с клеточной мембраной двумя отдельными связями: первая, создаваемая белками анкирином и полосой 4.2, связывает спектрин с трансмембранным ионным транспортером — полосой 3; вторая, включающая белок 4.1, связывает «хвост» спектрина с другим трансмембранным белком — гликофорином А.
Наследственный сфероцитоз вызывают различные мутации, приводящие к нарушениям скелета мембраны. В результате возникших изменений продолжительность жизни эритроцитов уменьшается в среднем до 10-20 сут (вместо 120 сут в норме). Патогенные мутации чаще всего затрагивают анкирин, полосу 3, спектрин или полосу 4.2, т.е. белки, участвующие в первом связующем взаимодействии. По всей видимости, этот комплекс особенно важен для стабилизации липидного бислоя. Большинство мутаций приводят к сдвигу рамки считывания или преждевременному стоп-кодону, в результате мутировавший аллель становится неспособным к продукции любого белка.
Дефект синтеза белка препятствует сборке скелета мембраны, в связи с чем снижается плотность его компонентов. Очевидно, что комбинированная гетерозиготность по двум дефектным аллелям вызывает более тяжелое нарушение скелета мембраны. Молодые эритроциты при наследственном сфероцитозе имеют нормальную форму, однако нарушение скелета мембраны уменьшает стабильность липидного бислоя, что приводит к утрате фрагментов мембраны по мере старения эритроцитов, находящихся в кровотоке. Отсутствие воздействия мембраны на цитоплазму приводит к установлению минимально возможного диаметра клеток для данного объема, т.е. эритроциты становятся сферичными (сфероциты).
Благоприятные эффекты спленэктомии доказывают важную роль селезенки в преждевременной гибели эритроцитов. Нормальные эритроциты сильно деформируются, покидая тяжи Бильрота, чтобы проникнуть в синусоиды. Сфероциты из-за своей формы и сниженной способности к деформации задерживаются в селезеночных тяжах, где служат мишенью для фагоцитов. Существующая в селезенке среда до некоторой степени усиливает тенденцию эритроцитов при наследственном сфероцитозе к потере через мембрану ионов калия и воды. Этому, вероятно, также способствуют продолжительный застой эритроцитов в селезенке (эритростаз), истощение запасов глюкозы и падение pH в эритроцитах. После спленэктомии сфероцитоз персистирует, однако анемия корригируется.
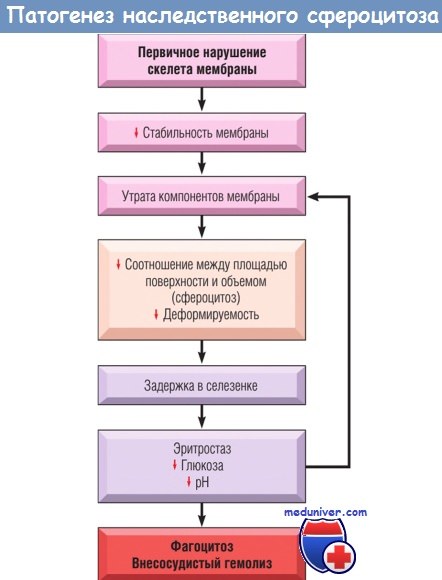
б) Морфология. Наиболее специфический морфологический признак — сфероцитоз, определяемый в мазках по наличию аномально малых гиперхромных эритроцитов, у которых отсутствует просветление в центре. Сфероциты — отличительный, но не пато-гномоничный признак наследственного сфероцитоза, т.к. сфероциты могут быть и при аутоиммунной гемолитической анемии. Другие признаки наследственного сфероцитоза являются общими для всех гемолитических анемий: ретикулоцитоз, эритроидная гиперплазия костного мозга, гемосидероз и слабая желтуха. Холелитиаз встречается у 40-50% взрослых больных. Характерно умеренное увеличение селезенки (500-1000 г); при некоторых других гемолитических анемиях селезенка увеличена в большей степени.
Спленомегалия возникает вследствие застоя в тяжах Бильрота и увеличения количества фагоцитов, необходимых для удаления сфероцитов.
в) Клинические признаки. Диагноз ставят на основе семейного анамнеза, результатов гематологического исследования и лабораторных данных. У 65% пациентов эритроциты обладают аномальной чувствительностью к осмотическому лизису при инкубации в гипотонических солевых растворах, когда происходит приток воды в сфероциты, у которых ограниченна способность к растяжению. Эритроциты при наследственном сфероцитозе имеют также повышенную среднюю концентрацию гемоглобина вследствие дегидратации, вызванной потерей калия и воды.
Характерные клинические признаки наследственного сфероцитоза — анемия, спленомегалия и желтуха. Тяжесть наследственного сфероцитоза значительно варьирует. В очень небольшом количестве случаев (главным образом при комбинированной гетерозигот-ности) заболевание обнаруживают уже при рождении и проводят обменную гемотрансфузию. У 20-30% пациентов болезнь протекает столь малозаметно, что ее можно считать практически бессимптомной. В этих случаях снижение выживаемости эритроцитов легко компенсируется повышением эритропоэза. Однако у большинства пациентов компенсаторные изменения оказываются недостаточными и развивается хроническая гемолитическая анемия от небольшой до умеренной степени тяжести.
В целом стабильное течение заболевания иногда прерывается апластическими кризами, обычно провоцируемыми парвовирусной инфекцией. Парвовирус инфицирует и убивает клетки-предшественники эритроцитов, останавливая продукцию эритроцитов, пока не разовьется эффективный иммунный ответ (обычно через 1-2 нед). Вследствие сниженной продолжительности жизни эритроцитов при наследственном сферо-цитозе прекращение эритропоэза даже на короткий срок приводит к внезапному утяжелению анемии. В этой ситуации может стать необходимой поддерживающая гемотрансфузия, пока иммунная система не справится с инфекцией.
Гемолитические кризы происходят под влиянием интеркуррентных процессов, усиливающих разрушение эритроцитов в селезенке (например, при инфекционном мононуклеозе). Клинически гемолитические кризы менее значимы, чем апластические.
Наличие желчных камней, обнаруживаемых у многих пациентов, также сопровождается симптомами. Методом лечения анемии и ее осложнений является спленэктомия, однако она сопряжена с риском развития сепсиса.
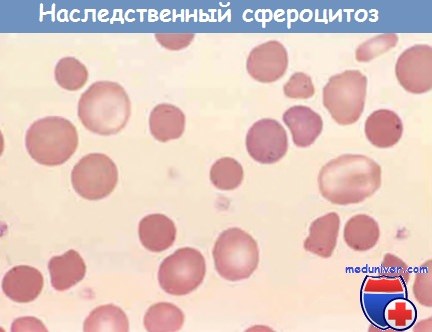
Обратите внимание на анизоцитоз и несколько более темные, чем другие клетки, сфероциты с отсутствием просветления в центре.
В эритроцитах присутствуют также тельца Хауэлла-Жолли (мелкие темные остатки ядра).
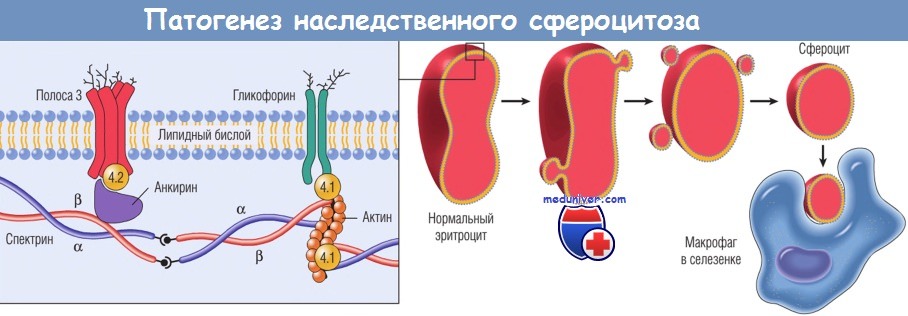
Слева — нормальное взаимодействие основных белков скелета мембраны эритроцитов.
Различные мутации спектрина (его а- и b-цепей), анкирина, полосы 4.2 и полосы 3 ослабляют взаимодействие между этими белками, вызывая утрату фрагментов мембраны эритроцитов.
Чтобы компенсировать изменения соотношения между площадью поверхности и объемом, эритроциты становятся сферичными.
Сфероциты обладают сниженной способностью к деформации по сравнению с нормальными эритроцитами, поэтому задерживаются в селезеночных тяжах, где их фагоцитируют макрофаги.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) наследственного дефицита глюкозо-6-фосфатдегидрогеназы (G6PD)"
Оглавление темы "Патогенез заболеваний крови":- Механизмы развития (патогенез) застойной спленомегалии
- Механизмы развития (патогенез) инфаркта селезенки
- Строение и функции тимуса
- Механизмы развития (патогенез) нарушений развития тимуса
- Механизмы развития (патогенез) тимомы
- Классификация анемий
- Механизмы развития (патогенез) анемии при кровопотере
- Механизмы развития (патогенез) гемолитической анемии
- Механизмы развития (патогенез) наследственного сфероцитоза
- Механизмы развития (патогенез) наследственного дефицита глюкозо-6-фосфатдегидрогеназы (G6PD)

