Ингибиторы 5-альфа-редуктазы в лечении пациентов с аденомой (доброкачественной гиперплазией) простаты
А.А.Андреев, г.Киев, Украина
Аденома (доброкачественная гиперплазия) простаты является одним из наиболее распространенных заболеваний, которое поражает мужчин старше среднего возраста. Гистологически заболевание обнаруживается более чем у 60% мужчин в возрасте старше 60 лет. Более 40% мужчин этого возраста имеют симптомы аденомы простаты, что отрицательно сказывается на качестве жизни половины из них. Ликвидация многих инфекционных заболеваний и прогресс в лечении заболеваний сердечно-сосудистой системы в развитых странах привели к значительному увеличению количества пожилых мужчин. Лица старше 65 лет составляют наиболее быстро растущую часть населения развитых стран. Подобные демографические изменения делают аденому предстательной железы (АПЖ) важной медицинской и экономической проблемой.
Если в прошлом веке аденома простаты и ее осложнения часто являлись причиной смерти, то на протяжение последних десятилетий в развитых странах отмечается значительное снижение смертности, связанной с АПЖ. В этих странах лечение направлено на улучшение качества жизни посредством освобождения от симптомов заболевания и редко касается сохранения жизни. Основываясь на изменении спектра лечения АПЖ, считается необходимым проводить экономическую оценку эффективности различных методов лечения.
Стоимость хирургического, медикаментозного или инструментального лечения складывается из 3- х компонентов:
- прямая стоимость, связанная с лабораторными, инструментальными исследованиями, лекарственным обеспечением, оплатой услуг больниц и врачей,
- непрямая стоимость, обусловленная потерей заработной платы пациентом и членами его семьи, стоимость переездов,
- "неуловимая" стоимость, связанная с болью и страданием пациента, которую создают серьезные симптомы, обусловленные АПЖ, снижающие качество жизни.
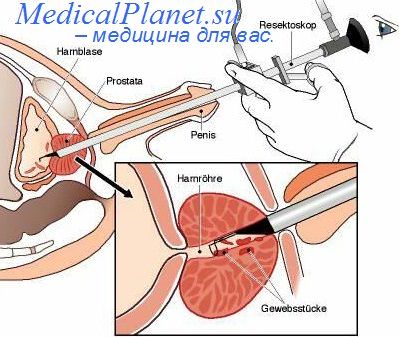
В лечении пациентов с аденомой простаты происходят значительные изменения. Количество трансуретральных резекций простаты (ТУРП) и аденомэктомий снижается по всему миру. В то время, как уменьшается количество хирургических вмешательств, медикаментозная терапия занимает все более важное место в стратегии лечения АПЖ. Применение ингибиторов 5-альфа-редуктазы (ИАР) и альфа-адреноблокаторов (ААБ) в качестве первичной медикаментозной терапии симптоматической АПЖ значительно снизило количество проводимых ТУРП и аденомэктомий.
Во время эры исключительно хирургического лечения многие мужчины, имеющие симптомы аденомы простаты, вынуждены были молча переносить страдания, отказываясь от хирургического вмешательства. Многие соглашались на операцию только в крайнем случае при развитии задержки мочи. С появлением медикаментозной терапии эти мужчины получили возможность выбора. При этом пациенты информированы, что облегчение симптоматики при медикаментозном лечении не достигает такой же степени, как после хирургического вмешательства. Они соглашаются на меньший результат в обмен на меньший риск. К медикаментозному лечению АПЖ имеются противопоказания (они же являются абсолютными показаниями к хирургическому лечению), которые включают: большое количество остаточной мочи (более 300 мл); почечная недостаточность вследствие АПЖ; повторная гематурия и рецидивирующая инфекция мочевых путей, обусловленная АПЖ; камни и большие дивертикулы мочевого пузыря; наличие рака простаты.
Для развития АПЖ необходимо сочетанное воздействие тестикулярных андрогенов и возраста. У мужчин, кастрированных до полового созревания, аденома простаты не развивается. Более того, у пациентов с различными генетическими заболеваниями, сопровождающимися подавлением образования или активности андрогенов, отмечается отсутствие или нарушение роста простаты. Клинические исследования показывают, что различные формы антиандрогенной терапии вызывают регрессию уже развившейся АПЖ. Однако, даже кастрация (медикаментозная или хирургическая) не может вернуть гиперплазированную железу к нормальному объему. Если аденома простаты уже развилась, только подавление андрогенного воздействия может быть недостаточным для возвращения клеток простаты, особенно стромальных, к норме. Основным простатическим андрогеном является дигидротестостерон (ДГТ). Несмотря на уменьшение уровня тестостерона (Т) плазмы с возрастом, уровень ДГТ в простате остается нормальным. Количество ДГТ, связанного со специфическими рецепторами ядра, является определяющим для реализации роли андрогенов в стимуляции как нормального, так и гиперпластического роста простаты. В тканях других андроген-зависимых органов, например, половом члене, количество андрогенных рецепторов (АР) снижается после полового созревания, что ограничивает возможности дальнейшего андроген-зависимого роста.
В простате такого снижения уровня АР с возрастом не наблюдается, что и позволяет обеспечить ее андроген-зависимый рост даже на фоне снижающегося с возрастом уровня Т плазмы. При развитии АПЖ количество АР может не повышаться, но поддерживается на нормальном уровне. Рецепторы факторов роста в простате также находятся под влиянием андрогенной регуляции. Основание для снижения андрогенной стимуляции в лечении АПЖ базируется на двух доказанных фактах: во-первых, для поддержания гиперпластического состояния железы необходим критический уровень простатических андрогенов; во-вторых, удаление андрогенов приводит к значительной инволюции простаты, что снижает сопротивление току мочи. Вместе с тем, удаление андрогенов у мужчин не приводит к инволюции гиперплазированной простаты до нормального состояния. Это наблюдение не противоречит андрогенной гипотезе, а лишь свидетельствует о многофакторности патогенеза АПЖ.
В мозгу, скелетных мышцах и сперматогенном эпителии Т непосредственно стимулирует андроген-зависимые процессы. В предстательной железе микросомальный фермент 5-альфа-редуктаза (5-АР) превращает Т в ДГТ, который и является основным гормоном для этой ткани. 90% общего простатического андрогена представлено в форме ДГТ, образующегося в основном из тестикулярных андрогенов. Надпочечниковые андрогены могут составлять до 10% всех простатических андрогенов, хотя значение этого источника стероидных гормонов в патогенезе АПЖ незначительно.
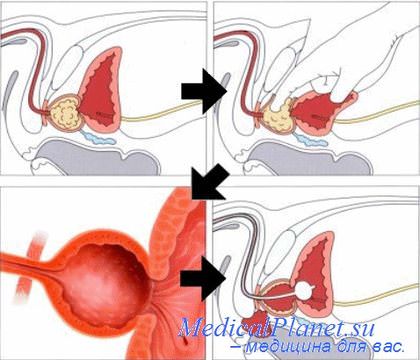
Внутри клеток Т и ДГТ связываются с белком-рецептором андрогенов. ДГТ является более "мощным" андрогеном, чем Т, вследствие более высокого сродства к АР. Более того, комплекс ДГТ-рецептор является более стабильным, чем комплекс Т-рецептор. Далее, комплекс гормон-рецептор связывается в ядре со специфическими участками ДНК, результатом чего является увеличенная транскрипция андроген-зависимых генов и, в конечном счете, стимуляция синтеза белка. И, наоборот, прекращение влияния андрогенов на андроген-зависимые ткани приводит к снижению синтеза белка и инволюции тканей.
Были открыты два стероидных фермента 5-альфа-редуктазы, каждый из которых закодирован в отдельном гене. 5-АР типа I - преимущественный фермент экстрапростатических тканей, таких как кожа и печень. Он нормально экспрессирован при синдроме дефицита 5-АР и слабо ингибируется финастеридом. 5-АР типа II является преимущественной, если не единственной, простатической 5-АР. Изменения 5-АР типа II ответственны за клинический фенотип, наблюдаемый при синдроме дефицита 5-АР. Данный тип фермента высоко чувствителен к ингибированию финастеридом. Очевидно, что 5-АР типа II является основным ферментом для нормального развития простаты, а также гиперпластического роста на протяжение жизни. Мужская сексуальная функция определяется нормальным уровнем Т в центральной нервной системе, обеспечивающим первичное поддержание либидо. Поэтому, любые дефекты в образовании или активности Т могут привести к сексуальной дисфункции. В противоположность этому, селективное ингибирование ДГТ не оказывает повреждающего влияния на либидо и эректильную функцию.
В начале 1980-х г.г. в Merck Research Laboratories были синтезированы первые представители класса 4-азастероидов, обладающие in vivo ингибирующей активностью по отношению к 5-АР. Финастерид - мощный обратимый ингибитор 5-АР типа II. Он эффективно снижает уровень ДГТ плазмы без влияния на уровень Т. Более того, финастерид снижает уровень интрапростатического ДГТ на 80-90%.
Таким образом, финастерид обеспечивает кастрационный уровень ДГТ в простатической ткани без снижения уровня Т плазмы, который необходим для поддержания либидо и обеспечения сексуальной активности. Тот факт, что финастерид не снижает сывороточный уровень ДГТ до нуля, возможно, связан с отсутствием ингибирования активности I типа 5-АР. Изучая in vitro ингибирующий эффект финастерида на 5-АР в эпителии и строме человеческой АПЖ, пришли к выводу, что ингибирующий эффект более выражен в эпителии, чем в строме. Авторы предполагают, что общее уменьшение в размерах АПЖ под влиянием терапии финастеридом происходит в основном за счет регрессии эпителия.
Однократный прием 5 мг финастерида вызывает снижение уровня циркулирующего ДГТ. Супрессия ДГТ при приеме 5 мг препарата ежедневно поддерживалась у пациентов при многомесячном наблюдении. Создается впечатление об отсутствии тахифилаксии к биохимическому эффекту финастерида. Финастерид вызывает значительное снижение уровня интрапростатического ДГТ. Концентрация сывороточного Т увеличивается на 8-10% после 3 недель лечения и остается на этом уровне. Несмотря на небольшое увеличение уровня циркулирующего Т, его показатели остаются в пределах нормы.
Клинической целью терапии финастеридом пациентов с симптоматической АПЖ является уменьшение объема гиперплазированной предстательной железы, увеличение скорости тока мочи, уменьшение выраженности симптомов, предотвращение прогрессирования заболевания.
Имея в виду возможность развития рака предстательной железы у пациентов с АПЖ, получающих финастерид, указывают на необходимость периодического пальцевого ректального исследования и мониторинга уровня простатического специфического антигена (ПСА). Рекомендуют для интерпретации уровней сывороточного ПСА у пациентов с АПЖ, применяющих финастерид на протяжение 6 мес. и более, умножить уровень ПСА на 2 и сравнивать с возраст-независимой или возраст-специфической верхней границей нормы ПСА сыворотки крови у нелеченных мужчин с АПЖ.
Дутастерид обладает способностью ингибировать оба типа ( I и II) 5-АР, в отличие от первого препарата этой группы - финастерида, который блокирует только 5-АР II типа. Это позволяет достигать подавления уровня ДГТ более чем на 90% у более 85% пациентов, принимавших дутастерид не менее 1 месяца. У финастерида за этот период времени уровень ДГТ снижается на 70%. Дутастерид обеспечивает устойчивое уменьшение симптоматики и предотвращает прогрессирование заболевания у пациентов с объемом простаты более 30 мл. Максимальная скорость потока мочи (МСПМ) и объем простаты изменяются уже в течение первого месяца терапии, что связано с ингибированием обоих типов 5-АР. Ингибиторы 5-АР приводят к значительному уменьшению как общего объема простаты, так и уменьшению переходной зоны предстательной железы у мужчин с АПЖ по сравнению с плацебо. Это приводит к уменьшению статического компонента инфравезикальной обструкции и, как следствие, к значительному облегчению симптомов нижних мочевых путей (СНМП) и увеличению МСПМ. Более того, долговременные плацебо-контролируемые исследования показали, что ингибиторы 5-АР приводят к значительному уменьшению риска развития острой задержки мочи (ОЗМ) и необходимости хирургического лечения.
Улучшение симптоматики на фоне приема ингибиторов 5-АР возникает, как правило, к 3-6 месяцу лечения. Ингибиторы 5-АР достоверно снижают риск развития ОЗМ и необходимость оперативно лечения в сравнении с плацебо; уменьшают симптоматику АПЖ; уменьшают объем простаты и увеличивают скорость потока мочи.
Данные клинических исследований показали, что ингибиторы 5-АР приводят к статистически значимому улучшению СНМП, уменьшению суммы баллов согласно шкале IPSS и к увеличению МСПМ. Ингибиторы 5-АР приводят к уменьшению объема простаты, и, как следствие, снижают риск развития ОЗМ, а также необходимость хирургического лечения. Препараты ингибиторов 5-АР хорошо переносятся пациентами. Частота встречаемости побочных эффектов низкая, они крайне редко являются значимыми и редко ведут к прекращению приема препарата.
Андреев Андрей Александрович, г.Киев
канд. мед. наук, старший научный сотрудник,
- Вернуться в оглавление раздела "Патофизиология."
Оглавление темы "Лекарственные средства в фармацеи.":1. Лекарственные средства. Лечебные средства.
2. Лекарственные формы. История лекарственных форм.
3. История отечественной фармации. История отечественных лекарственных средств.
4. Номенклатура лекарственных форм. Классификации лекарственных форм.
5. Ингаляции и инъекции. Физико-химическая классификация лекарственных средств.
6. Дозирование лекарств. Взвешивание лекарственных средств.
7. Весы рецептурные. Весы Мора.
8. Настольные весы. Проверка и уход за весами.
9. Разновесы - требования к гирям в фармации. Дозирование жидкостей в аптеке.
10. Приборы для измерения жидкости в фармацеи. Дозирование жидкостей каплями в аптеке.

