Механизм развития (патогенез) целиакии
Целиакия, также известная как нетропическая спру или глютеновая энтеропатия, является иммуноопосредованной энтеропатией, вызванной употреблением в пищу глютенсодержащих злаков (пшеницы, ржи или ячменя). Целиакия развивается только у генетически предрасположенных людей. В странах, населенных в основном представителями европеоидной расы, распространенность целиакии составляет 0,5-1,0%.
а) Патогенез. Целиакия — уникальное иммунное заболевание тонкой кишки, причина которого хорошо известна — глютен. Глютен является основным белком зерен пшеницы и сходных с ней злаков, а спирторастворимая фракция глютена, глиадин, содержит большинство компонентов, обусловливающих развитие заболевания.
Глютен расщепляется ферментами в просвете кишки и ферментами щеточной каемки до аминокислот и пептидов, включая 33-аминокислотный а-глиадиновый пептид, устойчивый к расщеплению протеазами желудка, поджелудочной железы и тонкой кишки. Опишем цепь иммунных реакций на глиадин, приводящих к развитию целиакии.
Некоторые пептиды глиадина индуцируют экспрессию эпителиальными клетками IL-15, который, в свою очередь, запускает активацию и пролиферацию внутриэпителиальных Т-лимфоцитов CD8+, вызывая в них экспрессию NKG2D (маркера NK-клеток). Такие лимфоциты становятся цитотоксическими и убивают энтероциты с поверхностным MIC-А (являющегося HLA-I-подобным белком, экспрессируемым в ответ на повреждение), т.к. NKG2D служит рецептором для MIC-A. Т-клетки CD8+ NKG2D+ не распознают глиадин, в отличие от Т-клеток CD4+.
Повреждение эпителия позволяет другим пептидам глиадина пройти через эпителиоциты в стенку кишки, где пептиды глиадина деаминируются тканевыми трансглутаминазами. Деаминированные пептиды глиадина способны взаимодействовать с рецепторами HLA-DQ2 или HLA-DQ8 на антигенпрезентирующих клетках, которые презентируют пептиды глиадина Т-клеткам CD4+. Эти Т-клетки вырабатывают цитокины, способствующие повреждению тканей и изменению слизистой оболочки.
Практически все люди едят хлеб и подвергаются воздействию глютена и глиадина, однако у большинства целиакия не развивается. Таким образом, именно от внутренних факторов организма человека зависит, разовьется ли данное заболевание или нет. Среди этих факторов решающее значение имеют белки HLA, т.к. практически все пациенты с целиакией имеют аллели HLA-DQ2 или HLA-DQ8 класса II. Система HLA ответственна не менее чем за 50% случаев целиакии.
Другими генетическими факторами являются, вероятно, полиморфизм иммунорегуляторных генов, например тех, которые кодируют синтез IL-2, IL-21, CCR3 и SH2B3, а также генов, определяющих полярность эпителия. Установлена связь целиакии с другими иммунными заболеваниями: сахарным диабетом типа I, тиреоидитом, синдромом Шегрена, а также атаксией, аутизмом, депрессией, некоторыми формами эпилепсии, IgA-нефропатией, синдромом Дауна и синдромом Тернера.
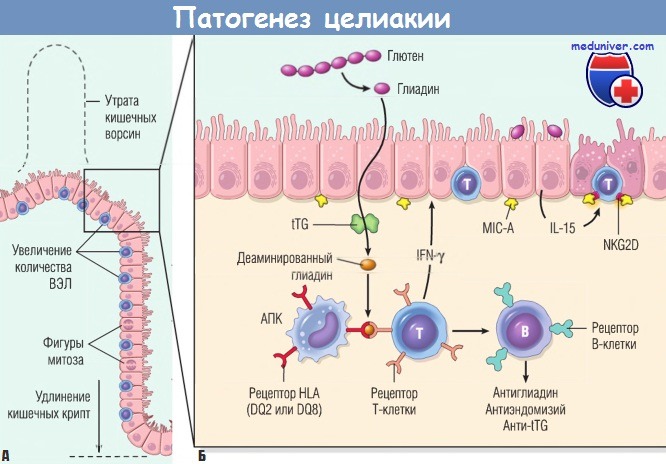
увеличение количества внутриэпителиальных лимфоцитов (ВЭЛ) и пролиферация эпителия с удлинением кишечных крипт.
(Б) Модель патогенеза целиакии. В тканевом ответе на глиадин участвуют компоненты и врожденной,
и приобретенной иммунной системы.
HLA — лейкоцитарные антигены человека; IFN — интерферон;
IL — интерлейкин; tTG — тканевая трансглютаминаза; АПК — антигенпрезентирующая клетка.
б) Морфология. Для постановки диагноза «целиакия» важно получить и исследовать биоптат из нисходящей части двенадцатиперстной кишки или проксимального отдела тощей кишки, которые больше всего подвергаются воздействию глютена. Патологические изменения: внутриэпителиальный лимфоцитоз (увеличение количества внутриэпителиальных Т-клеток CD8+), гиперплазия кишечных крипт и атрофия кишечных ворсин. Уменьшение площади слизистой оболочки и щеточной каемки приводит, вероятно, к развитию мальабсорбции.
Кроме того, увеличение скорости обновления эпителия, проявляющееся повышением митотической активности в криптах, может ограничить всасывание веществ за счет уменьшения количества дифференцированных энтероцитов, а также способствовать нарушению терминального пищеварения и трансэпителиального транспорта питательных веществ. Другие признаки целиакии — увеличение количества плазматических клеток, тучных клеток и эозинофилов, особенно в поверхностных отделах собственной пластинки слизистой оболочки кишки.
В связи с широким серологическим скринингом и ранним выявлением специфических антител в настоящее время считается, что внутриэпителиальный лимфоцитоз, особенно в кишечных ворсинах, является признаком медленно прогрессирующей целиакии. Однако внутриэпителиальный лимфоцитоз и атрофия кишечных ворсин не являются специфическими признаками целиакии и могут наблюдаться при других заболеваниях, например при вирусном энтерите. Наиболее специфичной для целиакии является комбинация гистологических и серологических признаков.
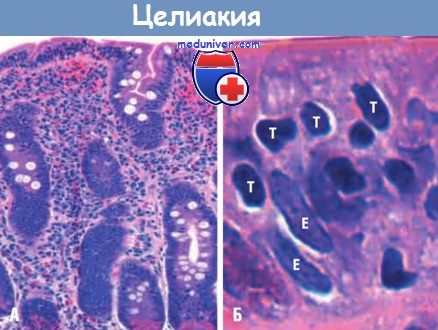
(А) При выраженной целиакии отмечается тотальная атрофия кишечных ворсин.
В собственной пластинке слизистой оболочки кишки видны плотные плазмоклеточные инфильтраты.
(Б) Инфильтрация поверхностного эпителия Т-лимфоцитами (Т), которые определяются по темноокрашенным ядрам.
Сравните с вытянутыми и более светлыми ядрами эпителиальных клеток (Е).
в) Клинические признаки. У взрослых целиакия обычно развивается в возрасте 30-60 лет. Однако в связи с ее нетипичными проявлениями диагностировать заболевание в течение длительного времени не удается. У некоторых пациентов целиакия имеет скрытое течение, и заболевание может быть выявлено только по положительным результатам серологического исследования и атрофии кишечных ворсин. Симптомная целиакия у взрослых часто сопровождается анемией, хронической диареей, метеоризмом и синдромом хронической усталости.
Несмотря на одинаковую частоту заболевания у лиц обоего пола, целиакию в 2-3 раза чаще выявляют у женщин, вероятно из-за того, что у них менструальные кровотечения увеличивают потребность в железе и витаминах и усугубляют эффект нарушенного всасывания.
В педиатрической практике целиакия может проявляться признаками мальабсорбции или другими атипичными симптомами, затрагивающими практически любой орган. Целиакия с классическими симптомами обычно манифестирует у детей в возрасте 6-24 мес после введения в их рацион продуктов, содержащих глютен, и проявляется раздражительностью, метеоризмом, анорексией, хронической диареей, плохой прибавкой или потерей массы тела, мышечным истощением.
Целиакия с неклассическими симптомами обычно наблюдается у детей старшего возраста и характеризуется болью в животе, тошнотой, рвотой, метеоризмом и запором. Внекишечные проявления — артрит или боль в суставах, эпилептические припадки, афтозный стоматит, железодефицитная анемия, замедление полового созревания и роста.
Кожный зуд, поражение кожи с образованием пузырей и герпетиформный дерматит имеют 10% пациентов, также могут развиться лимфоцитарный гастрит и лимфоцитарный колит. В настоящее время единственно возможным методом лечения целиакии является безглютеновая диета, которая, несмотря на некоторые сложности в ее соблюдении, улучшает состояние большинства пациентов. Безглютеновая диета также снижает риск отдаленных осложнений, в частности анемии, женского бесплодия, остеопороза и злокачественной опухоли.
Перед биопсией обычно проводят неинвазивное серологическое исследование. Наиболее чувствительный тест — обнаружение антител IgA к тканевым трансглутаминазам или антител IgA/IgG к деаминированному глиадину. Антиэндомизиальные антитела являются высокоспецифичными, но менее чувствительными, чем другие антитела. При отрицательном результате исследования на наличие антител IgA важно исключить дефицит IgA, который часто развивается у пациентов с целиакией.
При дефиците IgA необходимо измерить титры антител IgG к тканевым трансглутаминазам и деаминированному глиадину. Отсутствие HLA-DQ2 и HLA-DQ8 свидетельствует об отсутствии заболевания, однако наличие этих аллелей не подтверждает диагноз «целиакия».
У лиц с целиакией риск развития злокачественных новообразований выше, чем в общей популяции. Самой частой опухолью является ассоциированная с энтеропатией Т-клеточная лимфома — агрессивная лимфома из внутриэпителиальных Т-лимфоцитов. У пациентов с целиакией также относительно чаще, чем в популяции в целом, развивается аденокарцинома тонкой кишки.
В связи с этим, когда такие симптомы, как боль в животе, диарея и снижение массы тела, сохраняются, несмотря на строгую безглютеновую диету, следует предположить наличие злокачественной опухоли или резистентной спру, при которой реакция организма на безглютеновую диету также отсутствует. Наиболее распространенная причина рецидива болезни — нарушение безглютеновой диеты.
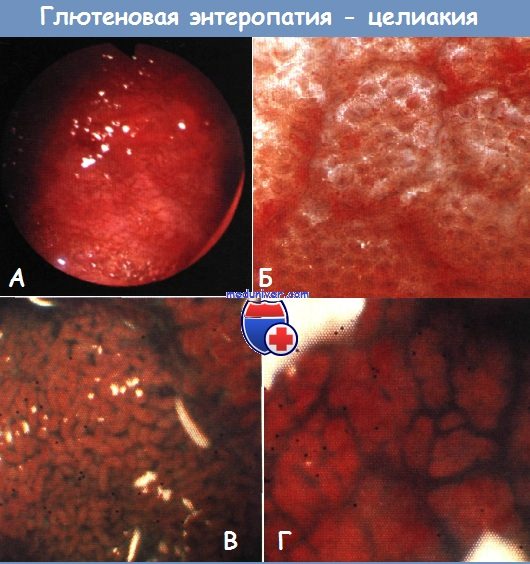
Б - Внешний вид мозаичных структур при микроскопии. Субтотальная а ворсинок
В, Г - Патология ворсинок при глютеновой болезни. Слизистая оболочка дистального отрезка двенадцатиперстной кишки обрисована в результате распыления по ее поверхности индигокармина (5 мл 0,4%). Нормальная картина (слева) замещена мозаичной (справа), видны трещины и преддверия устьев кишечных крипт.
- Рекомендуем ознакомиться со следующей статьей "Механизм развития (патогенез) тропического спру"
Оглавление темы "Патогенез болезней кишечника":- Механизм развития (патогенез) ишемической болезни кишечника
- Механизм развития (патогенез) ангиодисплазии стенки кишечника
- Механизм развития (патогенез) мальабсорбции
- Механизм развития (патогенез) диареи
- Механизм развития (патогенез) целиакии
- Механизм развития (патогенез) тропического спру
- Механизм развития (патогенез) аутоиммунной энтеропатии
- Механизм развития (патогенез) лактазной недостаточности
- Механизм развития (патогенез) абеталипопротеинемии
- Механизм развития (патогенез) холеры
- Симптомы и причины анорексии у взрослых

