Образование клеток крови (дифференцировка)
Компоненты гемопоэтической системы по традиции делят на миелоидные ткани, включающие костный мозг и происходящие из него клетки (в частности, эритроциты, тромбоциты, гранулоциты и моноциты), и лимфоидные ткани, состоящие из лимфатических узлов, селезенки и тимуса. Однако важно учитывать, что такое разделение искусственно, если иметь в виду нормальную физиологию гемопоэтических клеток и поражающие их болезни.
Хотя костный мозг содержит сравнительно немного лимфоцитов, он служит источником всех лимфоидных клеток-предшественников. В костном мозге также происходят неопластические изменения миелоидных клеток-предшественников (миелоидные лейкемии), поражающие селезенку и лимфоузлы (в меньшей степени).
Некоторые эритроцитарные расстройства, в частности иммуногемолитическая анемия, развиваются в результате образования аутоантител, что свидетельствует о первичной роли нарушений со стороны лимфоцитов. Таким образом, невозможно четкое разграничение между заболеваниями миелоидной и лимфоидной тканей.
Прежде чем излагать материал о специфических заболеваниях, кратко остановимся на происхождении кроветворных стволовых клеток (КСК), т.к. многие расстройства лейкоцитарной и эритроцитарной систем сопровождаются нарушениями развития и созревания клеток.
Предшественники клеток крови впервые появляются в желточном мешке в течение 3-й недели эмбрионального развития, однако считается, что сформировавшиеся КСК образуются на несколько недель позднее в мезодерме аортально-гонадно-мезонефральной области.
На протяжении 3-го месяца эмбриогенеза КСК мигрируют в печень, которая становится главным местом образования клеток крови вплоть до ранних сроков после рождения. На 4-м месяце эмбриогенеза КСК вновь меняют свою локализацию, на этот раз перемещаясь в костный мозг.
Ко времени рождения костный мозг всех костей плода гемопоэтически активен, а гемопоэз в печени сохраняется лишь на незначительном уровне в отдельных очагах и прекращается вскоре после рождения ребенка. До полового созревания гемопоэтически активный костный мозг обнаруживается во всех костях скелета, но вскоре после этого его локализация ограничивается лишь осевым скелетом.
Таким образом, у здорового взрослого человека только 50% костномозгового пространства гемопоэтически активно.

Форменные элементы крови (эритроциты, тромбоциты и лейкоциты) берут начало от общих клеток-предшественников — КСК, представляющих собой плюрипотентные клетки, которые находятся на вершине иерархической лестницы костномозговых клеток-предшественников. Большинство данных, подтверждающих эту схему, получено в исследованиях на мышах, однако считают, что гемопоэз у человека происходит сходным образом. КСК дают начало плюрипотентным клеткам двух типов — общим лимфоидным клеткам-предшественникам и общим миелоидным клеткам-предшественникам.
Общие лимфоидные клетки-предшественники служат источником образования предшественников Т-клеток, В-клеток и естественных клеток-киллеров (NK-клеток). Мы вернемся к вопросу о происхождении лимфоидных клеток, когда будем рассматривать опухоли, образующиеся из этих клеток.
Из общих миелоидных клеток-предшественников образуются различные типы коммитированных клеток-предшественников, ограниченных в своем развитии определенными линиями дифференцировки. Эти клетки получили наименование колониеобразующих единиц (КОЕ), т.к. при выращивании в культуре они образуют колонии зрелых клеток специфических типов. Из различных коммитированных клеток-предшественников образуются морфологически распознаваемые клетки-предшественники, такие как миелобласты, проэритробласты и мегакариобласты, которые, в свою очередь, превращаются в зрелые нейтрофилы, эритроциты и тромбоциты.
КСК обладают двумя существенными свойствами, необходимыми для поддержания гемопоэза: плюрипотентностью и способностью к самообновлению. Благодаря плюрипотентности одиночная КСК в состоянии генерировать все зрелые кроветворные стволовые клетки. Когда КСК делится, по меньшей мере одна дочерняя клетка должна самообновляться, чтобы избежать истощения популяции стволовых клеток. Считается, что деление с самообновлением происходит в специализированной костномозговой нише, где клетки стромы и секретируемые факторы обеспечивают питание КСК и каким-то образом способствуют их сохранению.
Как уже упоминалось, КСК мигрируют во время эмбрионального развития, т.е. являются подвижными. При определенных условиях, особенно в случае выраженного стресса (например, тяжелой анемии), КСК костного мозга мобилизуются и появляются в периферической крови. В этих ситуациях иногда происходит индукция, или раскрытие, дополнительных ниш для КСК в других тканях, в частности в селезенке и печени, которые затем становятся местами экстрамедуллярного гемопоэза.
Ответ костного мозга на кратковременные физиологические изменения регулируют гемопоэтические факторы роста, действуя на коммитированные клетки-предшественники. Поскольку зрелые элементы крови представляют собой терминально дифференцированные клетки с конечной продолжительностью жизни, их количество должно постоянно возобновляться. При некоторых делениях КСК одиночная дочерняя клетка начинает дифференцироваться. Переступив этот порог, новые коммитированные клетки утрачивают способность к самообновлению и вступают на уже необратимый путь, ведущий к терминальной дифференцировке и гибели.
Однако по мере дифференцировки они начинают экспрессировать рецепторы для факторов роста, стимулирующих кратковременный рост и выживаемость этих дифференцирующихся клеток. Некоторые факторы роста, например фактор стволовых клеток (называемый также лигандом с-KIT) и лиганд FLT3, действуют на очень ранние коммитированные клетки-предшественники. Другие факторы, такие как эритропоэтин, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), грану-лоцитарный колониестимулирующий фактор и тром-бопоэтин, действуют на коммитированные клетки-предшественники с более ограниченным потенциалом. Обратная связь, опосредуемая факторами роста, регулирует ответ костного мозга, сохраняя количество форменных элементов крови в определенных границах.
При многих заболеваниях продукция клеток крови изменяется. Костный мозг является основным источником всех клеток врожденной и адаптивной иммунной системы и реагирует на инфекции или воспалительные стимулы увеличением продукции гранулоцитов под влиянием специфических факторов роста и цитокинов. Другие расстройства ассоциируются с нарушениями гемопоэза, ведущими к дефициту одного или нескольких типов клеток крови. Первичные опухоли гемопоэтической ткани относят к наиболее значимым заболеваниям, нарушающим функции костного мозга. Специфические генетические болезни, инфекции, токсины и дефицит питания, а также хроническое воспаление, вызванное любыми причинами, способны уменьшать образование клеток крови костным мозгом.
Опухоли гемопоэтического происхождения часто ассоциируются с мутациями, блокирующими созревание клеток или устраняющими их зависимость от факторов роста. Конечный эффект такого нарушения состоит в нерегулируемой клональной экспансии гемопоэтических элементов, которые замещают нормальные клетки-предшественники в костном мозге и часто распространяются на другие гемопоэтические ткани. В некоторых случаях эти опухоли возникают из трансформированных КСК (с ограниченной способностью к дифференцировке в клетки многих линий), в иных ситуациях трансформированные КСК превращаются в более дифференцированные клетки-предшественники, имеющие аномальную способность к самообновлению.
Отражает ли такая ситуация просто блокаду дифференцировки или является следствием реактивации программы экспрессии генов, поддерживающих самообновление нормальных КСК, — вопрос для исследователей.
Морфология. Костный мозг является уникальной микросредой, где происходят пролиферация, дифференцировка и высвобождение клеток крови. Он заполнен сетью тонкостенных синусоидов, выстланных одним слоем эндотелиальных клеток, основу которого составляют прерывистая базальная мембрана и адвентициальные клетки. В интерстиции находятся скопления кроветворных и жировых клеток. Дифференцированные клетки крови переходят в кровоток через эндотелиальные клетки.
Организация нормального костного мозга отличается целесообразностью. Так, нормальные мегакариоциты, располагающиеся вблизи синусоидов, имеют цитоплазматические выросты, отпочковывающие образующиеся тромбоциты в кровоток. Клетки-предшественники эритроцитов часто окружены макрофагами (так называемыми клетками-нянями), передающими эритроцитам некоторое количество железа, необходимого для синтеза гемоглобина. Заболевания, нарушающие строение костного мозга, например гранулематозные болезни или метастазы злокачественных опухолей, могут вызвать аномальное высвобождение незрелых клеток-предшественников в периферический кровоток — процесс, называемый лейкоэритробластозом.
Лучший способ изучения морфологии кроветворных клеток — исследование мазков, приготовленных из аспиратов костного мозга. Наиболее зрелые костномозговые клетки-предшественники можно идентифицировать только на основе их морфологии. Незрелые клетки-предшественники (бластные формы) различных типов морфологически сходны, поэтому для их идентификации используют линейно-специфические антитела и гистохимические маркеры (см. далее описание лейкоцитарных неоплазий).
Биопсия — хороший метод определения активности костного мозга. У здоровых взрослых людей соотношение между жировыми клетками и гемопоэтическими элементами приблизительно 1:1. При гипопластических состояниях (например, при апластической анемии) доля жировых клеток существенно возрастает. И наоборот, жировые клетки почти исчезают, когда костный мозг поражен гемопоэтическими опухолями, а также при заболеваниях, характеризующихся компенсаторной гиперплазией (например, при гемолитических анемиях) и неопластической пролиферацией (в частности, при лейкемии).
Другие болезни (например, метастазирующие опухоли и гранулематозные заболевания) индуцируют местный фиброз костного мозга. Материал пораженных участков обычно не удается аспирировать, и для их исследования лучше прибегнуть к биопсии.
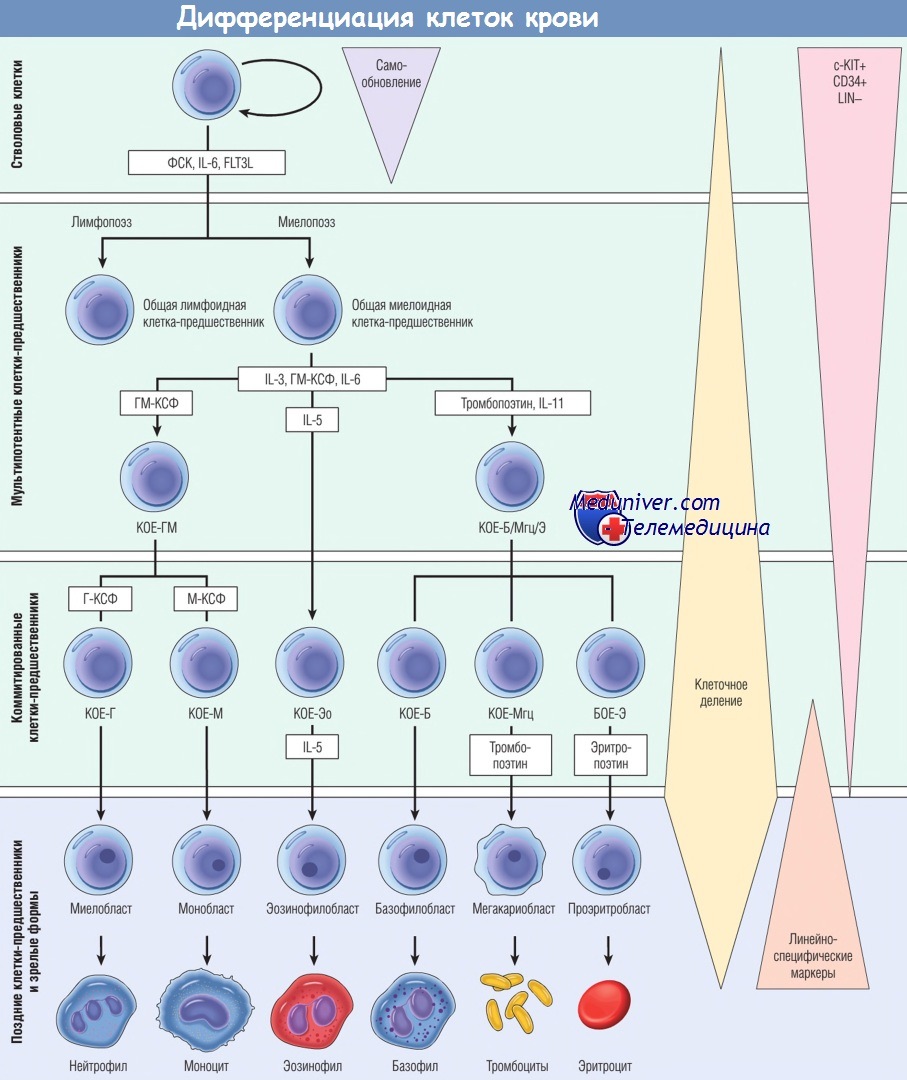
FLT3L — лиганд FLT3; IL — интерлейкин; LIN - отрицательный по линейно-специфическим маркерам;
БОЕ-Э — бурстообразующая единица эритроцитов; Г-КСФ — гранулоцитарный колониестимулирующий фактор;
ГМ-КСФ — гранулоцитарно-макрофагальный колониестимулирующий фактор; КОЕ-Б — колониеобразующая единица базофилов;
КОЕ-Г — колониеобразующая единица гранулоцитов; КОЕ-ГМ — колониеобразующая единица гранулоцитов и моноцитов;
КОЕ-М — колониеобразующая единица моноцитов; КОЕ-Мгц — колониеобразующая единица мегакариоцитов;
КОЕ-Э — колониеобразующая единица эритроцитов; КОЕ-Эо — колониеобразующая единица эозинофилов;
М-КСФ — макрофагальный колониестимулирующий фактор; ФСК — фактор стволовых клеток.
Учебное видео - общий анализ крови в норме и при болезни
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) лейкопении и агранулоцитоза"
Оглавление темы "Патогенез болезней":- Механизмы развития (патогенез) метастазов опухолей в сердце
- Механизмы развития (патогенез) осложнений трансплантации сердца
- Образование клеток крови (дифференцировка)
- Механизмы развития (патогенез) лейкопении и агранулоцитоза
- Механизмы развития (патогенез) лейкоцитоза
- Механизмы развития (патогенез) лимфаденита
- Механизмы развития (патогенез) неоплазий лейкоцитов
- Механизмы развития (патогенез) лимфоцитарного лейкоза и лимфомы
- Механизмы развития (патогенез) острого лимфоцитарного лейкоза
- Механизмы развития (патогенез) хронического лимфоцитарного лейкоза

