Морфология инфаркта миокарда
Развитие морфологических изменений во времени при остром ИМ и последующей организации поражения представлено в таблице ниже.
Почти все трансмуральные инфаркты захватывают по меньшей мере часть левого желудочка (в т.ч. свободную стенку и межжелудочковую перегородку) и почти всю зону кровоснабжения окклюзированной артерии, оставляя лишь узкий ободок (0,1 мм) сохранного субэндокардиального миокарда, жизнеспособность которого поддерживается диффузией кислорода и питательных веществ из желудочка.
15-50% ИМ, вызванных обструкцией правой коронарной артерии, распространяются от задней части свободной стенки левого желудочка до смежной стенки правого желудочка. Изолированный инфаркт правого желудочка возникает редко (в 1-3% случаев), как и инфаркт предсердий.
Частота поражения каждой из трех основных артерий и соответствующие области повреждения миокарда, приводящего к инфаркту (при типичной правосторонней доминантной циркуляции):
• передняя нисходящая артерия (40-50%): инфаркт захватывает переднюю стенку левого желудочка поблизости от верхушки, переднюю часть межжелудочковой перегородки, верхушку по окружности;
• правая коронарная артерия (30-40%): инфаркт локализуется в нижней/задней стенке левого желудочка, задней части межжелудочковой перегородки, в некоторых случаях в нижней/задней свободной стенке правого желудочка;
• огибающая артерия (15-20%): инфаркт поражает латеральную стенку левого желудочка, за исключением области у верхушки.

выявленный гистохимически по отсутствию окрашивания области некроза (стрелка) хлоридом трифенилтетразолия из-за высвобождения дегидрогеназ после гибели клеток.
Обратите внимание на геморрагию из-за разрыва сердца и рубец на месте старого инфаркта (острие стрелки).
Ориентация препарата: задняя стенка сердца вверху.
Встречаются и другие локализации коронарных поражений, вызывающих инфаркт, например поражение левой основной коронарной артерии, вторичных ветвей передней нисходящей артерии или маргинальных ветвей левой огибающей артерии.
Макро- и микроскопическая картина инфаркта миокарда (ИМ) зависит от продолжительности жизни пациента после события. Области повреждения подвергаются последовательным прогрессирующим морфологическим изменениям, которые начинаются с типичного ишемического коагуляционного некроза (преобладающий механизм клеточной смерти при ИМ, хотя возможен также апоптоз) и переходят в воспаление и репарацию, протекающие очень сходно с ответом тканей на повреждение в других участках организма.
Диагностика острого инфаркта миокарда (ИМ) на ранней стадии (как прижизненная, так и посмертная) может быть затруднена, особенно если смерть наступила в первые несколько часов после появления симптомов. При макроскопическом исследовании изменения обнаруживают в случае смерти пациента через 12 час после начала ИМ, но если пациент умер через 2-3 час, то возможно определить область некроза, погрузив срез миокарда в раствор хлорида трифенилтетразолия.
Такое гистохимическое окрашивание придает красно-коричневый цвет интактному, не пораженному миокарду, где сохраняется активность дегидрогеназ (в частности, лактатдегидрогеназы). Поскольку дегидрогеназы высвобождаются из мертвых клеток через поврежденные мембраны, область инфаркта остается неокрашенной, бледной зоной. Через 12-24 час ИМ можно идентифицировать макроскопически на поперечных срезах как область синевато-коричневого цвета из-за застоя крови.
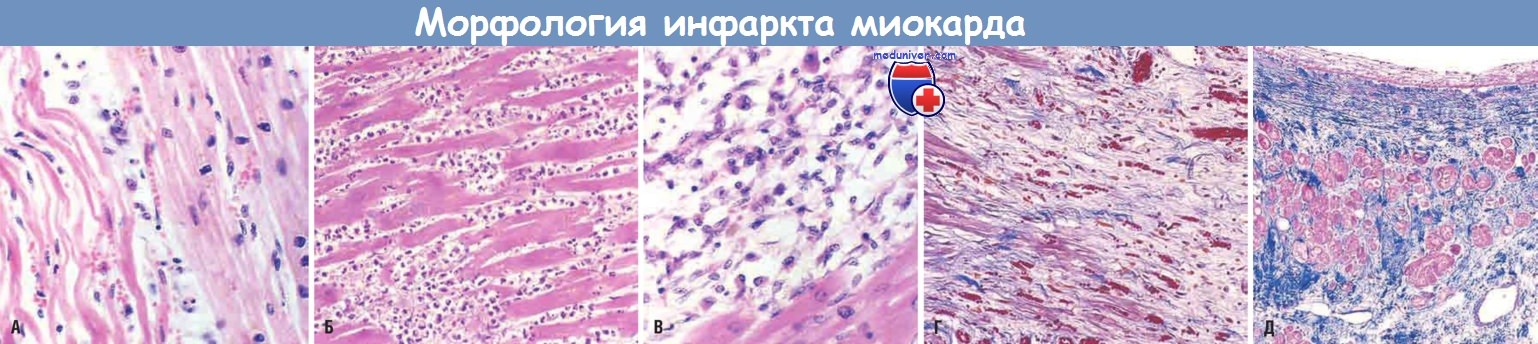
(А) Через сутки после инфаркта. Видны коагуляционный некроз и извитые кардиомиоциты (удлиненные и узкие по сравнению с расположенными справа сохранными кардиомиоцитами).
Расширенные пространства между погибшими клетками содержат отечную жидкость и нейтрофилы.
(Б) Через 3-4 сут после инфаркта. Плотный полиморфно-ядерный лейкоцитарный инфильтрат в области острого инфаркта миокарда.
(В) Через 7-10 сут после инфаркта. Почти полное удаление некротических клеток путем фагоцитоза.
(Г) Грануляционная ткань характеризуется присутствием рыхлого коллагена и обилием капилляров.
(Д) Заживший инфаркт с замещением некротических клеток плотным коллагеновым рубцом.
Видны немногочисленные оставшиеся кардиомиоциты.
После 24 час миокард в области инфаркта становится дряблым, желтовато-коричневого цвета, а зона ИМ приобретает более четкие границы. Через 10-14 сут зону ИМ окаймляет зона гиперемии из высоковаскуляризованной грануляционной ткани. На протяжении последующих недель у выжившего пациента в пораженной области формируется рубец.
Последовательность развития гистологических изменений вполне предсказуема. Типичные изменения, свойственные коагуляционному некрозу, можно увидеть при микроскопическом исследовании в первые 6-12 час после ИМ. На периферии зоны инфаркта могут присутствовать так называемые волны извитости.
Такие изменения, вероятно, обусловлены интенсивным воздействием сокращающихся жизнеспособных кардиомиоцитов на прилегающие к ним погибшие кардиомиоциты, которые растягиваются с образованием извитости. По краям инфаркта можно обнаружить сублетальные ишемические изменения — вакуольную дегенерацию, или миоцитолиз, — в виде крупных внутриклеточных вакуолей, содержащих, вероятно, воду. Некротические клетки вызывают острое воспаление, достигающее максимума за 1-3 сут.
После этого макрофаги удаляют некротические кардиомиоциты (этот процесс наиболее выражен на 3-7-е сутки), и область повреждения постепенно замещается высоковаскуляризованной грануляционной тканью (наиболее интенсивный процесс идет в течение 1-2 нед). По мере заживления грануляционная ткань замещается фиброзной. В большинстве случаев рубцевание завершается к концу 6-й недели, однако эффективность репарации зависит от размеров поражения.
В процессе заживления участвуют воспалительные клетки, мигрирующие в область повреждения через интактные кровеносные сосуды, которые часто сохраняются только по краям инфаркта. Именно поэтому репарация идет от краев инфаркта к его центру. Инфаркт в конце процесса репарации может оказаться неоднородным по структуре — заживление наиболее выражено на периферии. Как только репарация повреждения завершается, возраст рубца определить невозможно: плотный рубец спустя 8 нед после инфаркта и через 10 лет после него будет выглядеть одинаково.
Инфаркт может распространяться за пределы первоначальной границы в течение нескольких дней или недель в результате рецидивирующего некроза в прилегающих областях (расширение инфаркта). В подобных случаях присутствует центральная область, где заживление произошло раньше (т.е. оно более выражено), чем на периферии инфаркта. Этим процесс расширения инфаркта отличается от описанной ранее картины простого инфаркта, когда репарация на периферии опережает таковую в центре инфаркта.
Расширение инфаркта может произойти в результате ретроградного распространения тромба, проксимального сосудистого спазма, приводящего к недостаточному кровотоку через участок умеренного стеноза, ухудшения сократимости сердца, отложения микроэмболов, состоящих из тромбоцитов и фибрина, или аритмий, нарушающих функцию сердца.

Видео этиология, патогенез инфаркта миокарда
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патофизиология) реперфузии инфаркта миокарда"
Оглавление темы "Патогенез ишемической болезни сердца":- Механизмы развития (патофизиология) ишемической болезни сердца
- Механизмы развития (патофизиология) стенокардии
- Механизмы развития (патофизиология) инфаркта миокарда
- Различия трансмурального и субэндокардиального инфаркта миокарда
- Морфология инфаркта миокарда
- Механизмы развития (патофизиология) реперфузии инфаркта миокарда
- Клиника и маркеры инфаркта миокарда
- Механизмы развития (патогенез) осложнений инфаркта миокарда
- Механизмы развития (патогенез) хронической ИБС
- Механизмы развития (патогенез) внезапной сердечной смерти
- Велосипед для похудения. Реально ли снизить вес велопрогулками?

