Механизмы развития (патогенез) множественной миеломы
Множественная миелома — это плазмоклеточная опухоль, характеризующаяся мультифокальным поражением скелета. При этом заболевании доминирует поражение костей, однако на поздних стадиях процесс может распространяться на лимфоузлы и экстранодальные ткани, в частности кожу. В западных странах на долю множественной миеломы приходится 1% летальных исходов от всех злокачественных опухолей. Заболевание чаще возникает у мужчин и лиц африканского происхождения, главным образом у лиц пожилого возраста (обычно в интервале 65-70 лет).
а) Молекулярный патогенез. Гены Ig в миелоидных клетках всегда несут признаки соматической гипермутации. Это позволяет предположить, что опухоль возникла из В-клетки, покинувшей герминативный центр и мигрировавшей в костный мозг, где она дифференцировалась в плазматическую клетку. Некоторые исследования указывают на то, что опухоль возникает из клеток, сходных со стволовыми и напоминающих малые В-лимфоциты, и основой сохранения опухоли служат сигналы, сгенерированные и передаваемые по пути Hedgehog, ответственному за самообновление.
Пролиферация и выживаемость миелоидных клеток зависят от некоторых цитокинов и особенно от IL-6. Это важный фактор роста для плазматических клеток, продуцируемый самими опухолевыми клетками и оседлыми стромальными клетками костного мозга. У пациентов с активным заболеванием в сыворотке крови обнаруживается высокий уровень IL-6, что является плохим прогностическим признаком. Рост и выживаемость миелоидных клеток повышаются также в результате их прямого физического взаимодействия со стромальными клетками костного мозга. Этот процесс может служить целью для новых терапевтических подходов.
Факторы, продуцируемые неопластическими плазматическими клетками, опосредуют разрушение костей — главный патологический признак множественной миеломы. Особое значение имеет продуцируемый миеломой MIР-1а, повышающий экспрессию лиганда рецептора-активатора ядерного фактора каппа В (RANKL) стромальными клетками костного мозга. MIР-1а, в свою очередь, активирует остеокласты. Другие факторы, высвобождаемые опухолевыми клетками, например модуляторы сигнального пути WNT, являются сильными ингибиторами функций остеобластов. Конечный результат — заметное повышение резорбции костей, ведущее к гиперкальциемии и патологическим переломам.
Во многих миеломах происходят перестройки гена тяжелых цепей Ig на хромосоме 14q32. В транслокации участвуют: рецептор фактора роста фибробластов типа 3 (FGFR3) на хромосоме 4р16 — ген, кодирующий активность рецептора тирозинкиназы, участвующий в регуляции пролиферации клеток; регуляторные гены клеточного цикла — ген циклина D1 на хромосоме llql3 и ген циклина D3 на хромосоме 6р21; ген фактора транскрипции c-MAF на хромосоме 16q23; ген, кодирующий фактор транскрипции MUM1/IRF4 на хромосоме 6р25. Дисрегуляция циклинов D наблюдается часто в связи с тем, что присутствуют два разных гена циклинов D.
Другая частая кариотипическая аномалия — делеции 13q. Исследование профиля экспрессии генов выявляет разнообразие хромосомных аберраций, что на молекулярном уровне подтверждает крайнюю гетерогенность миеломы.
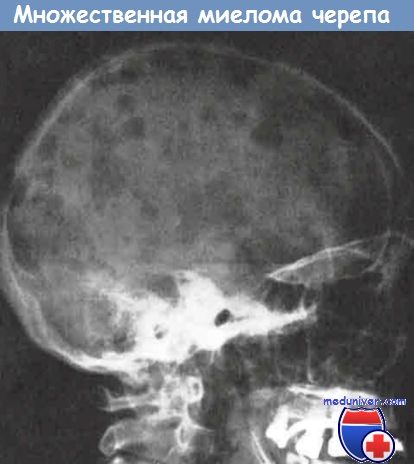
Четко видны дефекты в своде черепа.
б) Морфология. Множественная миелома представляет собой деструктивное плазмоклеточное новообразование осевого скелета. Чаще всего поражаются (в порядке убывания частоты): позвоночный столб, ребра, череп, таз, бедренная кость, ключица и лопатка. Первичная опухоль обычно образуется в костномозговой полости. Губчатое вещество кости подвергается эрозии, затем разрушается кортикальный слой кости, нередко приводя к патологическим переломам. В основном происходят переломы позвоночного столба, но возможны переломы любой пораженной кости.
На рентгенограмме поражения костей четко видны как очаговые дефекты диаметром 1-4 см, которые при макроскопическом исследовании представляют собой мягкую, желатинозную опухолевую ткань красного цвета. Реже наблюдается распространенное миеломатозное заболевание костей, приводящее к диффузной деминерализации (остеопении).
Даже в отсутствие опухолевой массы костный мозг содержит повышенное количество плазматических клеток (> 30%). Плазматические клетки могут инфильтрировать интерстиций или располагаться в виде пластов, полностью замещающих нормальные элементы. Злокачественные плазматические клетки, как и доброкачественные, имеют перинуклеарное просветление (хорошо развитый аппарат Гольджи) и эксцентрически расположенное ядро.
В ткани опухоли могут преобладать внешне относительно нормальные плазматические клетки, плазмобласты с ячеистым ядерным хроматином и хорошо заметным ядрышком или причудливые многоядерные клетки. Другие виды клеток появляются вследствие нарушения регуляции синтеза и секреции lg, что часто приводит к внутриклеточному накоплению интактных или частично деградированных белков. К таким вариантам относятся клетки с ярко-красной цитоплазмой, клетки Мотта с множеством гроздевидных цитоплазматических вакуолей и клетки, содержащие другие включения, в т.ч. фибриллы, палочковидные кристаллы и глобулы. Глобулярные включения представлены тельцами Русселя (в цитоплазме) или тельцами Датчера (в ядре).
В запущенных случаях инфильтраты, состоящие из плазматических клеток, могут присутствовать в селезенке, печени, почках, легких, лимфоузлах и других мягких тканях.
Обычно высокий уровень М-белка приводит к слипанию эритроцитов в мазках периферической крови с образованием так называемых монетных столбиков. Их формирование характерно, но неспецифично, т.к. они могут быть и при других нарушениях, связанных с повышенным уровнем lg (например, при СКВ и на ранних стадиях ВИЧ-инфекции). В редких случаях опухолевые клетки наполняют периферическую кровь, создавая картину плазмоклеточной лейкемии.
Белок Бенс-Джонса экскретируется почками и способствует развитию миеломной почки.
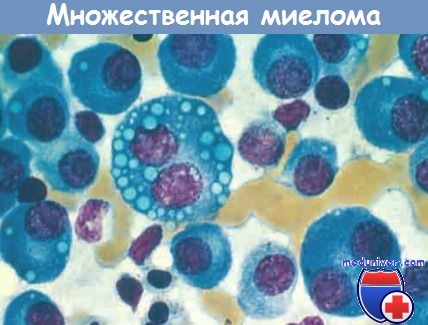
Клетки нормального костного мозга в значительной степени замещены плазматическими клетками,
включая формы с множественными ядрами, хорошо заметными ядрышками и цитоплазматическими вакуолями, содержащими Ig.
в) Клинические признаки. Клиническая картина множественной миеломы возникает вследствие
(1) роста плазматических клеток в тканях, особенно в костях;
(2) избыточной продукции Ig, часто обладающего аномальными физико-химическими свойствами;
(3) супрессии нормального гуморального иммунитета.
Резорбция костей приводит к патологическим переломам и хроническому болевому синдрому. Сопутствующая гиперкальциемия может вызвать неврологические проявления, в частности помрачение сознания, слабость и летаргию, запоры и полиурию и способствовать дисфункции почек. Снижение продукции нормальных Ig повышает восприимчивость организма к рецидивирующим бактериальным инфекциям. Клеточный иммунитет остается относительно интактным. Большое значение имеет почечная недостаточность как возможная причина летального исхода. Патогенез почечной недостаточности, которую имеют до 50% больных миеломой, многофакторный.
Наиболее важным фактором является протеинурия Бенс-Джонса, т.к. экскретируемые легкие цепи токсичны для эпителиальных клеток почечных канальцев. Некоторые легкие цепи (особенно семейств h6 и hЗ) склонны вызывать амилоидоз AL-типа, при котором усиливается дисфункция почек и амилоид откладываться в других тканях.
У 99% пациентов обнаруживают повышенный уровень Ig в сыворотке крови и/или легкие цепи Ig (белок Бенс-Джонса) в моче. Моноклональные Ig (М-белок) вначале определяют по аномальным белковым пикам на электрофореграммах крови и мочи, затем моноклональные Ig исследуют с помощью метода иммунофиксации. Большинство миелом ассоциируется с повышенным содержанием Ig в сыворотке (> 3 г/дл) и/или белка Бенс-Джонса в моче (> 6 г/дл). Наиболее распространенным типом моноклональных Ig является IgG (55%), затем следует IgA (25%). Довольно редко встречаются миеломы, экспрессирующие IgM, IgD или IgE.
Избыточная продукция и агрегация М-белка, особенно IgA или IgG3, у 7% пациентов приводят к развитию симптомов, обусловленных повышением вязкости крови (симптомы описаны при обсуждении лимфоплазмоцитарной лимфомы). Присутствие свободных легких цепей и М-белка в сыворотке одновременно наблюдается у 60-70% пациентов, в 20% случаев есть только легкие цепи. Около 1% миелом являются несекретирующими, т.е. отсутствие М-белка еще не исключает множественную миелому.
Клинико-патологическая диагностика множественной миеломы основывается на рентгенографических и лабораторных данных. Рентгенографические изменения позволяют предположить множественную миелому, однако для окончательного диагноза необходимо исследование костного мозга. Поражение костного мозга приводит к развитию нормоцитарной нормохромной анемии, иногда сопровождаемой умеренной лейкопенией и тромбоцитопенией.
Прогноз вариабелен, но в целом неблагоприятен. Медиана выживаемости составляет 4-6 лет. До настоящего времени заболевание не поддается полному излечению. Пациенты с множественными поражениями костей в отсутствие лечения редко живут более 12 мес, тогда как пациенты с «тлеющей» миеломой могут не иметь симптомов долгие годы. Транслокации с вовлечением циклина D1 ассоциируются с благоприятным исходом, тогда как делеции 13q, 17р и транслокация t(4;14) предвещают более агрессивное течение заболевания.
Цитотоксические агенты индуцируют ремиссию у 50-70% пациентов, и новые терапевтические подходы вселяют надежду. Миелоидные клетки чувствительны к ингибиторам протеасом — клеточных органелл, разрушающих дефектные и неправильно свернутые белки, активирующие апоптоз. Миелоидные клетки склонны накапливать неправильно свернутые, неспаренные Ig-цепи.
Ингибиторы протеасом способны усиливать эту присущую миелоидным клеткам склонность и индуцировать апоптоз, а также, по-видимому, замедлять резорбцию костей благодаря влиянию на стромальные клетки. Талидомид и его производные также обладают активностью против миеломы, возможно за счет изменения взаимодействия миелоидных и стромальных клеток костного мозга, а также подавления ангиогенеза. Бифосфонаты (лекарственные средства, ингибирующие резорбцию костей) снижают частоту патологических переломов и ограничивают гиперкальциемию. Трансплантация костного мозга увеличивает продолжительность жизни, однако терапевтический эффект этого вмешательства не доказан.
«Тлеющая» миелома занимает промежуточное положение между множественной миеломой и моноклональной гаммапатией неустановленной клинической значимости. Количество плазматических клеток достигает 10-30% общего числа клеток костного мозга, а уровень М-белка в сыворотке > 3 г/дл. Однако симптомов у пациентов нет. У 75% пациентов заболевание в течение 15 лет переходит в множественную миелому.

Для скрининга используют электрофорез белков сыворотки (SP).
Наличие поликлонального IgG в нормальной сыворотке на электрофореграмме отражается широкой полосой (стрелка)]
в отличие от этого сыворотка больного множественной миеломой дает в этой области электрофореграммы одиночную, четкую полосу (острие стрелки).
Для подтверждения моноклональности lg и его характеристик применяют метод иммунофиксации.
Белки, разделенные путем электрофореза в геле, реагируют со специфическими антисыворотками.
После основательного отмывания остаются перекрестно связанные с антисывороткой белки, которые определяют с помощью окрашивания.
Обратите внимание на четко выраженную полосу, образовавшуюся в результате перекрестной реакции с антисывороткой,
специфичной к тяжелой цепи IgG (G) и легкой цепи каппа (к); это указывает на присутствие М-белка IgGk.
Уровни поликлонального IgG, IgA (А) и легкой цепи лямбда (А) в сыворотке больного также снижены по сравнению с нормой — это типично для множественной миеломы.
- Рекомендуем ознакомиться со следующей статьей "Механизмы развития (патогенез) солитарной плазмоцитомы"
Оглавление темы "Патогенез болезней крови":- Механизмы развития (патогенез) фолликулярной лимфомы
- Механизмы развития (патогенез) диффузной В-клеточной лимфомы
- Механизмы развития (патогенез) лимфомы Беркитта
- Механизмы развития (патогенез) плазмоклеточных неоплазий
- Механизмы развития (патогенез) множественной миеломы
- Механизмы развития (патогенез) солитарной плазмоцитомы
- Механизмы развития (патогенез) моноклональной гаммапатии неустановленной значимости
- Механизмы развития (патогенез) лимфоплазмоцитарной лимфомы
- Механизмы развития (патогенез) лимфомы из клеток мантийной зоны
- Механизмы развития (патогенез) лимфомы из клеток маргинальной зоны

